2-Норборнил катион
В органической химии термин 2-норборнил-катион (или 2-бицикло[2.2.1]гептильный катион ) описывает один из трех карбокатионов, образующихся из производных норборнана . Хотя катионы 1-норборнила и 7-норборнила были изучены, наиболее обширные исследования и активные дебаты были сосредоточены на точной структуре катиона 2-норборнила.
2-норборнильный катион образуется из множества производных норборнана и реагентов. Первые сообщения о его образовании и реакционной способности, опубликованные Солом Уинштейном, вызвали споры по поводу природы его связи , поскольку он использовал трехцентровую двухэлектронную связь для объяснения стереохимического результата реакции. Герберт К. Браун оспорил это утверждение на том основании, что классические резонансные структуры могут объяснить эти наблюдения без необходимости адаптировать новый взгляд на связь. У взглядов обоих исследователей были свои сторонники, и десятки ученых провели изобретательно спланированные эксперименты, чтобы предоставить доказательства той или иной точки зрения. Со временем спор становился все более ожесточенным и ожесточенным, и дебаты приняли личный или ad hominem характер. [1]
Доказательства неклассической природы 2-норборнильного катиона росли в течение нескольких десятилетий, в основном за счет спектроскопических данных, собранных с использованием таких методов, как ядерный магнитный резонанс (ЯМР). Кристаллографическое подтверждение его неклассической природы пришло только в 2013 году. [2] Хотя большинство химиков сейчас согласны с тем, что 2-норборнильный катион сам по себе не является классическим, также широко признано, что энергетический ландшафт карбокатионов имеет тенденцию быть «плоским», причем многие потенциальные структуры различаются лишь незначительно по энергии. Конечно, не все бициклические карбокатионы неклассические; разница в энергии между классическими и неклассическими структурами часто тонко сбалансирована. Таким образом, теперь известно, что некоторые алкилзамещенные 2-бицикло[2.2.1]гептильные катионы принимают классические структуры.
Природа связи в 2-норборнильном катионе включила множество новых идей в понимание химических связей. Можно увидеть сходство между этим катионом и другими, такими как бораны .
Теория [ править ]
Природа связи в 2-норборнильном катионе была центром энергичных и известных дебатов в химическом сообществе в середине двадцатого века. В то время как большинство химиков полагали, что трехцентровая двухэлектронная связь лучше всего отображает электронную структуру основного состояния , другие утверждали, что все данные, касающиеся 2-норборнильного катиона, можно объяснить, изображая его как быстро уравновешивающую пару катионов.
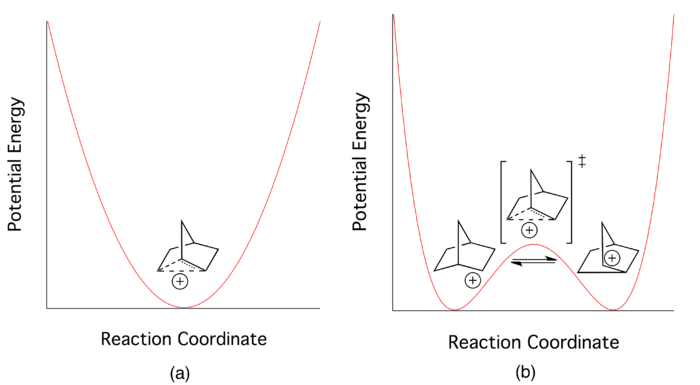
В разгар дебатов все химики согласились, что делокализованная картина электронной связи может быть применена к 2-норборнильному катиону. Но это не дало ответа на фундаментальный вопрос, вокруг которого зависели дебаты. Исследователи продолжали искать новые способы определить, описывает ли трехцентровая делокализованная картина низкоэнергетическое переходное состояние (седловая точка на многомерной поверхности потенциальной энергии ) или сам по себе минимум потенциальной энергии. [1] Сторонники «классической» картины считали, что система лучше всего описывается двухъямным потенциалом с очень низким барьером, в то время как сторонники «неклассического» лагеря предполагали, что делокализованное электронное состояние описывает единственную потенциальную энергетическую яму. [3]
неклассическая картина Гиповалентность :

Сторонники неклассической природы стабильного 2-норборнильного катиона обычно описывают виды, используя либо резонансные структуры , либо одну структуру с частичными связями ( см. Рисунок 2 ). Это гиповалентное взаимодействие можно представить как суммарный эффект i) частичной сигма-связи между атомами углерода 1 и 6, ii) частичной сигма-связи между атомами углерода 2 и 6 и iii) частичной пи-связи между атомами углерода 1 и 2. [4] Каждая частичная связь представлена как полная связь в одной из трех резонансных структур или как пунктирная частичная связь, если катион изображен через одну структуру.

Были некоторые споры о том, какой вклад резонансная структура с пи-связями на самом деле способствует делокализованной электронной структуре. [6] Через 1 Рука 13 С ЯМР-спектроскопией было подтверждено, что значительный положительный заряд лежит на метиленовом углероде 6. [7] Это удивительно, поскольку первичные карбокатионы гораздо менее стабильны, чем вторичные. Однако 2-норборнильный катион может образовываться из производных β-(Δ 3 -циклопентенил)-этан, что указывает на то, что резонансная структура с пи-связями имеет важное значение. [8]
Катион 2-норборнил был одним из первых примеров неклассического иона . Неклассические ионы можно определить как органические катионы, в которых электронная плотность заполненной связывающей орбитали распределяется по трем или более центрам и содержит некоторый характер сигма-связи. [9] Катион 2-норборнила рассматривается как прототип неклассических ионов. Другие простые катионы, такие как протонированный ацетилен (этиний, C
22Ч +
3 ), протонированный этилен (этений, C
22Ч +
5 ) и протонированный этан (этан, C
22Ч +
7 ), как было показано, лучше всего описывается как неклассический с помощью инфракрасной спектроскопии. [10]
Наиболее часто предлагаемое изображение молекулярной орбитали 2-норборнильного катиона показано на рисунке 3. Две орбитали p- типа, по одной на каждом из атомов углерода 1 и 2, взаимодействуют с sp 3 -гибридизированная орбиталь углерода 6 с образованием гиповалентной связи. [5] [11] Расчеты расширенной теории Хюккеля для 2-норборнильного катиона предполагают, что орбиталь углерода 6 вместо этого может быть sp 2 -гибридизированы, хотя это влияет только на геометрию геминальных атомов водорода. [12]
классическая картина Быстрое равновесие :

По мнению сторонников классического двухямного потенциала, 2-норборнильный катион существует в динамическом равновесии между двумя энантиомерными асимметричными структурами. Делокализованный вид, центральный в неклассической картине, представляет собой всего лишь переходное состояние между двумя структурами. Перегруппировки Вагнера-Меервейна используются как механизм преобразования двух энантиомеров ( см. рисунок 4 ).
Попытки изолировать асимметричные виды спектроскопически обычно безуспешны. Сообщается, что основной причиной этой неудачи является чрезвычайно высокая скорость прямой и обратной реакции , что указывает на очень низкий потенциальный барьер для взаимного превращения между двумя энантиомерами. [4]
неклассическая структура : еще одна Нортрициклоний
Некоторые химики также считают, что 2-норборнильный катион лучше всего представлен ионом нортрициклония, C 3 -симметричным протонированным нортрицикленом. Это изображение было впервые использовано для частичного объяснения результатов эксперимента. 14 C. по скремблированию изотопа Эксперимент [13] Молекулярно-орбитальное представление этой структуры включает синфазное взаимодействие между sp 2 -гибридизированные орбитали атомов углерода 1, 2 и 6 и 1s-орбиталь атома общего атома водорода ( см. рисунок 5 ). [14]

История [ править ]
Неклассические ионы [ править ]
Неклассические ионы отличаются от традиционных катионов своей электронной структурой : хотя химические связи обычно изображаются как обмен электронами между двумя атомами, стабильные неклассические ионы могут содержать три или более атомов, которые имеют одну общую пару электронов. [9] В 1939 году Томас Невелл и другие попытались выяснить механизм превращения гидрохлорида камфена в изоборнилхлорид . В одном из предложенных механизмов реакции, изображенных в статье, положительный заряд промежуточного катиона приписывался не отдельному атому, а структуре в целом. [15] Позже противники неклассического описания назвали это первым случаем использования неклассического иона. [16] Однако термин «неклассический ион» явно не появился в химической литературе до тех пор, пока более десяти лет спустя он не был использован для обозначения делокализованной связи в пирамидальном бутильном катионе. [17]
Термин «синартетический ион» также использовался для описания делокализованных связей в стабильных карбокатионах до того, как термин «неклассический ион» получил широкое распространение. Первые пользователи этого термина отмечали поразительное сходство между связью в этих типах катионов и связью в борогидридах . [18]
неклассические предложения Первые
В 1949 году Сол Уинстейн заметил, что 2- экзо -норборнилброзилат ( п- бромбензолсульфонат) и 2- эндо - норборнилтозилат ( п- дают рацемическую смесь одного и того же продукта — 2- - норборнилацетата экзо толуолсульфонат) при ацетолизе ( см. Рисунок 6 ). Поскольку тозилаты и брозилаты одинаково хорошо действуют как уходящие группы , он пришел к выводу, что и 2- эндозамещенный , и 2- экзозамещенный норборнан должны проходить через общий катионный промежуточный продукт с доминирующей экзо- реактивностью. Он сообщил, что это промежуточное соединение, скорее всего, представляет собой симметричный делокализованный 2-норборнильный катион. [19] Позже с помощью газофазной хроматографии было показано, что количество эндоэпимера полученного продукта составляет менее 0,02%, что доказывает высокую стереоселективность реакции. [20]


Когда одиночный энантиомер 2 -экзо не наблюдается оптической активности -норборнилброзилата подвергается ацетолизу, в образующемся 2- экзо -норборнилацетате ( см. фигуру 7 ). [19] При неклассическом описании 2-норборнильного катиона присутствующая плоскость симметрии (проходящая через атомы углерода 4, 5 и 6) обеспечивает равный доступ к обоим энантиомерам продукта, что приводит к наблюдаемой рацемической смеси .
Было также обнаружено, что 2- экзо -замещенные норборнаны реагируют в 350 раз быстрее, чем соответствующие эндо- изомеры. Анхимерное содействие сигма-связи между атомами углерода 1 и 6 было объяснено как объяснение этого кинетического эффекта. [19] Важно отметить, что использование анхимерной помощи побудило многих химиков постулировать, что энергетическая стабильность 2-норборнильного катиона напрямую связана с симметричной мостиковой структурой, используемой в неклассическом объяснении. Однако некоторые другие авторы предложили альтернативные объяснения высокой стабильности, не ссылаясь на неклассическую структуру. [1]
В 1951 году было впервые высказано предположение, что 2-норборнильный катион можно лучше описать, если рассматривать его как ион нортрициклония. [13] Было показано, что основным продуктом, образующимся в результате реакции отщепления 2-норборнильного катиона, является нортрициклен (а не норборнен), но утверждается, что это подтверждает оба постулата о неклассических ионах. [20]
Герберт С. Браун мнение особое :
Герберт К. Браун не считал необходимым использовать новый тип связей в стабильных промежуточных соединениях, чтобы объяснить интересную реакционную способность 2-норборнильного катиона. Критикуя многих химиков за игнорирование прошлых объяснений реакционной способности, Браун утверждал, что всю вышеупомянутую информацию о 2-норборнильном катионе можно объяснить, используя простые стерические эффекты, присутствующие в норборнильной системе. [4] Учитывая, что альтернативное объяснение, использующее быстро уравновешивающую пару ионов для описания 2-норборнильного катиона, было верным, он не видел необходимости ссылаться на стабильное, неклассическое описание связи. [21] Использование стабильных неклассических ионов становилось обычным явлением; Браун считал, что это не только неоправданно, но и контрпродуктивно для области химии в целом. Действительно, многие статьи, в которых сообщалось о стабильных неклассических ионах, были позже отозваны как нереалистичные или неверные. [3] Опубликовав эту противоречивую точку зрения в 1962 году, Браун начал поиск экспериментальных доказательств, несовместимых с делокализованной картиной связи в 2-норборнильном катионе. [22]
Браун также работал над доказательством нестабильности делокализованной электронной структуры 2-норборнильного катиона. Если бы можно было доказать, что неклассический ион имеет более высокую энергию, чем соответствующая классическая ионная пара, то неклассический ион можно было бы рассматривать только как переходное состояние между двумя асимметричными катионами. [3] [23] Хотя он не исключал возможности делокализованного переходного состояния, Браун продолжал отвергать предложенную отражательную симметрию 2-норборнильного катиона даже в конце своей карьеры. [24]
Влияние [ править ]
Введение трехцентровой двухэлектронной делокализованной связи, возникшей в неклассической картине 2-норборнильного катиона, позволило химикам исследовать совершенно новую область химических связей. Химики стремились применить характеристики гиповалентных электронных состояний как к новым, так и к старым системам (хотя некоторые слишком увлеклись). [6] Одной из наиболее фундаментально важных концепций, возникших в результате интенсивных исследований, посвященных неклассическим ионам, была идея о том, что электроны, уже участвующие в сигма-связях, могут участвовать в реакционной способности. Хотя было известно, что заполненные пи-орбитали являются донорами электронов , химики сомневались, что сигма-орбитали могут функционировать в том же качестве. Неклассическое описание 2-норборнильного катиона можно рассматривать как донорство электронной пары из сигма-связи углерод-углерод в пустую p-орбиталь углерода 2. Таким образом, этот карбокатион показал, что донорство электронов сигма-связи происходит как вполне вероятно как донорство электронов по пи-связи. [25] [26]
Интенсивные дебаты, последовавшие за вызовом Брауна сторонникам неклассических ионов, также оказали большое влияние на область химии. Чтобы доказать или опровергнуть неклассическую природу 2-норборнильного катиона, химики по обе стороны дискуссии ревностно искали новые методы химической характеристики и более инновационные интерпретации существующих данных. [27] Одним из спектроскопических методов, получивших дальнейшее развитие для исследования 2-норборнильного катиона, стала спектроскопия ядерного магнитного резонанса соединений в сильнокислых средах. [1] Сравнение 2-норборнильного катиона с нестабильными переходными состояниями с делокализованными электронными состояниями часто проводилось при попытке выяснить, стабильна или нет норборнильная система. Эти усилия побудили более тщательное исследование переходных состояний и значительно расширили понимание научным сообществом их электронной структуры. [27] Короче говоря, энергичная конкуренция между научными группами привела к обширным исследованиям и лучшему пониманию основных химических концепций.
Формирование [ править ]
2-норборнильный катион можно получить множеством синтетических путей. Эти маршруты можно сгруппировать в три разных класса: σ Формирование , π Формирование и Формирование путем перестановки . Каждый из них обсуждается отдельно ниже.

σ обучение [ править ]
Исходным материалом для этого пути является производное норборнана с хорошей уходящей группой в положении 2. Если уходящая группа находится на экзо -грани, электронная плотность из σ-связи между атомами углерода 1 и 6 передается в σ* -антисвязь между атомами углерода. 2 и уходящая группа ( см. рисунок 8б ). [28]
Если уходящая группа находится на эндофасе , то уходящая группа сначала уходит сама. Затем электронная плотность от σ-связи между атомами углерода 1 и 6 передается в образовавшуюся пустую атомную орбиталь на углероде 2. Однако этот путь образования гораздо медленнее, чем у экзо -изомера, поскольку σ-связь не может оказать анхимерную помощь для первого шаг, что делает энергию активации первого переходного состояния намного выше. Кроме того, если в реакционной смеси имеется высокая концентрация реакционноспособных электрофилов, образование вновь замещенного производного норборнана может препятствовать образованию неклассических ионов. [19] [29]
Примером такого пути образования является реакция, которая побудила Уинштейна и Трифана предложить делокализованную структуру 2-норборнильного катиона. 2-норборнилтозилаты и брозилаты образуют 2-норборнильный катион этим путем в качестве промежуточного продукта сольволиза . [19]
π тренировка [ править ]
Исходным материалом для этого пути является β-(Δ 3 Производное -циклопентенил)этана с хорошей уходящей группой на концевом атоме углерода этановой группы. Электронная плотность от π-связи алкенового фрагмента передается в σ*-антисвязь между концевым углеродом и уходящей группой ( см. рисунок 8c ). [28] [29]
Например, основной продукт ацетолиза β-(Δ 3 -циклопентенил)-этилнозилат ( п- нитробензолсульфонат) представляет собой 2- экзо -норборнилацетат. Недостаток β-(Δ 3 Присутствие -циклопентенил)-этилацетата после реакции объясняется большей стабильностью норборнильной системы по сравнению с декорированной циклопентенильной системой. [8]
Этот путь эффективен только в том случае, если циклопентенилолефин изолирован от любой более крупной системы с π-связями. Скорость реакции существенно снижается, если задействованная двойная связь образует шестичленное ароматическое кольцо, как это происходит в 2-инданилэтилнозилате. Было замечено, что алкильные замены в олефинах увеличивают скорость реакции за счет стабилизации образующегося карбокатиона. [30]
1-норборнильных и 7-норборнильных в результате перегруппировки катионов Образование
Катион 2-норборнила также может образовываться путем перегруппировки подобных ионов, таких как катионы 1-норборнила и 7-норборнила, хотя они, как правило, не так хорошо изучены. Эксперименты по мечению радиоактивным изотопом углерода-14 показали, что сложный скремблинг в системах норборнильных катионов позволяет 14 C должен присутствовать во всех семи положениях норборнильной системы. [13] При циклическом изменении низких и высоких температур во время гидролиза 1- и 7-хлорнорборнанов наблюдалось большое количество 2-норборнанола в дополнение к ожидаемым 1- и 7-норборнанолам соответственно. Таким образом, 1- и 7-норборнильные катионы обладают неким механизмом, с помощью которого они могут перегруппировываться в более стабильный 2-норборнильный катион во времени реакций сольволиза. [31]
Геометрия [ править ]
доказательства Спектроскопические
Одним из способов проверки того, является ли 2-норборнильный катион неклассическим, является исследование внутренней симметрии катиона. Многие спектроскопические инструменты, такие как спектроскопия ядерного магнитного резонанса (спектроскопия ЯМР) и спектроскопия комбинационного рассеяния света , дают подсказки об отражательной и вращательной симметрии, присутствующей в молекуле или ионе. Каждая из трех предложенных структур 2-норборнильного катиона демонстрирует разную молекулярную симметрию. Неклассическая форма содержит плоскость отражения, проходящую через атомы углерода 4, 5, 6 и среднюю точку атомов углерода 1 и 2. Классическая форма не содержит ни отражательной, ни вращательной симметрии. Структура протонированного нортрициклена содержит C 3 -симметричную ось вращения через углерод 4.
Каждый пик спектра ЯМР соответствует набору атомов определенного элемента, находящихся в сходном химическом окружении. Спектр ЯМР соли хлорпентафторида сурьмы 2-норборнильного катиона бесполезен при комнатной температуре, поскольку гидридные сдвиги происходят быстрее, чем временные рамки эксперимента ЯМР; Таким образом, большая часть атомов водорода рассматривается как эквивалентная и учитывается в одном и том же пике поглощения. При понижении температуры эксперимента ЯМР до -60 ° C гидридные сдвиги «замораживаются», и из спектра можно получить больше структурной информации. Исследователи обнаружили, что при таких низких температурах 1 Спектр ЯМР Н соответствовал ожидаемому для неклассической структуры иона. [31] [32]
1 Рука 13 Исследования ЯМР 1C смогли подтвердить, что любые предполагаемые перегруппировки Вагнера-Меервейна происходили быстрее, чем временные рамки эксперимента ЯМР, даже при низких температурах. [33] Для молекул, находящихся в статическом равновесии относительно перегруппировок, ЯМР показывает, сколько наборов ядер, связанных с симметрией, имеется в молекуле и сколько ядер приходится на каждый из этих наборов, посредством интегрирования спектра. Для молекул, находящихся в динамическом равновесии, таких как 2-норборнильный катион, ядра внутри каждого набора также могут превращаться друг в друга посредством перегруппировок с высокой скоростью реакции. [34] Поскольку предложенное динамическое равновесие сторонников классических ионов имело очень высокие скорости перегруппировки, первые исследования ЯМР не подтвердили и не опровергли ни одну из трех предложенных структур. [7] Но с помощью твердотельного ЯМР- анализа можно снизить температуру эксперимента ЯМР до 5 кельвинов (-268 ° C) и, таким образом, значительно замедлить любые явления перегруппировки. Твердотельный 13 Спектры ЯМР 13С 2-норборнильного катиона показывают, что атомы углерода 1 и 2 находятся в одинаковом химическом окружении, что согласуется лишь с неклассической картиной 2-норборнильного катиона. [35]
Спектры комбинационного рассеяния 2-норборнильного катиона показывают более симметричные виды, чем можно было бы ожидать для пары быстро уравновешивающих классических ионов. Поскольку предполагаемые скорости реакций классических перегруппировок ионов медленнее, чем временная шкала комбинационного рассеяния света, можно было бы ожидать, что спектры комбинационного рассеяния света укажут на менее симметричные виды, если классическая картина верна. [6]
Некоторые исследования 13 ЯМР 1С особенно благоприятствует интерпретации через структуру протонированного нортрициклена. [36] Кроме того, в спектрах комбинационного рассеяния 2-норборнильного катиона в некоторых кислых растворителях наблюдается полоса поглощения при 3110 см-1. -1 указывает на обедненное электронами циклопропановое кольцо. Поскольку такую полосу поглощения можно было бы ожидать в C 3 -симметричном протонированном нортрициклене, некоторые ученые заявили, что это является убедительным доказательством такой интерпретации. [37] Другие химики постулировали, что свойства 2-норборнильного катиона очень зависят от среды растворителя. Хотя высокая кислотность и низкая нуклеофильность растворителей, использованных в вышеупомянутых экспериментах, могут привести к тому, что геометрия протонированного нортрицилкония будет наиболее стабильной, эта геометрия не обязательно должна быть наиболее энергетически выгодной в других растворителях. [6]
Расчеты [ править ]
Для сравнения осуществимости различных предложенных геометрий было использовано множество расчетных исследований. Используя квантовый полуэмпирический метод MINDO/3 , исследователи не смогли сделать вывод, какая геометрия 2-норборнильного катиона является наиболее энергетически выгодной. Однако классическая структура оказалась единственным потенциальным минимумом для алкилзамещенного 2-метил-2-норборнильного катиона. [38] Было обнаружено, что дополнительные расчеты с использованием расширенной теории Хюккеля для молекулярных орбиталей подтверждают неклассическую геометрию катиона с отражательной симметрией. [12] [39]
Термодинамика [ править ]
В некоторых исследованиях использовались интересные сравнения, чтобы проверить энергетическую стабильность 2-норборнильного катиона, обеспечиваемую его делокализованной природой. Сравнивая перегруппировку между 3-метил-2-норборнильным катионом и 2-метил-2-норборнильным катионом с перегруппировкой между третичными и вторичными изопентановыми карбокатионами, можно обнаружить, что изменение энтальпии примерно на 6 ккал/моль меньше для норборнила. система. Поскольку основное различие между этими двумя обратимыми перегруппировками заключается в степени возможной делокализации в основном электронном состоянии, стабилизацию 3-метил-2-норборнильного катиона можно объяснить его неклассической природой. [40] Однако в некоторых экспериментальных исследованиях такую стабилизацию в реакциях сольволиза обнаружить не удалось. [3]
Другие исследования стабильности 2-норборнильного катиона показали, что алкильные замещения у углерода 1 или 2 делают систему явно классической. Третичные карбокатионы гораздо более стабильны, чем их вторичные аналоги, и поэтому им не требуется делокализованная связь, чтобы достичь минимально возможной потенциальной энергии. [41] [42]
Кинетика [ править ]
Чтобы обосновать свое предположение о неклассической природе 2-норборнильного катиона, Уинштейн и Трифан сначала использовали кинетические доказательства увеличения скорости реакции образования 2- экзо -норборнильного катиона по сравнению с 2- эндо -норборнильным катионом. [19] Другие исследователи исследовали скорость реакции соединений, которые могли бы проявлять анхимерную помощь, но не могли подвергаться перегруппировке, поскольку норборнильная система могла демонстрировать аналогичные тенденции к увеличению скорости. Некоторые утверждают, что это является окончательным доказательством неклассической картины. [43] Но не все согласны. Другие исследователи обнаружили, что производные циклопентана, структурно подобные норборнильной системе, по-прежнему демонстрируют повышенную скорость реакции, что привело их к утверждению, что классический норборнильный катион гораздо лучше описывает систему. [44] [45]
Эксперименты изотопов маркировке по

Эксперименты по мечению радиоактивными изотопами представляют собой мощный инструмент для определения структуры органических молекул. Систематически разлагая 2-норборнильный катион и анализируя количество радиоактивного изотопа в каждом продукте разложения, исследователи смогли продемонстрировать дополнительные доказательства неклассической картины делокализованной связи ( см. рисунок 9 ). Сторонники неклассической картины ожидают, что 50% образовавшегося CO 2 при разложении на рисунке 9 будет содержать 14 C, в то время как сторонники классической картины ожидают, что большая часть образовавшегося CO 2 будет радиоактивной из-за короткоживущей природы катиона. Было обнаружено, что 40% углекислого газа, образующегося в результате разложения, радиоактивны, что позволяет предположить, что неклассическая картина более правильна. [14]
Дальнейшее различие между неклассической и классической структурой 2-норборнильного катиона возможно путем объединения экспериментов ЯМР с экспериментами по мечению изотопов. Изотопное замещение одного из двух атомов дейтерия на атом водорода приводит к резкому изменению окружения близлежащих ЯМР-активных атомов. Асимметричное мечение изотопом дейтерия (замещение) приведет к тому, что набор атомов углерода, которые были эквивалентны у полностью водородных видов, будет разделен на два или более набора эквивалентных атомов углерода у видов, меченных дейтерием; это будет проявляться в спектре ЯМР как один пик в спектре полностью водородных частиц, превращающийся, по крайней мере, в два «расщепленных» пика в дейтеромеченных соединениях. Если система находится в состоянии быстрого равновесия со скоростью, превышающей временную шкалу 13 В эксперименте ЯМР С соответствующий пик будет резко разделен (порядка 10-100 м.д.). Если вместо этого система статична, пик будет разделен очень незначительно. [46] [47] 13 Спектр ЯМР 1С 2-норборнильного катиона при -150 °C показывает, что пики, соответствующие атомам углерода 1 и 2, разделены менее чем на 10 ppm (частей на миллион) при проведении этого эксперимента, что указывает на то, что система не подвергается быстрое равновесие, как в классической картине. [48]
Рентгеновская кристаллография [ править ]
Хотя характеристика кристаллов 2-норборнильного катиона, возможно, существенно препятствовала дальнейшим дебатам о его электронной структуре, он не кристаллизуется ни при каких стандартных условиях. Недавно кристаллическая структура была получена и описана творческим способом: добавление трибромида алюминия к 2-норборнилбромиду в дибромметане при низких температурах привело к образованию кристаллов [ C
7 ч.
11 ] + [ Ал
22 комн.
7 ] − · СН
22 комн.
2 . [2] Изучая полученную кристаллическую структуру, исследователи смогли подтвердить, что кристаллическая геометрия лучше всего подтверждает делокализованную связь в стабильном 2-норборнильном катионе. Было обнаружено, что длины связей между «мостиковым» углеродом 6 и каждым из атомов углерода 1 и 2 немного длиннее, чем типичные алкановые связи. Согласно неклассической картине, для этих связей можно было бы ожидать порядка связей от 0 до 1, что означает, что это хорошо объясняет кристаллическую структуру. Сообщалось, что длина связи между атомами углерода 1 и 2 находится между типичными длинами одинарных и двойных связей углерод-углерод, что согласуется с неклассическими предсказаниями о порядке связи немного выше 1. Исследователи, кристаллизовавшие 2-норборнильный катион, отметили, что катион оказался невозможным. кристаллизоваться, если не обеспечить химическую среду, которая зафиксирует его в одной определенной ориентации. [2]
См. также [ править ]
Ссылки [ править ]
- ^ Jump up to: Перейти обратно: а б с д Уоллинг, К. (1983). «Невинный свидетель смотрит на катион 2-норборнила». Отчеты о химических исследованиях . 16 (12): 448–454. дои : 10.1021/ar00096a004 .
- ^ Jump up to: Перейти обратно: а б с Шольц, Ф.; Химмель, Д.; Хайнеманн, ФРВ; Шлейер, PVR; Мейер, К.; Кроссинг, И. (2013). «Определение кристаллической структуры неклассического 2-норборнильного катиона». Наука . 341 (6141): 62–64. Бибкод : 2013Sci...341...62S . дои : 10.1126/science.1238849 . ПМИД 23828938 . S2CID 206549219 .
- ^ Jump up to: Перейти обратно: а б с д Браун, ХК (1983). «Энергия переходных состояний и промежуточного катиона при ионизации 2-норборнильных производных. Где находится энергия неклассической стабилизации?». Отчеты о химических исследованиях . 16 (12): 432–440. дои : 10.1021/ar00096a002 .
- ^ Jump up to: Перейти обратно: а б с Браун, ХК (1973). «Вопрос о мостиковом соединении при сольволизе 2-норборнильных производных». Отчеты о химических исследованиях . 6 (11): 377–386. дои : 10.1021/ar50071a003 .
- ^ Jump up to: Перейти обратно: а б Стрейтвизер, Эндрю (1961). «Глава 12: Ионы карбония». Теория молекулярных орбиталей для химиков-органиков . Нью-Йорк: John Wiley and Sons Inc., стр. 357–391 .
- ^ Jump up to: Перейти обратно: а б с д Сарджент, Джордж Данн (1971). «Глава 24: 2-норборнил-катион». В Оле, Джордж; фон Шлейер, Пол (ред.). Ионы карбония . Том III: Основные типы (продолжение). Нью-Йорк: Wiley-Interscience. стр. 1099–1200.
- ^ Jump up to: Перейти обратно: а б Ола, Джорджия; Лян, Г.; Матееску, Грузия; Рименшнейдер, Дж. Л. (1973). «Стабильные карбокатионы. Кл. Фурье-преобразование углерода-13, ядерный магнитный резонанс и рентгеновская фотоэлектронная спектроскопия, исследование 2-норборнильного катиона». Журнал Американского химического общества . 95 (26): 8698. doi : 10.1021/ja00807a032 .
- ^ Jump up to: Перейти обратно: а б Лоутон, Р.Г. (1961). «1,5-Участие в сольволизе β-(Δ 3 -циклопентенил)этил п- нитробензолсульфонат». Журнал Американского химического общества . 83 (10): 2399. doi : 10.1021/ja01471a047 .
- ^ Jump up to: Перейти обратно: а б Сарджент, Джорджия (1966). «Мостиковые неклассические ионы карбония». Ежеквартальные обзоры, Химическое общество . 20 (2): 301–1073. дои : 10.1039/QR9662000301 .
- ^ Да, ЛИ; Прайс, Дж. М.; Ли, Ю.Т. (1989). «Инфракрасная спектроскопия пентакоординированного иона карбония C.
22Ч +
7 ". Журнал Американского химического общества . 111 (15): 5597. doi : 10.1021/ja00197a015 . - ^ Ола, Джорджия; Матееску, Грузия; Рименшнайдер, Дж. Л. (1972). «Электронная спектроскопия органических ионов. II. Энергии связи электронов углерода 1s норборнила, 2-метилнорборнила и родственных катионов. Дифференциация между неклассическими ионами карбония и классическими ионами карбения». Журнал Американского химического общества . 94 (7): 2529. doi : 10.1021/ja00762a066 .
- ^ Jump up to: Перейти обратно: а б Трахановский, WS (1965). «Молекулярно-орбитальные расчеты норборнильного катиона с использованием расширенной теории Хюккеля». Журнал органической химии . 30 (5): 1666–1668. дои : 10.1021/jo01016a517 .
- ^ Jump up to: Перейти обратно: а б с Дж. Д. Робертс и Си Си Ли (1951). «Природа промежуточного продукта сольволиза норборнильных производных». Дж. Ам. хим. Соц. 73 (10): 5009–5010. дои : 10.1021/ja01154a555 .
- ^ Jump up to: Перейти обратно: а б с Робертс, доктор медицинских наук; Ли, CC; Сондерс, WH (1954). «Перегруппировки в реакциях карбониевого ионного типа C 14 -Меченые производные норборнила». Журнал Американского химического общества . 76 (18): 4501. doi : 10.1021/ja01647a001 .
- ^ Невелл, ТП; Де Салас, Э.; Уилсон, CL (1939). «259. Использование изотопов в химических реакциях. Часть I. Механизм перегруппировки Вагнера – Меервейна. Обмен радиоактивного хлора и дейтерия между гидрохлоридом камфена и хлористым водородом». Журнал Химического общества (возобновленный) : 1188–1199. дои : 10.1039/JR9390001188 .
- ^ Браун, ХК; Лю, КТ (1975). «Дополнения к бициклическим олефинам. VII. Электрофильные присоединения хлористого водорода и хлорида дейтерия к норборнену, 2-метиленнорборнану и родственным бициклическим олефинам. Доказательства процесса иона карбония и захвата несимметричных (классических) 2-норборнильных катионов». Журнал Американского химического общества . 97 (3): 600. doi : 10.1021/ja00836a022 .
- ^ Робертс, доктор медицинских наук; Мазур, Р.Х. (1951). «Природа промежуточного продукта в реакциях взаимопревращения карбониевого ионного типа производных циклобутил-, циклопропилкарбинила и аллилкарбинила». Журнал Американского химического общества . 73 (7): 3542. doi : 10.1021/ja01151a550 .
- ^ Браун, Ф.; Хьюз, Эд; Ингольд, СК; Смит, Дж. Ф. (1951). «Изменения Вагнера, синартетическое ускорение и синартетические ионы». Природа . 168 (4263): 65. Бибкод : 1951Natur.168...65B . дои : 10.1038/168065a0 . S2CID 4283069 .
- ^ Jump up to: Перейти обратно: а б с д и ж Уинштейн, С.; Трифан, Д.С. (1949). «Структура иона бицикло[2,2,1]2-гептил (норборнила) карбония». Журнал Американского химического общества . 71 (8): 2953. doi : 10.1021/ja01176a536 .
- ^ Jump up to: Перейти обратно: а б Уинштейн, С.; Клиппингер, Э.; Хау, Р.; Фогельфангер, Э. (1965). «Неклассический норборнил-катион». Журнал Американского химического общества . 87 (2): 376. doi : 10.1021/ja01080a040 .
- ^ Браун, Герберт (1962). «Напряженные переходные состояния». Специальная публикация . № 16: Переходное государство. Лондон: Химическое общество. стр. 140–178.
- ^ Браун, ХК; Хлупек, Ф.Дж.; Рей, Миннесота (1964). «Синтез и скорости этанолиза 2-фенил-экзо-норборнилхлорида. Вопрос о неклассическом 1- и 2-фенилнорборнильном катионе». Журнал Американского химического общества . 86 (6): 1246. doi : 10.1021/ja01060a058 .
- ^ Браун, ХК; Морган, Кей Джей; Хлупек, Ф.Дж. (1965). «Структурные эффекты в сольволитических реакциях. I. Роль уравновешивающих катионов в химии ионов карбония. Природа промежуточных продуктов, участвующих в сольволизе симметрично замещенных производных β-фенилэтила». Журнал Американского химического общества . 87 (10): 2137. doi : 10.1021/ja01088a011 .
- ^ Браун, ХК (1986). «Переписка - новый взгляд на 2-норборнильный катион». Отчеты о химических исследованиях . 19 (2): 34. дои : 10.1021/ar00122a001 .
- ^ Ола, Джорджия (1976). «Стабильные карбокатионы, 189. σ-мостиковый 2-норборнильный катион и его значение для химии». Отчеты о химических исследованиях . 9 (2): 41–52. дои : 10.1021/ar50098a001 .
- ^ Ола, Джорджия; Пракаш, ГКС; Сондерс, М. (1983). «Заключение классического и неклассического ионного спора на основе структурного исследования 2-норборнильного катиона». Отчеты о химических исследованиях . 16 (12): 440. doi : 10.1021/ar00096a003 .
- ^ Jump up to: Перейти обратно: а б Ола, Джорджия (1995). «Мой поиск карбокатионов и их роль в химии (Нобелевская лекция)». Angewandte Chemie International Edition на английском языке . 34 (1314): 1393–1405. дои : 10.1002/anie.199513931 .
- ^ Jump up to: Перейти обратно: а б Уинштейн, С.; Картер, П. (1961). «П-путь к бициклооктильному неклассическому катиону». Журнал Американского химического общества . 83 (21): 4485. doi : 10.1021/ja01482a057 .
- ^ Jump up to: Перейти обратно: а б Неницеску, Костин (1968). «Глава 1: Исторический обзор». В Оле, Джордж; фон Шлейер, Пол (ред.). Ионы карбония . Том I: Общие аспекты и методы исследования. Нью-Йорк: Wiley-Interscience. стр. 55–59.
- ^ Бартлетт, PD; Сарджент, Джорджия (1965). «Нуклеофильная реакционная способность двойной связи углерод-углерод. II. Сольволитическое замыкание кольца 2-(3-метил- и 3,4-диметил-Δ). 3 -циклопентенил)этил п- нитробензолсульфонаты». Журнал Американского химического общества . 87 (6): 1297. doi : 10.1021/ja01084a026 .
- ^ Jump up to: Перейти обратно: а б Шлейер, PVR; Уоттс, МЫ; Форт, Колорадо; Комисаров, МБ; Ола, Джорджия (1964). «Стабильные ионы карбония. X. Наблюдение 2-норборнильного катиона методом прямого ядерного магнитного резонанса». Журнал Американского химического общества . 86 (24): 5679. doi : 10.1021/ja01078a056 .
- ^ Ола, Джорджия; Пракаш, ГКС; Арванаги, М.; Анет, ФАЛ (1982). "Высокое поле 1 Рука 13 C-ЯМР-спектроскопическое исследование 2-норборнильного катиона». Журнал Американского химического общества . 104 (25): 7105. doi : 10.1021/ja00389a037 .
- ^ Леоне, Рональд; Барборак, Дж. К.; фон Шлейер, Пол (1973). «Глава 33: Вырожденные ионы карбония». В Оле, Джордж; фон Шлейер, Пол (ред.). Ионы карбония . Том IV: Основные типы (продолжение). Нью-Йорк: Wiley-Interscience. стр. 1911–1915.
- ^ Фрай, Джеймс; Карабацос, Герасим (1970). «Глава 14: Внутримолекулярные гидридные сдвиги в ионах карбония». В Оле, Джордж; фон Шлейер, Пол (ред.). Ионы карбония . Том II: Методы формирования и основные типы. Нью-Йорк: Wiley-Interscience. стр. 535–553.
- ^ Яннони, CS; Мачо, В.; Мире, ПК (1982). «Решено 13 Спектры ЯМР 1С ионов карбония при криогенных температурах. Норборнильный катион при 5 К». Журнал Американского химического общества . 104 (25): 7380. doi : 10.1021/ja00389a108 .
- ^ Ола, Джорджия; Уайт, AM (1969). «Стабильные ионы карбония. LXXXVI. Спектр ядерного магнитного резонанса углерода-13 стабильного неклассического норборнильного катиона. Несовместимость с концепцией уравновешивания классических ионов и дальнейшее доказательство структуры протонированного нортрициклена». Журнал Американского химического общества . 91 (14): 3954. doi : 10.1021/ja01042a053 .
- ^ Ола, Джорджия; Коммейрас, А.; Луи, Калифорния (1968). «Стабильные ионы карбония. LXXII. Рамановская спектроскопия и ЯМР-спектроскопическое исследование иона нортрициклония [протонированного трицикло [2.2.1.0] 2,6 ]гептан] и его связь с 2-норборнильным [бицикло[2.2.1]гептил] катионом. Природа стабильного долгоживущего норборнильного катиона в растворах сильных кислот». Журнал Американского химического общества . 90 (14): 3882. doi : 10.1021/ja01016a062 .
- ^ Радом, Лео ; Поппингер, Дитер; Хэддон, Роберт (1976). «Глава 38: Молекулярно-орбитальная теория карбокатионов». В Оле, Джордж; фон Шлейер, Пол (ред.). Ионы карбония . Том V: Разные ионы, теория и структура. Нью-Йорк: Wiley-Interscience. стр. 2390–2391.
- ^ Хоффманн, Р. (1964). «Расширенная теория Хюккеля. IV. Ионы карбония». Журнал химической физики . 40 (9): 2480–2488. Бибкод : 1964JChPh..40.2480H . дои : 10.1063/1.1725551 .
- ^ Шлейер, PVR; Чандрасекхар, Дж. (1981). «Оценка дополнительной стабильности мостикового 2-норборнильного катиона». Журнал органической химии . 46 : 225–227. дои : 10.1021/jo00314a065 .
- ^ Браун, ХК; Рей, Миннесота (1964). «Сравнение действия заместителей в положении 2 норборнильной системы с их действием в типичных вторичных алифатических и алициклических производных. Доказательства отсутствия неклассической стабилизации норборнильного катиона». Журнал Американского химического общества . 86 (22): 5008. doi : 10.1021/ja01076a058 .
- ^ Бантон, Калифорния (1963). «Глава 2. Структурное влияние на скорость замещения; Раздел 11. Неклассические ионы карбония». В Хьюзе, ЭД (ред.). Механизмы реакций в органической химии . Том I: Нуклеофильное замещение у насыщенного атома углерода. Амстердам: Издательство Elsevier. стр. 59–67.
- ^ Шлейер, ПВР (1964). «Неклассическая проблема ионов карбония: скорости реакций». Журнал Американского химического общества . 86 (9): 1856–1857. дои : 10.1021/ja01063a044 .
- ^ Браун, ХК; Хлупек, Ф.Дж.; Рей, Миннесота (1964). «Сравнение скоростей сольволиза типичных производных норборнила и циклопентила. Критическое исследование скоростей как основы постулируемой неклассической структуры норборнильных катионов». Журнал Американского химического общества . 86 (6): 1247. doi : 10.1021/ja01060a059 .
- ^ Браун, ХК; Хлупек, Ф.Дж.; Рей, Миннесота (1964). «Скорости сольволиза п -нитробензоатов экзо - эндо' третичных норборнеолов. Критическое исследование соотношения скоростей экзо - эндо как основы постулируемой неклассической структуры норборнильного катиона». Журнал Американского химического общества . 86 (6): 1248. doi : 10.1021/ja01060a060 .
- ^ Сондерс, М.; Тельковски, Л.; Кейтс, MR (1977). «Изотопическое возмущение вырождения. Спектры ядерного магнитного резонанса углерода-13 диметилциклопентильных и диметилнорборнильных катионов». Журнал Американского химического общества . 99 (24): 8070. doi : 10.1021/ja00466a060 .
- ^ Сондерс, М.; Кейтс, MR (1977). «Изотопическое возмущение резонанса. Спектры ядерного магнитного резонанса углерода-13 дейтерированных циклогексенильных и циклопентенильных катионов». Журнал Американского химического общества . 99 (24): 8071. doi : 10.1021/ja00466a061 .
- ^ Сондерс, М.; Кейтс, MR (1980). «Влияние изотопа дейтерия на спектр ЯМР углерода-13 бицикло[2.2.1]гептильного катиона. Неклассический норборнильный катион». Журнал Американского химического общества . 102 (22): 6867. doi : 10.1021/ja00542a044 .