Нильский красный
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК 9-(Диэтиламино)-5H - бензо[ а ]феноксазин-5-он | |
| Другие имена Нильский красный, нильский синий оксазон. | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.028.151 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 20 Н 18 Н 2 О 2 | |
| Молярная масса | 318.376 g/mol |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Нильский красный (также известный как нильский синий оксазон ) представляет собой липофильное пятно. Нильский красный окрашивает внутриклеточные липидные капли в желтый цвет. В большинстве полярных растворителей нильский красный не флуоресцирует; однако в среде, богатой липидами, он может интенсивно флуоресцировать с различными цветами от темно-красного (для полярных мембранных липидов) до сильного желто-золотого свечения (для нейтральных липидов во внутриклеточных хранилищах). Краситель обладает высокой сольватохромностью , и длина волны его излучения и возбуждения смещается в зависимости от полярности растворителя. [1] а в полярных средах вообще почти не флуоресцирует. [2]
Нильский красный находит применение в клеточной биологии, где его можно использовать в качестве мембранного красителя, который можно легко визуализировать с помощью эпифлуоресцентного микроскопа с длинами волн возбуждения и излучения, которые обычно совпадают с красным флуоресцентным белком . Нильский красный также использовался в рамках чувствительного процесса обнаружения микропластика в бутилированной воде . [3] [4] Кроме того, нильский красный является замечательным кандидатом при изготовлении мембран для различных датчиков для обнаружения изменений окружающей среды, таких как вкус, газ, pH и т. д. [5]
В триглицеридах (нейтральный липид) нильский красный имеет максимум возбуждения около 515 нм (зеленый) и максимум эмиссии около 585 нм (желто-оранжевый). [6] Напротив, в фосфолипидах (полярных липидах) нильский красный имеет максимум возбуждения около 554 нм (зеленый) и максимум эмиссии около 638 нм (красный). [7]
Сообщается, что коэффициент диффузии нильского красного в этаноле составляет 470 мкм. 2 /с. [8]
Синтез
[ редактировать ]Нильский красный можно получить кислотным гидролизом путем кипячения раствора нильского синего с серной кислотой . [9] В этом процессе иминиевая группа заменяется карбонильной группой. Альтернативно, нильский красный и его аналоги (нафтооксазиновые красители) могут быть получены кислотно-катализируемой конденсацией соответствующих 5-(диалкиламино)-2-нитрозофенолов с 2-нафтолом . Выходы обычно умеренные, поскольку в этой процедуре не используется соокислитель. [10] Поскольку реакция образования нильского красного обычно не полностью исчерпывает запасы нильского синего, требуются дополнительные этапы разделения, если требуется чистый нильский красный.

- Нильский красный в видимом и ультрафиолетовом (366 нм) свете в различных растворителях. Слева направо: 1. вода , 2. метанол , 3. этанол , 4. ацетонитрил , 5. диметилформамид , 6. ацетон , 7. этилацетат , 8. дихлорметан , 9. н- гексан , 10. метил трет- - бутиловый эфир , 11. циклогексан , 12. толуол .
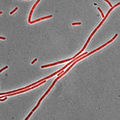
- Bacillus subtilis , окрашенная нильским красным в качестве мембранного красителя (показана красным). Этот штамм растет частично в виде клеточных цепей, поэтому мембранный краситель может быть полезен для различения внутренних границ клеток.
Ссылки
[ редактировать ]- ^ Плендерлейт, Ричард; Свифт, Томас; Риммер, Стивен (2014). «Сильноразветвленные поли(N-изопропилакриламиды) с морфологией ядро-оболочка ниже нижней критической температуры растворения». РСК Прогресс . 4 (92): 50932–50937. дои : 10.1039/C4RA10076J . hdl : 10454/11180 .
- ^ Гринспен, П; Майер, ЕП; Фаулер, SD (1 марта 1985 г.). «Нильский красный: селективное флуоресцентное окрашивание внутриклеточных липидных капель» . Журнал клеточной биологии . 100 (3): 965–973. дои : 10.1083/jcb.100.3.965 . ПМК 2113505 . ПМИД 3972906 .
- ^ Давид Шукман (15 марта 2018 г.). «Пластик: ВОЗ запускает обзор здравоохранения» . Новости BBC онлайн .
- ^ Мейсон, Шерри А.; Уэлч, Виктория Г.; Нератко, Джозеф (11 сентября 2018 г.). «Загрязнение синтетическими полимерами бутилированной воды» . Границы в химии . 6 : 407. Бибкод : 2018FrCh....6..407M . дои : 10.3389/fchem.2018.00407 . ПМК 6141690 . ПМИД 30255015 .
- ^ Халилиан, Алиреза; Хан, доктор Раджибур Рахаман; Кан, Шин Вон (1 октября 2017 г.). «Высокочувствительный волоконно-оптический датчик вкуса с широким динамическим диапазоном и боковой полировкой». Датчики и исполнительные механизмы B: Химические вещества . 249 : 700–707. дои : 10.1016/j.snb.2017.04.088 .
- ^ «Fluorescent SpectraViewer — триглицериды нильского красного» . Термо Фишер Сайентифик . 17 мая 2017 года . Проверено 6 марта 2020 г.
- ^ «Fluorescent SpectraViewer – фосфолипиды нильского красного» . Термо Фишер Сайентифик . 17 мая 2017 года . Проверено 6 марта 2020 г.
- ^ Шафии, Омид; Дженкинс, Саманта Г.; Ито, Такаши; Хиггинс, Дэниел А. (27 января 2023 г.). «Диффузия гидрофильных в гидрофобные формы нильского красного в водных гелях C12EO10 методом корреляционной флуоресцентной спектроскопии с переменной площадью» . Физическая химия Химическая физика . 25 (4): 2853–2861. дои : 10.1039/D2CP05578C . ISSN 1463-9084 .
- ^ Фаулер, SD; Гринспен, П. (5 января 2017 г.). «Применение нильского красного, флуоресцентного гидрофобного зонда, для обнаружения отложений нейтральных липидов в срезах тканей: сравнение с масляным красным О» . Журнал гистохимии и цитохимии . 33 (8): 833–836. дои : 10.1177/33.8.4020099 . ПМИД 4020099 . S2CID 10496865 .
- ^ Пак, Со Ён; Кубота, Ясухиро; Фунабики, Казумаса; Широ, Мотоо; Мацуи, Масаки (11 марта 2009 г.). «Твердотельные флуоресцентные нафтооксазиновые красители ближнего инфракрасного диапазона, присоединенные к объемным дибутиламино- и перфторалкенилокси-группам в 6- и 9-положениях». Буквы тетраэдра . 50 (10): 1131–1135. дои : 10.1016/j.tetlet.2008.12.081 .