Колонка хроматография

Колоночная хроматография в химии - это метод хроматографии, используемый для выделения одного химического соединения из смеси. Хроматография способна разделять вещества на основе дифференциальной адсорбции соединений адсорбенту; Соединения перемещаются через колонку с разными скоростями, позволяя их разделить на фракции. Техника широко применима, так как может использоваться множество различных адсорбентов (нормальная фаза, обратная фаза или иное)) с широким диапазоном растворителей. Техника может использоваться в масштабах от микрограммов до килограммов. Основным преимуществом колоночной хроматографии является относительно низкая стоимость и распоряжение стационарной фазы, используемой в процессе. Последнее предотвращает перекрестное загрязнение и деградацию стационарной фазы из-за переработки. Колоночная хроматография может быть выполнена с использованием гравитации для перемещения растворителя или с использованием сжатого газа для проталкивания растворителя через колонку.
Тонкослойный хроматограф может показать, как будет вести себя смесь соединений при очистке колоночной хроматографией. Разделение сначала оптимизируется с использованием тонкослойной хроматографии перед выполнением колоночной хроматографии.
Подготовка столбца
[ редактировать ]Колонна готовится путем упаковки сплошного адсорбента в цилиндрическое стекло или пластиковую трубку. Размер будет зависеть от количества изолированного соединения. Основание трубки содержит фильтр, хлопковую или стеклянную шерсть или стеклянную фритю, чтобы удерживать твердую фазу на месте. Резервуар растворителя может быть прикреплен в верхней части столбца.
Два метода обычно используются для приготовления колонки: сухой метод и мокрый метод. Для сухого метода колонна сначала заполняется сухим стационарным фазовым порошком, за которым следует добавление подвижной фазы, которая промывается через колонку до тех пор, пока она не станет полностью влажной, и с этой точки никогда не разрешается запускать сухой. [ 1 ] Для влажного метода со подготовлена элюента стационарной фазовой порошком, а затем тщательно выливается в колонну. Верхняя часть кремнезема должна быть плоской, а вершина кремнезема может быть защищена слоем песка. Элуент медленно проходит через колонку для продвижения органического материала.
Отдельные компоненты сохраняются стационарной фазой по -разному и отделены друг от друга, когда они работают на разных скоростях через колонку с элюентом. В конце колонны они элюируют по одному. В течение всего процесса хроматографии элюент собирается в серии фракций . Фракции могут быть собраны автоматически с помощью коллекционеров фракций. Производительность хроматографии может быть увеличена, запустив несколько колонн за раз. В этом случае используются мульти -потоки коллекционеров. Композиция потока элюента может контролироваться, и каждая фракция анализируется для растворенных соединений, например, аналитической хроматографией, спектрами поглощения ультрафиолета или флуоресценции . Цветные соединения (или флуоресцентные соединения с помощью ультрафиолетовой лампы) можно рассматривать через стеклянную стену как движущиеся полосы.
Стационарная фаза
[ редактировать ]
Стационарная фаза или адсорбент в колоночной хроматографии является твердым. Наиболее распространенной стационарной фазой для колоночной хроматографии является силикагель , следующим наиболее распространенным является глинозем . Порошок целлюлозы часто использовался в прошлом. Для выполнения ионной обменной хроматографии доступен широкий спектр стационарных фаз , хроматографии с обратной фазой (RP), аффинной хроматографии или расширенной адсорбции слоя (EBA). как Стационарные фазы, правило, являются тонко измельченными порошками или гелями и/или являются микропористыми для повышенной поверхности, хотя в EBA используется жидкое слой. Существует важное соотношение между весом стационарной фазы и сухой весом смеси аналита, которая может быть применена на колонку. Для хроматографии колонны кремнезема это соотношение лежит в пределах 20: 1 до 100: 1, в зависимости от того, насколько близко друг к другу компоненты аналита элюируются. [ 2 ]
Мобильная фаза (элюент)
[ редактировать ]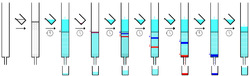
Мобильная фаза или элюент - это растворитель или смесь растворителей, используемых для перемещения соединений через колонку. Он выбран таким образом, чтобы значение коэффициента удержания представляющего собой соединения составляло примерно 0,2 - 0,3, чтобы минимизировать время и количество элюента для запуска хроматографии. Элуент также был выбран таким образом, чтобы различные соединения могли быть эффективно разделены. Элюент оптимизируется в небольших предварительных претензиях, часто используя тонкослойную хроматографию (TLC) с одной и той же стационарной фазой, используя растворители различной полярности, пока не будет обнаружена подходящая система растворителя. Общие растворители подвижной фазы, в порядке увеличения полярности, включают гексан , дихлорметан , этилацетат , ацетон и метанол . [ 3 ] Общая система растворителя представляет собой смесь гексана и этилацетата, с пропорциями, скорректированными до тех пор, пока целевое соединение не получит коэффициент удержания от 0,2 до 0,3. Вопреки общему заблуждению, только метанол может использоваться в качестве элюента для высокополярных соединений и не растворяет силикагель.
Существует оптимальная скорость потока для каждого конкретного разделения. Более быстрая скорость потока элюента минимизирует время, необходимое для запуска столбца, и, таким образом, минимизирует диффузию, что приводит к лучшему разделению. Тем не менее, максимальная скорость потока ограничена, потому что для аналита требуется конечное время, чтобы уравновешиваться между стационарной фазой и подвижной фазой, см. Уравнение Ван Демтера . Простая лабораторная колонка работает по гравитационному потоку. Скорость потока такого столбца может быть увеличена путем расширения свежей заполненной элюента столбца над верхней частью стационарной фазы или уменьшена с помощью контроля TAP. Более быстрые скорости потока могут быть достигнуты с помощью насоса или с использованием сжатого газа (например, воздуха, азота или аргона ), чтобы протолкнуть растворитель через колонку (хроматография Flash). [ 4 ] [ 5 ]

Размер частиц стационарной фазы, как правило, более тонкий в хроматографии флэш -колонны, чем в гравитационной колонне хроматографии. Например, одним из наиболее широко используемых сортов силикагеля в первой технике является сетка 230 - 400 (40 - 63 мкм), в то время как для последней техники обычно требуется сетка 70 - 230 (63 - 200 мкм) кремнезема. [ 6 ]
Была разработана электронная таблица, которая помогает успешной разработке колонн флеш. Электронная таблица оценивает объем удержания и объем полос аналитов, числа фракций, как ожидается, будут содержать каждый аналит, и разрешение между соседними пиками. Эта информация позволяет пользователям выбирать оптимальные параметры для разделения подготовительной шкалы до того, как будет предпринята попытка самого столбца. [ 7 ]
Автоматизированные системы
[ редактировать ]
Колоночная хроматография является чрезвычайно трудоемкой стадией в любой лаборатории и может быстро стать узким местом для любой лаборатории процесса. Многие производители, такие как Biotage, Buchi, Interchim и Teledy ISCO, разработали автоматизированные флэш -хроматографические системы (обычно называемые LPLC, жидкая хроматография с низким давлением, около 350–525 кПа или 50,8–76,1 фунтов на квадратный дюйм), что минимизирует вовлечение человека в процесс очистки. Автоматизированные системы будут включать компоненты, обычно обнаруживаемые в более дорогих высокопроизводительных системах жидкой хроматографии (ВЭЖХ), таких как насос градиента, порты впрыска образца, ультрафиолетовый детектор и коллектор фракции для сбора элюента. Как правило, эти автоматизированные системы могут отделять образцы от нескольких миллиграммов до промышленного масштаба килограмма и предлагают гораздо более дешевое и более быстрое решение для выполнения нескольких инъекций в системах PREP-HPLC.
Разрешение (или способность отделять смесь) на системе LPLC всегда будет ниже по сравнению с ВЭЖХ, поскольку упаковочный материал в колонке ВЭЖХ может быть намного меньше, как правило, только 5 микрометра, таким образом, увеличивая площадь стационарной фазы, увеличивая поверхностные взаимодействия и давая лучшее разделение. Тем не менее, использование этой небольшой упаковочной среды вызывает высокое обратное давление, и поэтому его называют жидкой хроматографией высокого давления. Колонны LPLC, как правило, упаковывают кремнеземами около 50 микрометров, тем самым снижая обратное давление и разрешение, но также устраняет необходимость в дорогих насосах высокого давления. Производители теперь начинают перемещаться в системы хроматографии с более высоким давлением и называют их системами жидкой хроматографии среднего давления (MPLC), которые работают выше 1 МПа (150 фунтов на квадратный дюйм).
Расчет разрешения хроматограммы колонки
[ редактировать ]
Как правило, колонна -хроматография настроена на перистальтические насосы, проточные буферы и образец раствора через верхнюю часть колонны. Решения и буферы проходят через колонку, где коллектор фракции в конце установки столбца собирает элюированные образцы. Перед сбором фракций образцы, которые элюируются из столбца, проходят через детектор, такой как спектрофотометр или масс -спектрометр, чтобы можно было определить концентрацию разделенных образцов в смеси раствора образца.
Например, если бы вы были разделять два разных белка с различными способностями связывания в колонке от образца раствора, хорошим типом детектора будет спектрофотометр с использованием длины волны 280 нм. Чем выше концентрация белка, который проходит через элюированный раствор через колонку, тем выше поглощение этой длины волны.
Поскольку колоночная хроматография имеет постоянный поток элюированного раствора, проходящего через детектор в различных концентрациях, детектор должен построить концентрацию элюированного образца в течение всего времени. Этот график концентрации образца в зависимости от времени называется хроматограммой.
Конечной целью хроматографии является отделение различных компонентов от смеси растворов. Резолюция выражает степень разделения между компонентами от смеси. Чем выше разрешение хроматограммы, тем лучше степень разделения образцов, которые дает колонка. Эти данные являются хорошим способом определения свойств разделения колонны этой конкретной выборки. Резолюция может быть рассчитана по хроматограмме.
Отдельные кривые на диаграмме представляют собой различные профили концентрации элюирования образца с течением времени, основываясь на их сродстве к смоле колонки. Для расчета разрешения требуются время удержания и ширина кривой.
Время удержания - это время от начала обнаружения сигнала детектором до пиковой высоты профиля концентрации элюирования каждого разных образцов.
Ширина кривой является шириной кривой профиля концентрации различных образцов в хроматограмме в единицах времени.
Упрощенным методом расчета разрешения хроматограммы является использование модели пластины. [ 8 ] Модель пластины предполагает, что столбец может быть разделен на определенное количество секций, или пластины, и баланс массы может быть рассчитан для каждой отдельной пластины. Этот подход приближается к типичной кривой хроматограммы в виде гауссовой кривой распределения . При этом ширина кривой оценивается в 4 раза выше стандартного отклонения кривой, 4σ. Время хранения - это время от начала обнаружения сигнала до времени пиковой высоты гауссовой кривой.
Из переменных на рисунке выше, разрешения, номера пластины и высоты пластины модели столбца могут быть рассчитаны с использованием уравнений:
Резолюция (R S ):
- R s = 2 (t rb - t ra )/(w b + w a ),
где:
- t rb = время удержания растворенного вещества B
- t ra = время удержания растворенного
- W B = Гауссовая кривая ширина растворенного вещества B
- w a = Гауссовая ширина растворенного
Номер пластины (n):
- N = (t r ) 2 /(W/4) 2
Высота тарелки (H):
- H = l/n
где L - длина колонны. [ 8 ]
Адсорбционное равновесие столбца
[ редактировать ]Для адсорбционной колонны колонна смола (стационарная фаза) состоит из микробур. Еще более мелкие частицы, такие как белки, углеводы, ионы металлов или другие химические соединения, конъюгированы на микробурках. Каждая частица связывания, которая прикреплена к Microbead, может быть связывается в соотношении 1: 1 с образцом растворенного вещества, отправленным через колонку, который необходимо очистить или разделить.
Связывание между целевой молекулой, которая должна быть разделена, и молекулой связывания на бусинках колонны можно моделировать с использованием простой равновесной реакции k eq = [cs]/([c] [s], где k eq - равновесная постоянная , [c] и [s] являются концентрациями молекулы -мишени и молекулы связывания на смоле колонны соответственно. [CS] является концентрацией комплекса молекулы -мишени, связанной с смолой столбца. [ 8 ]
Используя это в качестве основы, можно использовать три разные изотермы для описания динамики связывания хроматографии столбца: линейный, лангмюр и Фрейндлих.
Линейная изотерма возникает, когда необходимо очистить концентрацию растворенного вещества, очень мала по сравнению с молекулой связывания. Таким образом, равновесие можно определить как:
- [Cs] = k eq [c].
Для промышленного использования используются общие молекулы связывания на бусинках из колонны смолы должны учитываться, поскольку необходимо учитывать незанятые участки. Изотерма Langmuir и изотерма Freundlich полезны для описания этого равновесия. Изотерма Langmuir определяется:
- [Cs] = (k eq s tot [c])/(1 + k eq [c]), где s tot - это молекулы общего связывания на шариках.
Изотерма Фрейндлиха определяется:
- [Cs] = k eq [c] 1/n
Изотерма Freundlich используется, когда колонка может связываться со многими различными образцами в растворе, которые необходимо очистить. Поскольку множество разных образцов имеют разные константы связывания с шариками, существует много разных k уравнений . Следовательно, изотерма Langmuir не является хорошей моделью для связывания в этом случае. [ 8 ]
Смотрите также
[ редактировать ]- Быстрая белковая жидкая хроматография (FPLC) - разделение белков с использованием колоночной хроматографии
- Высокопроизводительная жидкая хроматография (ВЭЖХ)-колоночная хроматография с использованием высокого давления
Ссылки
[ редактировать ]- ^ Шустерман, AJ; McDougal, PG; Glasfeld, A (1997). «Хроматография флэш-колона». J Chem Educ . 74 (10): 1222. Bibcode : 1997jched..74.1222S . doi : 10.1021/ed074p1222 . ISSN 0021-9584 .
- ^ «Как установить флэш-хроматографию из диоксида кремнезема и на самом деле добиться успеха при разделении» . ReachDevices.com . Достигнуть Defices, LLC . Получено 3 января 2019 года .
- ^ Furniss, Brian S.; Hannaford, Antony, J.; Смит, Питер В.Г.; Tatchell, Austin S. (1989). Учебник Фогеля практической органической химии . Longman Scientific & Technical. п. 203. ISBN 978-0582462366 .
{{cite book}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Тем не менее, WC; Кан, м; Митра, А (1978). «Быстрая хроматографическая техника для препаративного разделения с умеренным разрешением». J Org Chem . 43 (14). ACS : 2923–2925. doi : 10.1021/jo00408a041 .
- ^ Harwood LM, Moody CJ (13 июня 1989 г.). Экспериментальная органическая химия: принципы и практика (иллюстрировано изд.). Лондон: Блэквелл. С. 180–185 . ISBN 978-0-632-02017-1 Полем OCLC 1079261960 .
- ^ «Материал сбора силикагеля для нормальной фазовой колоночной хроматографии» . Материал Уборка. 2008 Получено 3 января 2019 года .
- ^ Ярмарка, JD; Kormos, CM (2008). «Флэш-колонна хроматограммы, оцененные по данным тонкослойной хроматографии». J Chromatogra a . 1211 (1–2): 49–54. doi : 10.1016/j.chroma.2008.09.085 . ISSN 0021-9673 . PMID 18849041 .
- ^ Jump up to: а беременный в дюймовый Харрисон Р.Г., Тодд П.В., Рудж С.Р., Петридес Д.П. (2003). Биозепации Наука и инженерия (2 -е изд.). Нью -Йорк, Нью -Йорк: издательство Оксфордского университета . ISBN 9780190213732 Полем OCLC 899240244 .