Люминол
| |
| |
| Имена | |
|---|---|
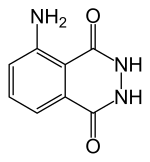
| Предпочтительное название ИЮПАК
5-Амино-2,3-дигидрофталазин-1,4-дион | |
| Другие имена
5-амино-2,3-дигидро-1,4-фталазиндион
о- Аминофталоилгидразид о- Аминофталилгидразид 3-аминофталгидразид 3-аминофталевой гидразид | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.007.556 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| C8H7N3OC8H7N3O2 | |
| Молярная масса | 177.16 g/mol |
| Температура плавления | 319 ° С (606 ° F; 592 К) |
| Опасности | |
| NFPA 704 (огненный алмаз) | |
| Паспорт безопасности (SDS) | Паспорт безопасности люминола |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Люминол (C 8 H 7 N 3 O 2 ) представляет собой химическое вещество , проявляющее хемилюминесценцию с синим свечением при смешивании с соответствующим окислителем . Люминол представляет собой кристаллическое твердое вещество от белого до бледно-желтого цвета, растворимое в большинстве полярных органических растворителей, но нерастворимое в воде.
Судебно- медицинские эксперты используют люминол для обнаружения следов крови на месте преступления , поскольку он вступает в реакцию с железом в гемоглобине . Биологи используют его в клеточных анализах для обнаружения меди , железа , цианидов , а также специфических белков посредством вестерн-блоттинга . [ 2 ]
Когда люминол равномерно распыляется по площади, следы активирующего окислителя заставляют люминол излучать синее свечение, которое можно увидеть в затемненной комнате. Свечение длится всего около 30 секунд, но его можно задокументировать фотографически. Свечение сильнее в областях, на которые попадает больше брызг; интенсивность свечения не указывает на количество присутствующей крови или другого активатора.
Синтез
[ редактировать ]Люминол синтезируется в два этапа, начиная с 3-нитрофталевой кислоты . [ 3 ] [ 4 ] Сначала гидразин (N 2 H 4 ) нагревают с 3-нитрофталевой кислотой в высококипящем растворителе, таком как триэтиленгликоль и глицерин . Происходит реакция ацилзамещения конденсации с потерей воды с образованием 3-нитрофтальгидразида. Восстановление нитрогруппы до аминогруппы дитионитом натрия ( Na 2 S 2 O 4 ) через временный промежуточный гидроксиламин приводит к образованию люминола.
Соединение было впервые синтезировано в Германии в 1902 году. [ 5 ] но не назывался «люминол» до 1934 года. [ 3 ] [ 6 ]
Хемилюминесценция
[ редактировать ]
Чтобы проявить люминесценцию, люминол необходимо активировать окислителем. раствор, содержащий перекись водорода (H 2 O 2 ) и гидроксид- Обычно активатором является ионы в воде. В присутствии катализатора , такого как железо или периодат , перекись водорода разлагается с образованием кислорода и воды:
- 2 Ч 2 О 2 → О 2 + 2 Ч 2 О
- Н 2 О 2 + КИО 4 → КИО 3 + О 2 + Н 2 О
часто используют феррицианид калия или периодат калия В лабораторных условиях в качестве катализатора . При судебно-медицинском обнаружении крови катализатором является железо, присутствующее в гемоглобине . [ 7 ] Ферменты в различных биологических системах также могут катализировать разложение перекиси водорода.
Точный механизм хемилюминесценции люминола представляет собой сложную многостадийную реакцию, особенно в водных условиях. Недавнее теоретическое исследование позволило объяснить каскад реакций, как показано ниже. [ 8 ] Люминол сначала депротонируется в основных условиях, затем окисляется до анионного радикала. Что, в свою очередь, имеет два пути получения ключевого промежуточного соединения α-гидроксипероксида. После циклизации до эндопероксида моноанион будет подвергаться разложению без люминесценции, если pH слишком низкий (< 8,2) для второго депротонирования. Однако эндопероксид-дианион может давать ретро-продукт Дильса-Альдера: 1,2-диоксан-3,6-дион-дианион. А после хемивозбуждения посредством двух одноэлектронных переносов (SET) дает 3-аминофталат-дианион в своем первом синглетном возбужденном состоянии (S1). Эта крайне нестабильная молекула релаксирует в основное состояние, тем самым излучая свет с длиной волны около 425 нм (фиолетово-синий), так называемую хемилюминесценцию .
Использование в уголовном расследовании
[ редактировать ]История
[ редактировать ]В 1928 году немецкий химик Х. О. Альбрехт обнаружил, что кровь , среди других веществ, усиливает свечение люминола в щелочном растворе перекиси водорода. [ 9 ] [ 10 ] В 1936 году Карл Глей и Карл Пфаннштиль подтвердили это усиление в присутствии гематина , компонента крови. [ 11 ] В 1937 году немецкий судмедэксперт Вальтер Шпехт провел обширные исследования применения люминола для обнаружения крови на местах преступлений. [ 12 ] В 1939 году патологоанатомы из Сан-Франциско Фредерик Прошер и А.М. Муди сделали три важных наблюдения о люминоле: [ 13 ] [ 14 ]
- хотя тест является предположительным, можно быстро исследовать большие площади подозрительного материала;
- засохшая и разложившаяся кровь давала более сильную и продолжительную реакцию, чем свежая кровь; и
- если свечение исчезает, его можно воспроизвести применением свежего раствора люминола с перекисью водорода; Таким образом, засохшие пятна крови можно многократно люминесцировать.
Теория
[ редактировать ]Следователи на месте преступления используют люминол, чтобы найти следы крови, даже если кто-то их очистил или удалил. Исследователь распыляет раствор люминола и окислителя. Железо в крови катализирует свечение. Количество катализатора, необходимое для того, чтобы вызвать реакцию, очень мало по сравнению с количеством люминола, что позволяет обнаруживать даже следовые количества крови. Голубое свечение длится около 30 секунд на одно применение. Для обнаружения свечения требуется достаточно темная комната. Любое обнаруженное свечение можно задокументировать с помощью фотографии с длинной выдержкой .
Недостатки
[ редактировать ]Использование Люминола при осмотре места преступления несколько затруднено тем, что он реагирует на железо- и медьсодержащие соединения, [ 15 ] отбеливатели , хрен , фекалии или остатки сигаретного дыма. [ 14 ] Нанесение люминола на улики может помешать проведению на них других тестов; однако ДНК была успешно извлечена из образцов, подвергшихся воздействию люминола. [ 16 ]
Родственные молекулы
[ редактировать ]- Люминол: 5-амино-2,3-дигидро-1,4; 3-аминофталгидразид; 1,4-фталазиндион, 5-амино-2,3-дигидро; КАС: [521-31-3]
C 8 H 7 N 3 O 2 – ММ: 177,16
λ абс (в 0,1 н. NaOH) λ макс 1: 347 нм и λ макс 2: 300 нм; ЕС (при λ макс. 1): 7650 л/моль × см
λ абс / λ em (MeOH): 355/413 нм - Люминол, натриевая соль: 3-аминофталгидразид натрия; КАС: [20666-12-0]
C 8 H 6 N 3 O 2 Na – MW: 199,12 - Люминола полугидрат: гидрат 3-аминофталгидразида натрия; КАС: [206658-90-4]
C 8 H 6 N 3 O 2 Na H 2 O 217,16 – MW: - Люминола гидрохлорид: гидрохлорид 3-аминофталгидразида; КАС: [74165-64-3]
C8H7N3O2 H7N : MМ HCl 213,62 - Изолюминол: 4-аминофталгидразид; КАС: [3682-14-1]
C 8 H 7 N 3 O 2 – ММ: 117,16 (Xi) - Моногидрат изолюминола: моногидрат 4-аминофталгидразида.
C 8 H 7 N 3 O 2 H 2 O 195,15 – ММ: - Изолюминол ABEI: моногидрат 4-аминофталгидразида; КАС: [66612-29-1]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Индекс Merck , 11-е издание, 5470 .
- ^ Хан, Парвез; Идрис, датский; МОксли, Майкл А.; и др. (май 2014 г.). «Хемилюминесцентные сигналы на основе люминола: клиническое и доклиническое применение и будущее использование» . Прикладная биохимическая биотехнология . 173 (2): 333–355. дои : 10.1007/s12010-014-0850-1 . ПМЦ 4426882 . ПМИД 24752935 .
- ^ Перейти обратно: а б Эрнест Хантресс; Лестер Стэнли; Алмон Паркер (1934). «Приготовление 3-аминофталгидразида для демонстрации хемилюминесценции». Журнал Американского химического общества . 56 (1): 241–242. дои : 10.1021/ja01316a077 .
- ^ Синтез люминола
- ^ См.:
- Алоис Йозеф Шмитц, «Ueber das Hydrazid der Trimesinsäure und der Hemimellithsäure». Архивировано 2 января 2015 г. в Wayback Machine (О гидразиде тримезиновой кислоты [1,3,5-бензолтрикарбоновой кислоты] и гемимеллитовой кислоты [1,2, 3-бензолтрикарбоновая кислота]), вступительная диссертация, Гейдельбергский университет, 1902 г.; стр. 17, 39–43. Шмитц называет люминол «1-амино-2,3-фталзаурегидразидом».
- Примечание: Гилл утверждает, что люминол был получен еще в 1853 году. См.: Стивен К. Гилл (1983) «Новые достижения в исследованиях хемилюминесценции», Aldrichimica Acta 16 (3): 59–61; есть сноска 2 на стр. 60. Доступно по адресу: Aldrichimica Acta. Архивировано 8 января 2015 г. в Wayback Machine . Однако в источниках, которые цитирует Гилл, не упоминается получение люминола до 1902 года. Гилл, вероятно, перепутал люминол с лофином (2,4,5-трифенил-1Н - имидазолом), о котором упоминаются в цитируемых им источниках. Лофин также является хемилюминесцентным веществом и впервые был получен в 1844 году Огюстом Лораном. (См.: Огюст Лоран (1844) «Sur un nouvel alcali Organique, la lophine» (О новой органической щелочи, лофине), Revue scientifique et industrielle , 18 : 272–278.) Хемилюминесценцию лофина впервые наблюдал: Радзишевский , Бронислав Л. (1877) «Untersuruchungen über HydroBenzamid, Amarin und Lophin». Архивировано 14 декабря 2015 г. в Wayback Machine (Исследования гидробензамида, амарина и лофина), Berichte der Deutschen chemischen Gesellschaft zu Berlin. , 10 :70–75. В 1853 году Людвиг Тейхман разработал тест крови, но он не основывался на хемилюминесценции. См.: Л. Тейхман (1853) «О кристаллизации органических компонентов крови» , Journal of Rational Medicine , новая серия, 3 : 375–388.
- ^ См. также: Эрнест Х. Хантресс, Лестер Н. Стэнли и Алмон С. Паркер (март 1934 г.) «Окисление 3-аминофталгидразида («люминола») как лекция, демонстрирующая хемилюминесценцию», Journal of Chemical Education , 11 ( 3) : 142–145. два : 10.1021/ed011p142
- ^ Плес, Марек. «Хемилюминесценция, активируемая кровью» . www.weirdscience.eu (на польском языке). Архивировано из оригинала 3 января 2015 года . Проверено 23 декабря 2014 г.
- ^ Юэ, Линг; Лю, И-Тонг (3 сентября 2020 г.). «Механистический взгляд на pH-зависимую хемилюминесценцию люминола в водном растворе» . Журнал физической химии Б. 124 (35): 7682–7693. doi : 10.1021/acs.jpcb.0c06301 . ISSN 1520-6106 . ПМИД 32790377 . S2CID 221125324 .
- ^ Х.О. Альбрехт (1928) «О хемилюминесценции гидразида аминофталевой кислоты» Журнал физической химии 136 : 321–330.
- ^ Стюарт Х. Джеймс и Уильям Г. Эккерт, Интерпретация следов крови на местах преступлений , 2-е изд. (Бока-Ратон, Флорида: CRC Press LLC, 1998), стр. 154. Архивировано 15 февраля 2017 г. в Wayback Machine .
- ^ Глю, Карл; Пфаннстиль, Карл (1936) «О гидразиде 3-аминофталевой кислоты» Журнал практической химии 146 : 137–150.
- ^ Шпехт, Уолтер (1937) «Хемилюминесценция гемина, помощь в обнаружении и распознавании криминалистически значимых следов крови», Angewandte Chemie 50 (8): 155-157.
- ^ Прошер Ф. и Муди А.М. (1939) «Обнаружение крови с помощью хемилюминесценции», Журнал лабораторной и клинической медицины , 24 : 1183–1189.
- ^ Перейти обратно: а б Джеймс, Стюарт; Киш, Пол Э.; Саттон, Полетт Саттон (2005). Принципы анализа закономерностей кровавых пятен . Бока-Ратон, Лондон, Нью-Йорк, Сингапур: Группа Тейлора и Фрэнсиса. п. 376 . ISBN 0-8493-2014-3 .
- ^ Плес, Марек. «Хемилюминесценция люминола, активированного соединением меди» . www.weirdscience.eu (на польском языке). Архивировано из оригинала 3 января 2015 года . Проверено 23 декабря 2014 г.
- ↑ Техническая записка о Hemaglow. Архивировано 2 января 2015 г. в Wayback Machine.

