Эпоксидокозапентаеновая кислота
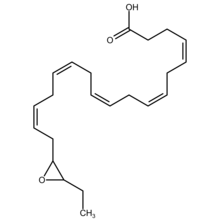
Эпоксид докозапентаеновые кислоты ( эпоксидокозапентаеновые кислоты , EDP или EpDPE ) представляют собой метаболиты 22-углеродной прямой жирной кислоты омега-3 , докозагексаеновой кислоты (DHA). Типы клеток, которые экспрессируют определенные эпоксигеназы цитохрома P450 (CYP), метаболизируют полиненасыщенные жирные кислоты (ПНЖК), превращая одну из их двойных связей в эпоксид . В наиболее известном из этих метаболических путей клеточные CYP-эпоксигеназы метаболизируют 20-углеродную линейную жирную кислоту омега-6 , арахидоновую кислоту , до эпоксиэйкозатриеновых кислот (EET); другой путь эпоксигеназы CYP метаболизирует 20-углеродную жирную кислоту омега-3, эйкозапентаеновую кислоту (EPA), до эпоксиэйкозатетраеновых кислот (EEQ). Эпоксигеназы CYP аналогичным образом преобразуют различные другие ПНЖК в эпоксиды (см. Эпоксигеназа ). Эти эпоксидные метаболиты обладают разнообразной активностью. Однако по существу все они быстро превращаются в соответствующие, но, как правило, гораздо менее активные вицинальные дигидроксижирные кислоты под действием повсеместно распространенной клеточной растворимой эпоксидгидролазы. (sEH; также называется эпоксидгидролазой 2). Следовательно, эти эпоксиды, включая EDP, действуют как короткоживущие сигнальные агенты, которые регулируют функцию своих родительских или близлежащих клеток. Особенностью EDP (и EEQ), отличающей их от EET, является то, что они происходят из жирных кислот омега-3 и, как предполагается, несут ответственность за некоторые полезные эффекты, приписываемые жирным кислотам омега-3 и продуктам, богатым омега-3, таким как как рыбий жир . [ 1 ]
Структура
[ редактировать ]EDP представляют собой метаболиты эпоксид- эйкозапентаеновой кислоты DHA. ДГК имеет 6 цис-(см. Цис-транс-изомерия ) двойных связей , каждая из которых расположена между атомами углерода 4–5, 7–8, 10–11, 13–14, 16–17 или 19–20. Эпоксигеназы цитохрома P450 атакуют любую из этих двойных связей с образованием соответствующего региоизомера эпоксида докозапентаеновой кислоты (DPA) (см. Структурный изомер § Позиционная изомерия (региоизомерия) ). Таким образом, данная эпоксигеназа может превращать DHA в 4,5-EDP (т.е. 4,5-эпокси-7 Z ,10 Z ,13 Z ,16 Z ,19 Z -DPA), 7,8-EDP (т.е. 7,8- эпоксидная смола-4 Z ,10 Z ,13 Z ,16 Z ,19 Z -DPA), 10,11-EDP (т.е. 10,11-эпоксиди-4 Z ,7 Z ,13 Z ,16 Z ,19 Z -ДПА), 13,14-ЭДФ (т.е. 13,14-эпоксиди-4 Z ,7 Z ,10 Z ,16 Z ,19 Z -DPA), 16,17-EDP (т.е. 16,17-эпоксид-4 Z ,7 Z ,10 Z ,13 Z ,19 Z -DPA или 19,20-EDP (т.е. 19,20-эпокси-4 Z , 7 Z , 10 Z , 13 Z , 16 Z -DPA. Ферменты эпоксигеназы обычно образуют оба R / S -энантиомера в каждом из первых положение двойной связи, например, эпоксидазы цитохрома P450 атакуют DHA в положении 16,17-двойной связи с образованием двух; эпоксидные энантиомеры, 16 R ,17 S -EDP и 16 S ,17 S -EDP. [ 2 ] Метаболит 4,5-EDP нестабилен и обычно не обнаруживается среди EDP, образуемого клетками. [ 3 ]
Производство
[ редактировать ]Ферменты суперсемейства цитохрома P450 (CYP), которые классифицируются как эпоксигеназы на основании их способности метаболизировать ПНЖК, особенно арахидоновую кислоту, до эпоксидов, включают: CYP1A, CYP2B, CYP2C, CYP2E, CYP2J, а в подсемействе CYP3A - CYP3A4. У людей CYP2C8 , CYP2C9 , CYP2C19 , CYP2J2 и, возможно, CYP2S1 изоформы являются основными эпоксигеназами, ответственными за метаболизм арахидоновой кислоты в EET (см. § Производство эпоксиэйкозатриеновой кислоты ). В целом, те же самые эпоксигеназы CYP также метаболизируют DHA в EDP (а также EPA в EEQ; CYP2S1 еще не тестировался на способность метаболизировать DHA), делая это со скоростью, которая часто превышает скорость метаболизма арахидоновой кислоты в EET. ; то есть DHA (и EPA), по-видимому, предпочтительнее арахидоновой кислоты в качестве субстратов для многих эпоксигеназ CYP. [ 4 ] CYP1A1 , CYP1A2 , CYP2C18 , CYP2E1 , CYP4A11 , CYP4F8 и CYP4F12 также метаболизируют DHA до EDP. [ 5 ] CYP2C8, CYP2C18, CYP2E1, CYP2J2, VYP4A11, CYP4F8 и CYP4F12 преимущественно атакуют терминальную двойную связь омега-3, которая отличает DHA от жирных кислот омега-6, и, следовательно, метаболизируют DHA преимущественно до изомеров 19,20-EDP, тогда как CYP2C19 метаболизирует DHA в Изомеры 7,8-ЭДФ, 10,11-ЭДФ и 19,20-ЭДФ [ 5 ] [ 6 ] CYP2J2 метаболизирует DHA в EPA, главным образом в 19,20-EPA, в два раза быстрее, чем метаболизирует арахидоновую кислоту в EET. [ 7 ] В дополнение к указанным CYP, CYP4A11 , CYP4F8 , CYP4F12 , CYP1A1 , CYP1A2 и CYP2E1 , которые классифицируются как монооксигеназы CYP, а не эпоксигеназы CYP, поскольку они метаболизируют арахидоновую кислоту до моногидроксиэйкозатетраеновых кислот (см. 20-Гидроксикозатетраеновая кислота ), т.е. 19-гидроксиэйкозатетраеновая кислота и/или 20-гидроксиэйкозатетраеновая кислота, приобретают эпоксигеазную активность при превращении DHA преимущественно в изомеры 19,20-EDP (см. Эпоксиэйкозатриеновая кислота ). [ 5 ] Эпоксигеназы CYP450, способные метаболизировать DHA в EDP, широко распространены в органах и тканях, таких как печень, почки, сердце, легкие, поджелудочная железа, кишечник, кровеносные сосуды, лейкоциты крови и мозг. [ 8 ] [ 9 ] Известно, что эти ткани метаболизируют арахидоновую кислоту до EET; было показано или предполагается, что они также метаболизируют DHA в EPD. [ 10 ] [ 11 ] [ 12 ]
EDP обычно производятся путем стимуляции определенных типов клеток с помощью тех же механизмов, которые производят EET (см. Эпоксиэйкозатриеновая кислота ). То есть стимуляция клеток вызывает высвобождение DHA из позиции sn-2 их мембраносвязанных клеточных фосфолипидных пулов посредством действия фермента типа фосфолипазы А2 и последующей атаки высвобожденной DHA эпоксидазой CYP450. Примечательно, что потребление продуктов, богатых жирными кислотами омега-3, резко повышает уровни EDP и EEQ в сыворотке и тканях как у животных, так и у людей. Действительно, это повышение уровней EDP (и EEQ) у людей на сегодняшний день является наиболее заметным изменением в профиле метаболитов ПНЖК, вызванным пищевыми жирными кислотами омега-3, и, как предполагается, может быть ответственным, по крайней мере, за некоторые из полезных эффектов. эффекты, приписываемые пищевым жирным кислотам омега-3. [ 1 ] [ 13 ]
Метаболизм ЭДП
[ редактировать ]Подобно EET (см. Эпоксиэйкозатриеновая кислота ), EDP быстро метаболизируются в клетках цитозольной растворимой эпоксидгидролазой (sEH, также называемой эпоксидгидролазой 2 [EC 3.2.2.10.]) с образованием соответствующих вицинальных диолдигидроксиэйкозапентаеновых кислот. Так, sEH превращает 19,20-EDP в 19,10-дигидроксидокозапентаеновую кислоту (DPA), 16,17-EDP в 16,17-дигидрокси-DPA, 13,14-EDP в 13,14-дигидрокси-DPA, 10, 11-EDP в 10,11-дигидрокси-DPA и от 7,8-ЭДФ до 7,8-дигидрокси-ЭДФ; 4,5-ЭДФ нестабилен и поэтому обычно не обнаруживается в клетках. [ 14 ] Продукты дигидрокси-ЭДФ, как и их эпоксидные предшественники, представляют собой энантиомеров смеси ; например, sEH превращает 16,17-EDP в смесь 16( S ),17( R )-дигидрокси-ДФА и 16( R ),17( S )-дигидрокси-ДФА. [ 2 ] Эти дигидрокси-ДПА обычно гораздо менее активны, чем их эпоксидные предшественники. Путь sEH действует быстро и на сегодняшний день является преобладающим путем инактивации EDP; его действие заставляет EDP функционировать как короткоживущие медиаторы, действие которых ограничено родительскими и близлежащими клетками, т.е. они являются аутокринными и паракринными сигнальными агентами соответственно. [ 14 ] [ 15 ] [ 16 ]
В дополнение к пути sEH, EDP, подобно EET, могут ацилироваться в фосфолипиды в реакции, подобной ацилированию ; этот путь может служить для ограничения действия EET или сохранения их для будущего выпуска. [ 2 ] Наконец, как и EET, EDP подвергаются инактивации в результате дальнейшего метаболизма посредством бета-окисления . [ 17 ]
Клиническое значение
[ редактировать ]EDP изучены не так хорошо, как EET. Это особенно относится к исследованиям на животных их потенциальной клинической значимости. По сравнению с некоторыми видами активности, приписываемыми EET (см. Эпоксиэйкозатриеновая кислота ), исследования на животных, о которых сообщалось на сегодняшний день, показывают, что некоторые EDP (чаще всего исследовались 16,17-EDP и 19,20-EDP): 1) более эффективен, чем ЭЭТ, в снижении гипертензии и восприятия боли; 2) более эффективное подавление воспаления или, по крайней мере, равное по эффективности EET; и 3) действуют противоположно EET, поскольку EDP ингибируют ангиогенез , миграцию эндотелиальных клеток, пролиферацию эндотелиальных клеток, а также рост и метастазирование клеточных линий рака молочной железы и простаты человека, тогда как EET оказывают стимулирующее действие на каждую из этих систем. [ 1 ] [ 3 ] [ 16 ] [ 17 ] Как указано в разделе «Метаболизм», потребление диеты, богатой жирными кислотами омега-3, резко повышает уровни EDP и EEQ в сыворотке и тканях как у животных, так и у людей, а у людей это, безусловно, наиболее заметное изменение в профиле метаболитов ПНЖК. вызвано пищевыми жирными кислотами омега-3. Следовательно, метаболизм DHA в EDP (и EPA в EEQ) может быть ответственным, по крайней мере, за некоторые полезные эффекты, приписываемые диетическим жирным кислотам омега-3. [ 1 ] [ 13 ] [ 17 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д Флеминг, я (2014). «Фармакология оси цитохром P450 эпоксигеназа/растворимая эпоксидгидролаза в сосудистой и сердечно-сосудистой системе» . Фармакологические обзоры . 66 (4): 1106–40. дои : 10.1124/пр.113.007781 . ПМИД 25244930 .
- ^ Jump up to: а б с Спектор, А.А.; Ким, HY (2015). «Эпоксигеназный путь цитохрома P450 метаболизма полиненасыщенных жирных кислот» . Biochimica et Biophysical Acta (BBA) - Молекулярная и клеточная биология липидов . 1851 (4): 356–65. дои : 10.1016/j.bbalip.2014.07.020 . ПМК 4314516 . ПМИД 25093613 .
- ^ Jump up to: а б Чжан, Г; Кодани, С; Гамак, Б.Д. (2014). «Стабилизированные эпоксигенированные жирные кислоты регулируют воспаление, боль, ангиогенез и рак» . Прогресс в исследованиях липидов . 53 : 108–23. дои : 10.1016/j.plipres.2013.11.003 . ПМЦ 3914417 . ПМИД 24345640 .
- ^ Фремель, Т; Флеминг, я (2015). «Что случилось с гиперполяризующим фактором, подобным эпоксиэйкозатриеновой кислоте, происходящим из эндотелия? Идентификация новых классов липидных медиаторов и их роли в сосудистом гомеостазе». Антиоксиданты и окислительно-восстановительная сигнализация . 22 (14): 1273–92. дои : 10.1089/ars.2014.6150 . ПМИД 25330284 .
- ^ Jump up to: а б с Вестфаль, К; Конкель, А; Шунк, WH (2011). «CYP-эйкозаноиды — новая связь между жирными кислотами омега-3 и сердечно-сосудистыми заболеваниями?». Простагландины и другие липидные медиаторы . 96 (1–4): 99–108. doi : 10.1016/j.prostaglandins.2011.09.001 . ПМИД 21945326 .
- ^ Фер, М; Дреано, Ю; Лукас, Д; Коркос, Л; Салаун, Япония; Берту, Ф; Амет, Ю (2008). «Метаболизм эйкозапентаеновой и докозагексаеновой кислот рекомбинантными цитохромами человека P450». Архив биохимии и биофизики . 471 (2): 116–25. дои : 10.1016/j.abb.2008.01.002 . ПМИД 18206980 .
- ^ Конкель, А; Шунк, WH (2011). «Роль ферментов цитохрома P450 в биоактивации полиненасыщенных жирных кислот». Biochimica et Biophysical Acta (BBA) - Белки и протеомика . 1814 (1): 210–22. дои : 10.1016/j.bbapap.2010.09.009 . ПМИД 20869469 .
- ^ Спектор, А.А. (2009). «Путь эпоксигеназы цитохрома P450 арахидоновой кислоты» . Журнал исследований липидов . 50 (Приложение): S52–6. doi : 10.1194/jlr.R800038-JLR200 . ПМЦ 2674692 . ПМИД 18952572 .
- ^ Сюй, М; Джу, Вт; Хао, Х; Ван, Дж; Ли, П. (2013). «Цитохром P450 2J2: распространение, функции, регуляция, генетический полиморфизм и клиническое значение». Обзоры метаболизма лекарств . 45 (3): 311–52. дои : 10.3109/03602532.2013.806537 . ПМИД 23865864 . S2CID 22721300 .
- ^ Ким Х.С., Мун С.Дж., Ли С.Э., Хван Г.В., Ю Х.Дж., Сон Дж.В. (май 2021 г.). «Метаболит арахидоновой кислоты 11,12-эпоксиэйкозатриеновая кислота облегчает фиброз легких» . Эксп Мол Мед . 53 (5): 864–874. дои : 10.1038/s12276-021-00618-7 . ПМЦ 8178404 . ПМИД 33990688 .
- ^ Гросс Г.Дж., Фальк Дж.Р., Гросс Э.Р., Исбелл М., Мур Дж., Нитипатиком К. (октябрь 2005 г.). «Цитохром P450 и метаболиты арахидоновой кислоты: новый взгляд на роль в ишемии / реперфузионном повреждении миокарда». Кардиоваскулярный рез . 68 (1): 18–25. doi : 10.1016/j.cardiores.2005.06.007 . ПМИД 15993870 .
- ^ Ван Б, Ву Л, Чен Дж, Донг Л, Чен С, Вэнь Цз, Ху Дж, Флеминг И, Ван Д.В. (2021). «Пути метаболизма арахидоновой кислоты: механизмы и потенциальные терапевтические цели» . Сигнальная трансдукция и таргетная терапия . 6 (1): 94. doi : 10.1038/s41392-020-00443-w . ПМК 7910446 . ПМИД 33637672 .
- ^ Jump up to: а б Фишер, Р; Конкель, А; Мехлинг, Х; Блосси, К; Гапелюк А; Вессель, Н.; фон Шаки, К; Дехенд, Р; Мюллер, Д.Н.; Роте, М; Люфт, ФК; Вейландт, К; Шунк, WH (2014). «Пищевые жирные кислоты омега-3 модулируют профиль эйкозаноидов у человека главным образом посредством CYP-эпоксигеназного пути» . Журнал исследований липидов . 55 (6): 1150–1164. дои : 10.1194/jlr.M047357 . ПМК 4031946 . ПМИД 24634501 .
- ^ Jump up to: а б Харрис, TR; Гамак, Б.Д. (2013). «Растворимая эпоксидгидролаза: структура гена, экспрессия и делеция» . Джин . 526 (2): 61–74. дои : 10.1016/j.gene.2013.05.008 . ПМЦ 3733540 . ПМИД 23701967 .
- ^ Беллиен, Дж; Джоаннидес, Р. (2013). «Путь эпоксиэйкозатриеновой кислоты в здоровье и заболеваниях человека». Журнал сердечно-сосудистой фармакологии . 61 (3): 188–96. дои : 10.1097/FJC.0b013e318273b007 . ПМИД 23011468 . S2CID 42452896 .
- ^ Jump up to: а б Он, Дж; Ван, К; Чжу, Ю; Ай, Д (2016). «Растворимая эпоксидгидролаза: потенциальная мишень метаболических заболеваний» . Журнал диабета . 8 (3): 305–13. дои : 10.1111/1753-0407.12358 . ПМИД 26621325 .
- ^ Jump up to: а б с Вагнер, К; Вито, С; Инджеоглу, Б; Гамак, Б.Д. (2014). «Роль длинноцепочечных жирных кислот и их эпоксидных метаболитов в передаче ноцицептивных сигналов» . Простагландины и другие липидные медиаторы . 113 : 2–12. doi : 10.1016/j.prostaglandins.2014.09.001 . ПМЦ 4254344 . ПМИД 25240260 .