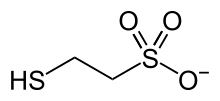
Коэнзим М
 | |
| Имена | |
|---|---|
| Название ИЮПАК 2-Сульфанилэтансульфонат | |
| Систематическое название ИЮПАК 2-Сульфанилэтансульфонат | |
| Другие имена 2-меркаптоэтилсульфонат; 2-меркаптоэтансульфонат; кофермент Манион; HS-CoM; AC1L1HCY; 2-сульфанилэтан-1-сульфонат; CTK8A8912 | |
| Идентификаторы | |
| |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ХимическийПаук | |
ПабХим CID | |
| НЕКОТОРЫЙ |
|
| Характеристики | |
| С 2 Н 5 О 3 С 2 | |
| Молярная масса | 141.18 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Коэнзим М — кофермент, для реакций переноса метила в метаболизме метаногенов архей необходимый . [1] [2] и в метаболизме других субстратов у бактерий . [3] Он также является необходимым кофактором метаболического пути алкен-окисляющих бактерий. CoM помогает устранить токсичные эпоксиды, образующиеся в результате окисления алкенов, таких как пропилен. [4] Структура этого кофермента была открыта К. Д. Тейлором и Р. С. Вулфом в 1974 году, когда они изучали метаногенез — процесс, посредством которого углекислый газ превращается в метан у некоторых архей. [5] Кофермент представляет собой анион с формулой HSCH.
2 СН
2 ТАК −
3 . Он получил название 2-меркаптоэтансульфонат и сокращенно HS–CoM . Катион наиболее неважен, но натриевая соль доступна . Меркаптоэтансульфонат содержит как тиол , который является основным центром реакционной способности, так и сульфонатную группу, которая придает растворимость в водных средах.
Биохимическая роль
[ редактировать ]Метаногенез
[ редактировать ]Коэнзим является донором С1 в метаногенезе . Он превращается в тиоэфир метилкофермента М, тиоэфир CH.
3 СЧ
2 СН
2 ТАК −
3 , на предпоследнем этапе образования метана . [6] Метил-кофермент M реагирует с коферментом B , 7-тиогептаноилтреонинфосфатом, с образованием гетеродисульфида, выделяя метан:
- CH 3 –S–CoM + HS–CoB → CH 4 + CoB–S–S–CoM
Эта индукция катализируется ферментом метилкоэнзим М-редуктазой , который ограничивает кофактор F430 в качестве простетической группы .
Алкеновый метаболизм
[ редактировать ]Коэнзим М также используется для получения ацетоацетата из CO 2 и пропилена или этилена у аэробных бактерий. В частности, у бактерий, окисляющих алкены в эпоксиды. После того как пропилен (или другой алкен) подвергается эпоксидированию и становится эпоксипропаном, он становится электрофильным и токсичным. Эти эпоксиды реагируют с ДНК и белками, влияя на функцию клеток. Бактерии, окисляющие алкены, такие как Xanthobacter autotropicus. [4] используют метаболический путь, при котором СоМ конъюгируется с алифатическим эпоксидом. На этом этапе создается нуклеофильное соединение, которое может реагировать с CO 2 . В результате карбоксилирования образуется ацетоацетат, расщепляющий пропилен. [4]
См. также
[ редактировать ]- Месна - адъювант химиотерапии рака той же структуры.
Ссылки
[ редактировать ]- ^ Балч В.Е., Вулф Р.С. (1979). «Специфичность и биологическое распределение кофермента М (2-меркаптоэтансульфоновой кислоты)» . Дж. Бактериол . 137 (1): 256–63. дои : 10.1128/JB.137.1.256-263.1979 . ПМК 218444 . ПМИД 104960 .
- ^ Тейлор CD, Вулф RS (10 августа 1974 г.). «Структура и метилирование кофермента М( HSCH
2 СН
2 ТАК
3 )" . J. Biol. Chem . 249 (15): 4879–85. doi : 10.1016/S0021-9258(19)42403-4 . PMID 4367810 . - ^ Партови, Сара Э.; Мюс, Флоренция; Гуткнехт, Эндрю Э.; Мартинес, Хантер А.; Трипет, Брайан П.; Ланге, Бернд Маркус; Дюбуа, Дженнифер Л.; Питерс, Джон В. (06 апреля 2018 г.). «Биосинтез коэнзима М у бактерий включает удаление фосфата с помощью функционально отличного члена суперсемейства аспартазы/фумаразы» . Журнал биологической химии . 293 (14): 5236–5246. дои : 10.1074/jbc.RA117.001234 . ISSN 1083-351X . ПМЦ 5892593 . ПМИД 29414784 .
- ^ Jump up to: а б с Кришнакумар, Арати М.; Слива, Дариус; Эндрицци, Джеймс А.; Бойд, Эрик С.; Прапорщик, Скотт А.; Питерс, Джон В. (сентябрь 2008 г.). «Понимание роли коэнзима М в метаболизме алкенов» . Обзоры микробиологии и молекулярной биологии . 72 (3): 445–456. дои : 10.1128/MMBR.00005-08 . ISSN 1092-2172 . ПМК 2546864 . ПМИД 18772284 .
- ^ Парри, Рональд Дж. (1 января 1999 г.), Бартон, сэр Дерек; Наканиси, Кодзи; Мет-Кон, Отто (ред.), «1.29 – Биосинтез серосодержащих натуральных продуктов» , Комплексная химия натуральных продуктов , Оксфорд: Пергамон, стр. 825–863, номер документа : 10.1016/b978-0-08-091283-7.00031 -х , ISBN 978-0-08-091283-7 , получено 10 мая 2022 г.
- ^ Тауэр, Рудольф К. (1 сентября 1998 г.). «Биохимия метаногенеза: дань уважения Марджори Стивенсон: лекция о премии Марджори Стивенсон 1998 года» . Микробиология . 144 (9): 2377–2406. дои : 10.1099/00221287-144-9-2377 . ISSN 1350-0872 . ПМИД 9782487 .