Спермидинсинтаза
| спермидинсинтаза | |||
|---|---|---|---|
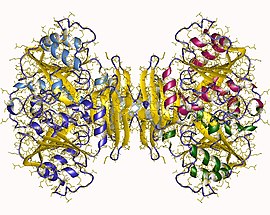 Тетрамер спермидинсинтазы, Bacillus subtilis | |||
| Идентификаторы | |||
| Символ | СРМ | ||
| Альт. символы | СРМЛ1 | ||
| ген NCBI | 6723 | ||
| HGNC | 11296 | ||
| МОЙ БОГ | 182891 | ||
| RefSeq | НМ_003132 | ||
| ЮниПрот | P19623 | ||
| Другие данные | |||
| Номер ЕС | 2.5.1.16 | ||
| Локус | Хр. 1 п36-п22 | ||
| |||
Спермидинсинтаза - фермент ( EC 2.5.1.16 ), катализирующий перенос пропиламиновой группы от S -аденозилметионинамина к путресцину при биосинтезе спермидина . Систематическое название — S-аденозил-3-(метилтио)пропиламин:путресцин-3-аминопропилтрансфераза, и он принадлежит к группе аминопропилтрансфераз. Ему не нужны никакие кофакторы. Большинство спермидинсинтаз существует в растворе в виде димеров. [ 1 ]
Специфика
[ редактировать ]За исключением спермидинсинтаз Thermotoga maritimum и Escherichia coli , которые акцептируют различные виды полиаминов, все ферменты высокоспецифичны к путресцину. [ 2 ] Ни одна известная спермидинсинтаза не может использовать S -аденозилметионин . Этому препятствует консервативный аспартатильный остаток в активном центре, который, как полагают, отталкивает карбоксильную часть S -аденозилметионина. [ 3 ] Путресцин -N-метилтрансфераза, субстратами которой являются путресцин и S -аденозилметионин и которая эволюционно родственна спермидинсинтазам, лишена этого аспартильного остатка. [ 4 ] С помощью некоторых мутаций можно даже преобразовать спермидинсинтазу в функциональную путресцин-N-метилтрансферазу. [ 5 ]
Механизм
[ редактировать ]Предполагается, что синтез спермидина происходит по S n 2 -механизму . [ 6 ] Существует некоторая неопределенность, происходит ли реакция по механизму пинг-понга или по механизму тройного комплекса . Некоторые кинетические данные, но не все, предполагают механизм пинг-понга. [ 7 ] в то время как исследование стереохимического пути реакции свидетельствует в пользу тройного сложного механизма. [ 8 ] Перед нуклеофильной атакой путресцина на S -аденозилметионинамин путресцин должен быть депротонирован, что делает азот нуклеофильным, поскольку путресцин протонируется при физиологическом pH и, следовательно, неактивен.
Ингибиторы
[ редактировать ]Спермидинсинтазу можно ингибировать с помощью широкого спектра аналогов путресцина, S -аденозилметионинамина и аналогов переходного состояния, таких как Адодато (дополнительную информацию см. здесь ).
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Икегути Ю., Бьюли М.К., Пегг А.Е. (январь 2006 г.). «Аминопропилтрансферазы: функция, структура и генетика». Журнал биохимии . 139 (1): 1–9. дои : 10.1093/jb/mvj019 . ПМИД 16428313 .
- ^ Ву Х, Мин Дж, Икегути Ю, Цзэн Х, Донг А, Лоппнау П, Пегг А.Э., Плотников А.Н. (июль 2007 г.). «Строение и механизм спермидинсинтаз» . Биохимия . 46 (28): 8331–9. дои : 10.1021/bi602498k . ПМИД 17585781 .
- ^ Королев С., Икегути Ю., Скарина Т., Бисли С., Эроусмит С., Эдвардс А., Йоахимиак А., Пегг А.Е., Савченко А. (январь 2002 г.). «Кристаллическая структура спермидинсинтазы с мультисубстратным ингибитором аддукта» . Структурная биология природы . 9 (1): 27–31. дои : 10.1038/nsb737 . ПМК 2792006 . ПМИД 11731804 .
- ^ Биастофф С., Брандт В., Дрегер Б. (01.10.2009). «Путрецин N-метилтрансфераза - начало алкалоидов». Фитохимия . Эволюция метаболического разнообразия. 70 (15–16): 1708–18. Бибкод : 2009PChem..70.1708B . doi : 10.1016/j.phytochem.2009.06.012 . ПМИД 19651420 .
- ^ Юнкер А., Фишер Дж., Зиххарт Ю., Брандт В., Дрегер Б. (01.01.2013). «Эволюция ключевого алкалоидного фермента путресцин-N-метилтрансферазы из спермидинсинтазы» . Границы в науке о растениях . 4 : 260. дои : 10.3389/fpls.2013.00260 . ПМЦ 3725402 . ПМИД 23908659 .
- ^ Голдинг Б., Насереддин Л.К., Биллингтон Д. «Биосинтез спермидина. Часть I: Биосинтез спермидина из L-[3,4-13C2] метионина и L-[2,3,3-2H3] метионина». Дж. Хим. Соц. Перкин Транс .
- ^ Юн СО, Ли Ю.С., Ли Ш., Чо Ю.Д. (июнь 2000 г.). «Синтез полиаминов в растениях: выделение и характеристика спермидинсинтазы из осей сои (Glycine max)». Biochimica et Biophysical Acta (BBA) – Общие предметы . 1475 (1): 17–26. дои : 10.1016/s0304-4165(00)00039-8 . ПМИД 10806333 .
- ^ Голдинг Б., Насередин I (1985). «Биосинтез спермидина. Часть 3: Стереохимия образования группы N-CH2 в биосинтезе спермидина». Дж. Хим. Соц. Перкин Транс. : 2017. дои : 10.1039/P19850002017 .
Внешние ссылки
[ редактировать ]- Спермидинсинтаза в BRENDA
- Спермидинсинтаза в ExPASy
- Спермидин + синтаза Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)