Соединения гомолептической кислоты
Гомолептические азидосоединения представляют собой химические соединения, в которых единственным анионом или лигандом является азидная группа -N 3 . Спектр гомолептических азидных соединений охватывает почти всю таблицу Менделеева. [ 1 ] За редкими исключениями, азидосоединения очень чувствительны к ударам, и с ними следует обращаться с особой осторожностью. Бинарные азидные соединения могут иметь несколько различных структур, включая дискретные соединения, одно-, двух- и трехмерные сети, что заставляет некоторых называть их «полиазидами». [ 2 ] Исследования реакционной способности азидных соединений относительно ограничены из-за их чувствительности. Чувствительность этих соединений имеет тенденцию коррелировать с количеством ионного или ковалентного характера связи азид-элемент, причем ионный характер гораздо более стабильен, чем ковалентный характер. [ 3 ] Следовательно, такие соединения, как азид серебра или натрия, обладающие сильным ионным характером, имеют тенденцию обладать большей синтетической полезностью, чем их ковалентные аналоги. [ 1 ] Несколько других заметных исключений включают полимерные сетки, обладающие уникальными магнитными свойствами, азиды группы 13, которые, в отличие от большинства других азидов, разлагаются до нитридных соединений (важных материалов для полупроводников), другие ограниченные применения в качестве синтетических реагентов для переноса азидных групп или для исследования материя с высокой плотностью энергии . [ 2 ] [ 4 ] [ 5 ] [ 6 ]
Синтез
[ редактировать ]
Существует несколько общих путей и стратегий, используемых при синтезе гомолептических азидосоединений. метатезиса соли между азидной солью, такой как азид натрия или азид серебра , и хлоридом металла. Многие ранние азиды были получены путем [ 7 ] Другой популярный путь включает кислотно-основные реакции с азотистоводородной кислотой HN 3 и комплексами оснований гидрида или Льюиса. [ 7 ] Однако современные методы часто полагаются на галогенид-азидный обмен триметилсилилазидом SiMe 3 N 3 с фторидами металлов, поскольку при использовании хлоридных производных часто наблюдается неполный галогенид-азидный обмен. [ 7 ] [ 3 ]

Нейтральные бинарные азиды довольно трудно изучать из-за флюкционной природы азидо-лигандов и отсутствия у них термической и ударной стабильности. [ 3 ] Их недостаточная стабильность частично обусловлена ковалентным связыванием азидо-лиганда с металлическим центром, что благоприятствует одинарной и тройной связи в азидном фрагменте . Увеличение ионного характера азидогруппы - либо за счет образования аниона, либо за счет N-донорных аддуктов - вместо этого благоприятствует образованию двух двойных связей. [ 3 ] [ 8 ] Таким образом, этот мотив ионной связи увеличивает активационный барьер для разрыва связи NN с высвобождением N 2 и помогает стабилизировать соединения. Полученные соединения по-прежнему могут быть очень чувствительными к ударам , и с ними необходимо обращаться с осторожностью.
Переходные металлы
[ редактировать ]Группа 3
[ редактировать ]Нейтральный несольватированный полиазид группы 3 известен только для соединения двухвалентного европия(II) Eu(N 3 ) 2 . [ 9 ] Попытки взаимодействия гидроксидов лантаноидов с HN 3 приводят к получению их основных азидов Ln(OH)(N 3 ) 2 или Ln(OH) 2 N 3 . [ 10 ]
Группа 4
[ редактировать ]полиазиды группы 4 формулы M(N 3 ) 4 Предполагается, что будут иметь линейные или почти линейные углы MNN в отличие от их аналогов из основной группы , которые, по прогнозам, будут иметь изогнутые углы MNN. [ 11 ] В случае Ti(N 3 ) 4 это доказать не удалось из-за сложности кристаллизации. [ 12 ] Однако включение крупных спейсерных противоионов или аддуктов N-донора значительно облегчает работу с соединениями. В случае [PPh 4 ] 2 [M(N 3 ) 6 ] (M=Ti, Zr, Hf) только аксиальные лиганды демонстрируют близкие к линейным углы MNN, тогда как экваториальные лиганды ближе к изогнутым углам. [ 12 ] [ 13 ] Это отклонение в теории наблюдается также в N-донорных аддуктах. [ 8 ]

Основная гипотеза, объясняющая, почему эти соединения не имеют линейных углов MNN, несмотря на теоретические расчеты, заключается в том, что эти аддукты не являются тетраэдрическими. [ 12 ] В гомолептических тетраэдрических соединениях азот, ближайший к металлическому центру (+IV), расположен таким образом, что три пары валентных электронов могут отдавать свои средства на вакантные d-орбитали металла, и, следовательно, азидо может действовать как тридентатный донорный лиганд. в этом случае ожидаемая координация будет линейной. Поскольку соединения- аддукты не являются тетраэдрическими, азидогруппа может действовать только как монодентатный донор с двумя стерически активными электронными парами, что приводит к искривлению валентных углов MNN.
Группа 5
[ редактировать ]Известны нейтральный бинарный азид V(IV), а также азидо-ионы V(III), V(IV) и V(V). [ 3 ] [ 14 ] Как и нейтральный азид Ti(IV), V(N 3 ) 4 трудно изучать из-за высокой ударной и температурной нестабильности. [ 3 ] Однако [V(N 3 ) 6 ] 2- в сочетании с большим инертным противоионом относительно стабилен и кристаллизуется в виде почти идеального октаэдра . В отличие от V(IV), нейтральный бинарный V(V) не удалось синтезировать, и попытки приводят к восстановлению V(V) до V(IV) с удалением газа N 2 . К счастью, потенциалы окисления анионов ниже, чем у их исходных соединений, поэтому [V(N 3 ) 6 ] - можно сформировать. В отличие от [V(N 3 ) 6 ] 2- , [В(N 3 ) 6 ] - очень чувствителен к ударам и имеет искаженную октаэдрическую симметрию с тремя длинными и тремя короткими связями MN в мерных положениях.
Нейтральные бинарные Nb(N 3 ) 5 и Ta(N 3 ) 5 также существуют, а ацетонитрильные аддукты этих соединений содержат почти линейный азидо-транс к координирующему ацетонитрилу. [ 15 ] Они представляют собой первое свидетельство линейной связи MNN. Соответствующие анионы [Nb(N 3 ) 6 ] - , [Nb(N 3 ) 7 ] 2- , [Та(N 3 ) 6 ] - , и [Ta(N 3 ) 7 ] 2- известны и, соответственно, гораздо менее чувствительны к ударам. [ 15 ] [ 16 ] Структура гексаазидомононионов аналогична структуре других гептаазидомононионов с изогнутыми азидолигандами, несмотря на то, что было предсказано, что они имеют идеальную симметрию S 6 в газовой фазе для [Nb(N 3 ) 6 ). [ 15 ] Гептаазидодианионы обладают одношапочной треугольно-призматической структурой 1/4/2 в отличие от актинидного трианиона [U(N 3 ) 7 ] 3- который кристаллизуется в виде одношапочного октаэдра или пятиугольной бипирамиды. [ 16 ] Известно также, что существует несколько N-донорных аддуктов. [ 17 ] Реакции нейтральных бинарных NbF 5 и TaF 5 в присутствии Me 3 SiN 3 с N-донорами, содержащими малые углы прикуса, такими как 2,2'-бипиридин или 1,10-фенантролин, приводят к продуктам самоионизации типа [M (N 3 ) 4 L 2 ] + [М(N 3 ) 6 ] - (L= N-донор), тогда как N-доноры, содержащие большие углы прикуса, такие как 3,3'-биприидин или 4,4'-бипиридин, образуют нейтральные пентаазидные аддукты M(N 3 ) 5 ·L (L = N-донор) .
Группа 6
[ редактировать ]Оба Mo(N 3 ) 6 и W(N 3 ) 6 были синтезированы, и W(N 3 ) 6 достаточно стабилен, чтобы выращивать монокристаллы . [ 18 ] В отличие от бинарных азидосоединений 4-й и 5-й групп, анионные [Mo(N 3 ) 7 ] - и [W(N 3 ) 7 ] - менее стабильны и более чувствительны к обращению, чем их нейтральные исходные соединения. При нагревании растворов гептаазидо-анионов в MeCN или SO 2 до комнатной температуры тетраазидо-нитридо-ионы [NMo(N 3 ) 4 ] - и [NW(N 3 ) 4 ] - образуются при удалении N 2 .
Группа 7
[ редактировать ]
В азидных соединениях 7-й группы преобладает химия марганца . О первом полиазиде Mn сообщили Wöhler et al. в 1917 году по реакции MnCO 3 с HN 3 с образованием Mn(N 3 ) 2 . [ 19 ] Многие соли двухвалентного Mn были синтезированы и представляют собой настоящие полимерные системы. Азидогруппа может связываться по принципу «конец к концу» (EO) (μ-1,1) или «конец к концу» (EE) (μ-1,3), обычно образуя ферромагнитное или антиферромагнитное соединение соответственно. [ 2 ] [ 20 ] 1D-цепи образуются при использовании бидентатного лиганда 2,2'-бипиридина в качестве противоиона в реакции между Mn(ClO 4 ) 2 • 6H 2 O и избытком NaN 3 . [ 21 ] В результате образуется цепочка с чередующимися мостиками EE и EO, которая предсказуемо дает чередующуюся антиферромагнитно-ферромагнитную связь. Однако, к сожалению, за исключением абсолютного 0К, одномерные системы не обнаруживают магнитного упорядочения . [ 22 ] Поэтому интерес представляют полимеры возрастающей размерности. Двумерная система образуется при взаимодействии MnCl 2 • 4H 2 O и NaN 3 в присутствии 4,4'-дипиридино-N,N'диуксусной кислоты, которая подвергается in situ декарбоксилированию с образованием чередующихся слоев [Mn(N 3 ) 4 ] 2- с EE-мостиковыми азидами и дикатионом 4,4'-дипиридина. [ 23 ] Металлические центры в этом соединении действительно демонстрируют антиферромагнитное взаимодействие, но это строго не связано с наклоном спина из-за необычной центросимметрии мостиковых азидо-лигандов. Другая двумерная структура достигается за счет реакции (PPh 4 ) 2 MnCl 2 с AgN 3 с образованием невзрывоопасного [PPh 4 ] 2 [Mn(N 3 ) 4 ] с чередующимися ионными слоями. [ 24 ]
Первый пример 3D-азидосоединения был синтезирован по реакции Mn(NO 3 ) 2 · 4H 2 O в горячем водном растворе [N(CH 3 ) 4 ][N 3 ], насыщенном HN 3, с образованием [N(CH 3 ) 4 ][Mn(N 3 ) 3 ]. [ 25 ] Это соединение имеет структуру псевдоперовскита с [N(CH 3 ) 4 ] + ионы в полостях между центрами Mn. Азидные фрагменты расположены по принципу ЭЭ, и действительно, это соединение демонстрирует ожидаемое антиферромагнитное поведение. [ 22 ] Аналог цезия Cs[Mn(N 3 ) 3 ] синтезируется таким же образом, но с использованием CsN 3 вместо [N(CH 3 ) 4 ][N 3 ] и структурно уникален по сравнению с тетраметиламмониевой версией. [ 20 ] Для каждых шести координат Mn четыре азидосвязи представляют собой EE, а две - EO вместо всех шести, являющихся EE. Такое расположение приводит к сотовой форме и является редким примером чередующихся ферро-антиферромагнитных взаимодействий в трехмерном твердом теле.
Примеры азидосоединений марганца в более высоких степенях окисления относительно редки. Аддукт триазида -ацетонитрила может быть получен с использованием пути фторидного обмена с получением Mn(N 3 ) 3 CN в виде темно-красного чувствительного к ударам соединения. [ 26 ] При добавлении PPh 4 N 3 соединение диспропорционируется в нечувствительную смесь [PPh 4 ] 2 [Mn(N 3 ) 2 ] и [PPh 4 ] 2 [Mn(N 3 ) 6 ]. Соль Mn(IV) можно получить самостоятельно, используя Cs 2 MnF 6 в качестве исходного материала с получением взрывоопасного Cs 2 [Mn(N 3 ) 6 ].
Группа 8
[ редактировать ]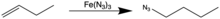
Первым пентакоординационным азидом и девятым тригонально-бипирамидальным соединением был ион пентаазидожелеза (III) [Fe(N 3 ) 5 ] 2- и это соединение может быть получено путем удаления галогенида или нитрата из исходного материала железа (III). [ 27 ] [ 28 ] Однако для применений азиды железа, как правило, не выделяются, а вместо этого генерируются in situ при получении азидоалканов. [ 29 ] NaN 3 и сульфат железа (III) Fe 2 (SO 4 ) 3 объединяют в метаноле и добавляют к органоборану с последующим медленным добавлением 30% перекиси водорода, предположительно образуя Fe(N 3 ) 3 . В сочетании с алкенами азид будет внедряться антимарковниковским способом . [ 5 ] Роль пероксида еще не совсем понятна, но он имеет решающее значение для протекания этой реакции.
рутения Соль тетрабутиламмония можно получить реакцией K 2 [Ru IV Cl 6 ] с NaN 3 в этаноле и воде. [ 30 ] N 2 Выделяется газ восстановленные виды рутения (III) [n-Bu 4 N] 3 [Ru(N 3 ) 6 и образуются ]. Это соединение в значительной степени изучено с точки зрения его оптических свойств.
Группа 9
[ редактировать ]Тетраазидосоединения кобальта(II) были выделены в виде солей тетрафенилфосфония и тетрафениларсония из растворов сульфата кобальта с 15-кратным содержанием NaN 3 с получением [Ph 4 P] 2 [Co(N 3 ) 4 ] и [Ph 4 As ] 2 [Co(N 3 ) 4 ] соответственно. [ 31 ] Автоокисление ) растворов [Co( 3 4 N ] 2- может использоваться в качестве колориметрического точечного теста на наличие сульфит- ионов. [ 32 ]
Тетрабутиламмониевые соли азидов родия(III) и иридия(III) известны и получаются реакцией большого избытка NaN 3 в водном растворе с соответствующей солью хлорида металла Na 3 [MCl 6 ] · 12H 2 O с образованием [n -Bu 4 N] 3 [Rh(N 3 ) 6 ] и [n-Bu 4 N] 3 [Ir(N 3 ) 6 ]. [ 30 ]
Группа 10
[ редактировать ]Азид никеля можно получить путем перегонки HN 3 на карбонат никеля и осаждения ацетоном с получением Ni(N 3 ) 2 . [ 33 ] Образец Ni(N 3 ) 2 начнет быстро разлагаться при нагревании до 490К примерно на 35% с последующим медленным разложением оставшегося материала. Считается, что первая фаза разложения приводит к образованию микрокристаллов с металлическим никелем снаружи и Ni(N 3 ) 2 в ядре. Реакция замедляется, поскольку теперь разложение должно происходить на границе раздела Ni/Ni(N 3 ) 2 .
[Pd(N 3 ) 4 ] 2- анионы имеют плоскую квадратную форму , и степень взаимодействия между анионом и соответствующим ему катионом может быть определена по величине отклонения торсионных углов от идеальной геометрии. [ 34 ] Различные платинаты [Pt(N 3 ) 4 ] 2- и [Pt(N 3 ) 6 ] 4- известны и получаются из хлоридных солей Pt с NaN 3 . [ 30 ] Соли Pt(II), как правило, гораздо менее стабильны, чем версии Pt(IV), и они либо довольно быстро разлагаются при стоянии, либо взрываются. [ 35 ] Их чувствительность частично объясняется плохой упаковкой кристаллов . [ 34 ]
Группа 11
[ редактировать ]Бинарный азид меди(I) CuN 3 представляет собой одномерное ионное соединение с цепями, идущими по диагонали к элементарной ячейке. [ 36 ] Известно множество ионов азидов меди (II) из ряда [Cu(N 3 ) 3 ] - , [Cu(N 3 ) 4 ] 2- и [Cu(N 3 ) 6 ] 2- . [ 27 ] Трехкоординационные комплексы азида меди образуют линейные 1D-цепи с двумя азидо-лигандами EE и одним EO, в отличие от аналога Mn, образующего 3D-структуру. [ 22 ] Двуядерные виды и [Cu(N 3 ) 4 ] 2- оба являются мономерными по своей природе. [ 37 ] Все азиды меди взрывоопасны, но их чувствительность широко варьируется от исходных азидов CuN 3 и Cu(N 3 ) 2 , которые чрезвычайно чувствительны к ионам в паре с крупными противокатионами, практически нечувствительными. [ 1 ]
Азид серебра (I) является хорошо известным взрывчатым соединением, и было продемонстрировано, что он образует двумерный координационный полимер с плоским квадратным серебром. + ионы окружены азидо-лигандами по принципу ЭЭ. [ 38 ] Медленное повышение температуры от 150°C до 251°C приводит к плавлению и медленному разложению, но быстрое нагревание до 300°C приводит к взрыву. [ 1 ]
Азид золота(III) известен как соль тетраэтиламмония [Et 4 N][Au(N 3 ) 4 ] и также имеет плоскую квадратную структуру. [ 30 ] Однако в отличие от азида серебра азид золота нестабилен при комнатной температуре и разлагается через несколько дней, а его металлазидные связи имеют значительный ковалентный характер.
Группа 12
[ редактировать ]Хотя Zn(N 3 ) 2 известен с конца 1890-х годов, Zn(N 3 ) 2 без растворителя был впервые выделен в 2016 году из сухого эфирного раствора HN 3 и Et 2 Zn в н -гексане . [ 39 ] Zn(N 3 ) 2 кристаллизуется в трех различных полиморфах α-Zn(N 3 ) 2 и образуются лабильные β-Zn(N 3 ) 2 и γ - Zn(N 3 ) 2 .

Первый азид ртути (I) был получен Курциусом в 1890 году путем объединения водных солей ртути (I) с азидами щелочных металлов или путем объединения HN 3 с элементарной ртутью с получением Hg 2 (N 3 ) 2 , о чем свидетельствует локализация электронов. функцию соединение стабилизируется за счет ионных связей между азидо-лигандами N 3 - и ртуть + и ковалентная связь между + Hg-Hg + . [ 40 ] [ 41 ] Азиды ртути (I) и ртути (II) можно легко получить путем смешивания соответствующих нитратов ртути с азидом натрия в водном растворе при комнатной температуре. [ 41 ] Азид ртути (II) Hg(N 3 ) 2 существует в двух полиморфных модификациях α-Hg(N 3 ) 2 и β-Hg(N 3 ) 2. β-форма очень лабильна и при комнатной температуре быстро превращается в α-полиморфы. . Однако β-полиморф можно получить аналогично β-Pb(N 3 ) 2 путем медленной диффузии водного NaN 3 в раствор Hg(NO 3 ) 2 , отделенный слоем водного NaNO 3 , но кристаллы почти всегда взрываются при образование, приводящее к смеси полиморфов α и β.
Бинарный азид кадмия Cd(N 3 ) 2 можно получить из CdCO 3 и водного раствора HN 3 . [ 42 ] Однако он структурно не связан с аналогами ртути или цинка и основан на повторяющихся звеньях двойных октаэдров Cd 2 (N 3 ) 10 .
Соединения основной группы
[ редактировать ]Группа 13
[ редактировать ]Триазид бора был впервые получен добавлением диборана к эфирному раствору HN 3 с получением B(N 3 ) 3 . Соединение относительно летучее и может подвергаться взрывному разложению при температуре выше -35°C. [ 43 ] Напротив, азид алюминия Al(N 3 ) 3 относительно стабилен и дефлагируется только при проведении спичечного теста. [ 1 ] Однако он гидролитически разлагается в течение нескольких минут под воздействием атмосферной влаги. Al(N 3 ) 3 имеет некоторые синтетические применения и при образовании in situ может реагировать с β-ненасыщенными цианоэфирами с образованием тетразолов в больших объемах. [ 44 ] газофазные реакции AlMe 3 и HN 3 Сообщалось, что приводят к образованию Al(N 3 ) 3 . Однако при комнатной температуре это соединение разлагается на AlN 2 и AlN, что позволяет предположить, что Al(N 3 ) 3 можно использовать для получения AlN. [ 45 ]
Из-за интереса к GaN как полупроводнику в химии азидогруппы 13 преобладают азиды галлия. [ 4 ] [ 46 ] Na[Ga(N 3 ) 4 ] представляет собой полимерную трехмерную сетку с мостиковыми азидами ЭО. [ 46 ] Это соединение служит ценным предшественником для синтеза донорно-стабилизированных мономерных триазидов галлия Ga(N 3 ) 3 L m , которые при нагревании разлагаются до полимера [Ga(N 3 ) 3 ] ∞ и после детонации образуют GaN. [ 46 ] [ 47 ] [ 48 ] Ga(N 3 ) 3 легко анализируется в виде его тетрафосфониевой соли [PPh 4 ] 2 [Ga(N 3 ) 5 ]. [ 4 ] Повышенная ионность азидо-лигандов и присутствие двух крупных противоионов, которые уменьшают распространение удара, делают соединение значительно менее чувствительным.
Азид индия In(N 3 ) 3 также может быть получен путем фторидного обмена и стабилизируется аналогично тетрафосфониевой соли [PPh 4 ] 3 [In(N 3 ) 6 ). [ 4 ]
Азид таллия (I) TlN 3 взрывается при механическом или термическом ударе, но он имеет более низкую чувствительность к удару, чем родственные азиды ртути или свинца. [ 49 ] Интересно, что TlN 3 — один из немногих азидов, который плавится перед взрывом. [ 1 ] Его чувствительность к трению наиболее высока в тонких слоях, поэтому с ним следует обращаться осторожно. Азид таллия (III) Tl(N 3 ) 3 недавно был синтезирован методом фторид-азидного обмена, но полученное соединение очень чувствительно, и кристаллы можно анализировать только в виде тетрафосфониевой соли [PPh 4 ] 3 [Tl(N 3 ) 6 ]. [ 4 ]
Группа 14
[ редактировать ]Диазидо- и триазидометан можно получить простым нуклеофильным замещением метиленхлорида или бромоформа соответственно азид-ионом на четвертичной аммиачной смоле. [ 11 ] [ 50 ] Следует избегать растворов диазидометана с чистотой более 70 %, поскольку они имеют тенденцию взрываться при любом незначительном механическом воздействии, например при пипетировании. Тетраазидометан C(N 3 ) 4 не может быть получен из тетрагалогенидов углерода, а может быть получен реакцией трихлорацетонитрила Cl 3 CCN с NaN 3, хотя и с относительно низкими выходами. [ 51 ] Выходы можно значительно улучшить путем взаимодействия гексахлорантимоната триазидометилия [C(N 3 ) 3 ][SbCl 6 ] с азидом натрия или лития LiN 3 ; этот маршрут несет в себе высокий риск случайного взрыва. В общем, следует избегать использования чистого тетраазидометана и даже с растворами не следует обращаться вручную. Соединение может взорваться произвольно в любой момент без видимой причины, а единичная капля способна разбить стекло и вакуумные сосуды Дьюара.
В отличие от углеродного аналога тетраазид кремния Si(N 3 ) 4 можно получить из SiCl 4 и NaN 3 . [ 52 ] Однако эта реакция также приведет к осаждению различных количеств хлоразидов кремния, чего можно избежать, продлевая время реакции. Кроме того, в отличие от азидов бора и алюминия, Si(N 3 ) 4 не может быть получен реакцией SiH 4 и HN 3 . Соль гексаазидосикальта [(Ph 3 P) 2 N] 2 [Si(N 3 ) 6 ] существует и имеет очень редкий октаэдрический каркас SiN 6 . [ 53 ]
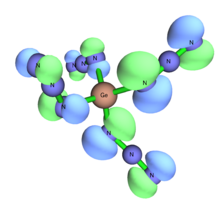
Существование тетраазида германия Ge(N 3 ) 4 в чистой форме не подтверждено, и при попытках его синтеза предполагается, что он частично галогенирован. [ 54 ] Однако, в отличие от своих аналогов из переходных металлов (см. группу 4), прогнозируется, что он будет иметь изогнутые углы Ge-N, а не линейные. [ 11 ] При переключении растворителя с неполярного на полярный NaN 3 , используемый в реакции, становится гораздо более растворимым и приводит к гексаазидогерманату Na 2 [Ge(N 3 ) 6 ). [ 55 ] Наличие слабокоординирующего противоиона, такого как тетрафениларсоний, позволяет образовывать низковалентные германаты из трихлорид-аниона с образованием германия (II) [Ge(N 3 ) 3 ] - он не превратится в германий (IV) при дальнейшем воздействии NaN 3 , но низковалентные соли очень склонны к окислению. [ 56 ]
Исходное соединение Sn(IV) не описано, а о нейтральном Sn(N 3 ) 4 сообщалось только со вспомогательными лигандами. [ 57 ] Реакции с SnCl 4 и NaN 3 вместо этого приводят к гексаазидо Na 2 Sn(N 3 ) 6 , гораздо более стабильному соединению, чем его аналоги в группе 14. [ 58 ] Соль незначительно чувствительна к воде и сгорает при испытании на пламя. Низковалентные станнаты типа [Sn(N 3 ) 3 ] - синтезированы и, как и аналогичные германаты, являются очень чувствительными соединениями. [ 56 ] По-видимому, они не имеют стерически активной неподеленной пары и имеют тенденцию к димеризации при взаимодействиях EE.
Азид свинца является одним из наиболее распространенных гомолептических азидов из-за его повсеместного использования в качестве основного взрывчатого вещества. [ 1 ] Уникально то, что это единственный азид группы 14, в котором более распространен двухвалентный Pb. 2+ форма. Полиморфы α, β, γ и ∂ существуют, но форма α — единственная, которая находит широкое техническое применение. Гомолептические азиды Pb(IV) существуют, но, как и оловянные версии, Pb(N 3 ) 4 не является стабильным соединением, и попытки синтезировать его из PbO 2 и HN 3 образуют красные иглы, которые быстро взрываются и разлагаются до Pb(N 3 ). 2 . [ 59 ] Однако соединение можно выделить в виде [Pb(N 3 ) 6 ] 2- ионы с крупными органическими катионами с получением невзрывоопасного соединения. [ 1 ]
Группа 15
[ редактировать ]В общем смысле азиды элементов 15-й группы имеют тенденцию напоминать их хлориды, но с более высокой летучестью и меньшей термостабильностью. [ 1 ] Соединения, богатые азотом, такие как N(N 3 ) 3 , считались возможными синтетически, но еще не были созданы. [ 60 ]
Триазид фосфора P(N 3 ) 3 может быть синтезирован реакцией NaN 3 и PCl 3 , но успешного синтеза ионного азидосоединения фосфора (III) не было. [ 61 ] [ 62 ] Несмотря на существование PCl 5 , псевдогалогенидный аналог P(N 3 ) 5 был описан, но еще не подтвержден. [ 61 ] [ 7 ] Азиды фосфора (V) ограничены их ионными солями и могут быть получены либо в виде антимонатной соли [P(N 3 ) 4 ] + [SbCl 6 ] - из PCl 3 или натриевой соли Na[P(N 3 ) 6 ] из PCl 5 . [ 7 ] [ 63 ]
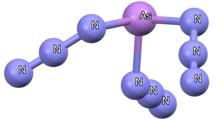

As(N 3 ) 3 может быть получен путем фторидного обмена, и полученная кристаллическая структура имеет мостиковые ЭО двух азидогрупп, что дает координационное число 7 и бесконечную зигзагообразную цепную структуру. [ 64 ] Однако состояние решения 14 N-ЯМР As(N 3 ) 3 подтверждает, что эти соединения фактически являются мономерами в растворе, а неподеленная пара мышьяка рассчитана как стерически активная, о чем свидетельствуют оптимизированная геометрия газовой фазы и контурный график общей электронной плотности. [ 64 ] [ 65 ] В отличие от фосфора, исходный азид мышьяка(V) выделен в виде As(N 3 ) 5 и существует в виде желтой жидкости. [ 66 ] Сообщается о всей серии азидо-ионов мышьяка [As(N 3 ) 4 ] - , [As(N 3 ) 4 ] + и [As(N 3 ) 6 ] - . [ 65 ] [ 67 ] Катионные соединения имеют самые короткие расстояния As-N и N β -N γ, тогда как анионные соединения, как правило, имеют гораздо более длинные расстояния As-N, что частично объясняет, почему катионные соединения имеют тенденцию быть гораздо более взрывоопасными. [ 67 ]
Азид сурьмы(III) Sb(N 3 ) 3 получают аналогично азиду мышьяка и имеют аналогичную структуру, за исключением того, что все три азидо-лиганда участвуют в образовании мостиков ЭО и образуют высокосимметричный лист. [ 64 ] Sb(N 5 ) 5 существует как очень нестабильное соединение, и с ним нельзя обращаться без взрыва при температуре окружающей среды. [ 66 ] Ряд солей азида сурьмы [Sb(N 3 ) 4 ] - , [Sb(N 3 ) 4 ] + , и [Sb(N 3 ) 6 ] - известны и имеют схожие тенденции с мышьяковыми. [ 67 ]
Бинарные азиды висмута оставались неуловимыми до 2010 года, когда чистый Bi(N 3 ) 3 был выделен с использованием пути фторидного обмена. [ 68 ] Ряд ионов висмута (III) [Bi(N 3 ) 4 ] - , [Би(N 3 ) 5 ] 2- и [ N3 ) ( Би 3- были синтезированы и структурно охарактеризованы. [ 68 ] [ 69 ] Неподеленная пара висмута стерически активна во всех ионах. [ 69 ] В твердом состоянии структуры висмута, как правило, сильно отличаются от своих более легких аналогов из группы 15, поскольку висмут может иметь большие координационные числа, а структуры основаны на параллелограмме Bi 2 N 2 с координационным числом 8. Попытки создания Bi(V) соединения приводят к восстановлению до Bi(III) N 3 - . [ 69 ]
Группа 16
[ редактировать ]диазид кислорода O(N 3 ) 2 Предполагается, что является промежуточным продуктом образования циклического закиси азота N 2 O из OF 2 и NaN 3 , но его существование пока не подтверждено. [ 70 ] Исходные азиды серы S(N 3 ) 2 или S(N 3 ) 4 не синтезированы и изучены лишь теоретические расчеты их существования. [ 71 ] Хотя сульфурилазид SO 2 (N 3 ) 2 известен и полностью охарактеризован. [ 72 ]
Ряд бинарных азидов селена Se(N 3 ) 4 , [Se(N 3 ) 5 ] - и [Se(N 3 ) 6 ] 2- были получены путем обмена фторида. [ 73 ] Нейтральный Se(N 3 ) 4 относительно нестабилен и может без всякой причины детонировать даже при -64°С под действием SO 2 . Таким образом, характеристика твердого состояния ограничивается ионами и показывает, что азидогруппы имеют сильный ковалентный характер. [Se(N 3 ) 6 ] 2- ион кристаллизуется с идеальной симметрией S6 , и поэтому неподеленная пара не считается стерически активной.
Азиды теллура (IV) [Te(N 3 ) 3 ] + , Те(N 3 ) 4 , [Те(N 3 ) 5 ] - , и [Te(N 3 ) 6 ] 2- обычно получают восстановлением фторида теллура (VI) TeF 6 по пути фторидного обмена. [ 74 ] [ 75 ] Неудивительно, что Te(N 3 ) 4 является очень чувствительным соединением, а его соли гораздо менее чувствительны к ударам. В отличие от указанной выше соли селена, неподеленная пара в дианионе теллура [Te(N 3 ) 6 ] 2- стерически активен и, следовательно, вызывает искаженную псевдопентагональную бипирамидальную структуру.
Группа 17
[ редактировать ]четыре азидогалогенида FN 3 , ClN 3 , BrN 3 и IN 3 содержат чисто ковалентные азид-галогенидные связи, что делает их чрезвычайно чувствительными. Все [ 1 ] Газофазная реакция между F 2 и HN 3 приводит к образованию FN 3 , но F 2 необходимо разбавлять инертным газом и следует избегать быстрого смешивания, чтобы F 2 N 2 . не образовывался [ 76 ] [ 77 ] Азид хлора также является газом и может быть получен путем барботирования разбавленного газообразного хлора через раствор NaN 3 . [ 78 ] Однако азид хлора имеет тенденцию самопроизвольно взрываться даже при пониженных температурах. Азид брома — жидкость, но он не менее коварен. [ 78 ] Используемый NaN 3 должен быть сухим, поскольку BrN 3 гидролизуется в воде. Аналогично, азид йода чувствителен к влаге и может быть получен из ICl и AgN 3 в твердом виде. [ 79 ] Однако, поскольку с AgN 3 можно безопасно обращаться только во влажном состоянии, к реакционной смеси обычно добавляют осушающий агент, чтобы предотвратить гидролиз конечного продукта. И BrN 3 , и IN 3 находят применение в синтезе как удобный способ получения азидиридинов и азиринов. [ 80 ] Азиды хлора, брома и йода охарактеризованы в твердом состоянии. [ 81 ] Азид хлора имеет сильные взаимодействия Cl-Cl и сравним с расположением «елочкой» других галогенных структур. Напротив, азиды брома и йода предпочитают межмолекулярные взаимодействия XN, образуя спиральную структуру для BrN 3 и плоские цепи для IN 3 .
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж Гарри Дэвид Фэйр; Раймонд Ф. Уокер, ред. (1977). Физика и химия неорганических азидов . Нью-Йорк: Пленум Пресс. ISBN 0-306-37076-Х . ОСЛК 2985662 .
- ^ Jump up to: а б с Рибас, Джон; Эскуэр, Альберт; Монфор, Монтсеррат; Висенте, Рамон; Кортес, Роберто; Лезама, Луис; Рохо, Теофило (1 октября 1999 г.). «Полиядерные азидо-мостиковые комплексы NiII и MnII. Структурные тенденции и магнитное поведение» . Обзоры координационной химии . 193–195: 1027–1068. дои : 10.1016/S0010-8545(99)00051-X . ISSN 0010-8545 .
- ^ Jump up to: а б с д и ж Хейгес, Ральф; Боатц, Джерри А.; Кристе, Карл О. (18 октября 2010 г.). «Синтез и структура бинарных азидов ванадия (IV) и ванадия (V) V(N3)4, [V(N3)6]2- и [V(N3)6]-» . Angewandte Chemie, международное издание . 49 (43): 8008–8012. дои : 10.1002/anie.200906537 . ПМИД 20715219 .
- ^ Jump up to: а б с д и Хейгес, Ральф; Боатц, Джерри А.; Уильямс, Джоди М.; Кристе, Карл О. (12 сентября 2011 г.). «Получение и характеристика азидов бинарной группы 13 M(N3)3 и M(N3)3⋅CH3CN (M=Ga, In, Tl), [Ga(N3)5]2- и [M(N3)6». ]3− (M=In, Tl)" . Angewandte Chemie, международное издание . 50 (38): 8828–8833. дои : 10.1002/anie.201103101 . ПМИД 21766406 .
- ^ Jump up to: а б Уайт, Эндрю Д. (15 апреля 2001 г.), «Азид железа (III)» , Энциклопедия реагентов для органического синтеза , Чичестер, Великобритания: John Wiley & Sons, Ltd, номер документа : 10.1002/047084289x.ri053 , ISBN 0471936235 , получено 13 декабря 2022 г.
- ^ Чжоу, Цзин; Чжан, Цзюньлинь; Ван, Бочжоу; Цю, Лили; Сюй, Руцянь; Шереметьев, Алексей Б. (2022). «Недавние синтетические усилия по созданию материалов с высокой плотностью энергии: как создавать высокоэффективные энергетические структуры?» . ОгоньФизХим . 2 (2): 83–139. Бибкод : 2022ФФЧ...2...83З . дои : 10.1016/j.fpc.2021.09.005 . S2CID 244214466 .
- ^ Jump up to: а б с д и Портиус, Питер; Дэвис, Мартин (01 марта 2013 г.). «Новейшие достижения в химии гомолептических азидокомплексов элементов основной группы» . Обзоры координационной химии . Последние достижения в химии основной группы. 257 (5): 1011–1025. дои : 10.1016/j.ccr.2012.09.019 . ISSN 0010-8545 .
- ^ Jump up to: а б Саал, Томас; Деокар, Пиюш; Кристе, Карл О.; Хейгес, Ральф (15 мая 2019 г.). «Бинарные аддукты азида группы 4 [(bpy)Ti(N 3 ) 4 ], [(phen)Ti(N 3 ) 4 ], [(bpy) 2 Zr(N 3 ) 4 ] 2 ·bpy и [( бpy) 2 Hf(N 3 ) 4 ] 2 ·bpy" . Европейский журнал неорганической химии . 2019 (18): 2388–2391. дои : 10.1002/ejic.201900334 . ISSN 1434-1948 . S2CID 132294068 .
- ^ Томас Г. Мюллер; Фридрих Карау; Вольфганг Шник; Флориан Краус. Новый путь к азидам металлов. Международное издание прикладной химии. 2014. два : 10.1002/anie.201404561
- ^ Кати Розенстенгель, Аксель Шульц, Оливер Нихаус, Оливер Янка, Райнер Петтген, Александр Виллингер. Бинарные полиазиды церия и гадолиния. Европейский журнал неорганической химии. 2017. два : 10.1002/ejic.201701408 .
- ^ Jump up to: а б с Ли, Цянь Шу; Дуань, Хун Ся (01 октября 2005 г.). «Теоретическое исследование функционала плотности ряда бинарных азидов M(N 3 ) n ( n = 3, 4)» . Журнал физической химии А. 109 (40): 9089–9094. Бибкод : 2005JPCA..109.9089L . дои : 10.1021/jp052726t . ISSN 1089-5639 . ПМИД 16332016 .
- ^ Jump up to: а б с Хейгес, Ральф; Боатц, Джерри А.; Шнайдер, Стефан; Шрёр, Торстен; Юсуфуддин, Мухаммед; Кристе, Карл О. (14 июня 2004 г.). «Бинарные азиды 4-й группы [Ti(N3)4], [P(C6H5)4][Ti(N3)5] и [P(C6H5)4]2[Ti(N3)6] и на линейном Ti NNN Координация» . Angewandte Chemie, международное издание . 43 (24): 3148–3152. дои : 10.1002/anie.200454156 . ISSN 1433-7851 . ПМИД 15199563 .
- ^ Деокар, Пиюш; Василиу, Моника; Диксон, Дэвид А.; Кристе, Карл О.; Хейгес, Ральф (07 ноября 2016 г.). «Бинарные азиды 4-й группы [PPh 4 ] 2 [Zr(N 3 ) 6 ] и [PPh 4 ] 2 [Hf(N 3 ) 6 ]» . Angewandte Chemie, международное издание . 55 (46): 14350–14354. дои : 10.1002/anie.201609195 . ПМИД 27735115 .
- ^ Гутманн, В.; Лейтманн, О.; Шерхауфер, А.; Чуба, Х. (1 января 1967 г.). «Азидокомплексы в неводных растворителях, 3-е соединение: Ti(III), V(III) и Cr(III) в ацетонитриле, пропандиол-1,2-карбонате и триметилфосфате» . Ежемесячные журналы по химии и смежным разделам других наук (на немецком языке). 98 (1): 188–199. дои : 10.1007/BF00901117 . ISSN 1434-4475 .
- ^ Jump up to: а б с Хейгес, Ральф; Боатц, Джерри А.; Шрёр, Торстен; Юсуфуддин, Мухаммед; Кристе, Карл О. (17 июля 2006 г.). «Экспериментальные доказательства линейной координации металла и азидо: бинарные азиды 5-й группы [Nb(N3)5], [Ta(N3)5], [Nb(N3)6]- и [Ta(N3)6]-, и ацетонитриловые аддукты 1:1 [Nb(N3)5(CH3CN)] и [Ta(N3)5(CH3CN)]" . Angewandte Chemie, международное издание . 45 (29): 4830–4835. дои : 10.1002/anie.200601060 . ISSN 1433-7851 . ПМИД 16795097 .
- ^ Jump up to: а б Хейгес, Ральф; Боатц, Джерри А.; Юсуфуддин, Мухаммед; Кристе, Карл О. (13 апреля 2007 г.). «Монокапированные тригонально-призматические гептаазиды переходных металлов: синтез, свойства и структуры [Nb(N3)7]2- и [Ta(N3)7]2-» . Angewandte Chemie, международное издание . 46 (16): 2869–2874. дои : 10.1002/anie.200604520 . ПМИД 17348060 .
- ^ Хейгес, Ральф; Деокар, Пиюш; Кристе, Карл О. (19 мая 2014 г.). «Координационные аддукты азидов ниобия(V) и тантала(V) M(N 3 ) 5 (M=Nb, Ta) с лигандами-донорами азота и их самоионизация» . Angewandte Chemie, международное издание . 53 (21): 5431–5434. дои : 10.1002/anie.201402775 . ПМИД 24756882 .
- ^ Хейгес, Ральф; Боатц, Джерри А.; Бау, Роберт; Шнайдер, Стефан; Шрёр, Торстен; Юсуфуддин, Мухаммед; Кристе, Карл О. (11 марта 2005 г.). «Химия полиазидов: первые азиды бинарной группы 6, Mo(N3)6, W(N3)6, [Mo(N3)7]? и [W(N3)7]?, а также [NW(N3)4 ] и ионы [NMo(N3)4] ? Angewandte Chemie, международное издание . 44 (12): 1860–1865. дои : 10.1002/anie.200462740 . ISSN 1433-7851 . ПМИД 15723363 .
- ^ Денике, К.; Дубген, Р. (1978). «Реакции азида йода с карбонилами металлов» . Журнал неорганической и общей химии (на немецком языке). 444 (1): 61–70. дои : 10.1002/zaac.19784440106 . ISSN 0044-2313 .
- ^ Jump up to: а б Гохер, Мохамед А.С.; Кано, Джоан; Журно, Ив; Абу-Юсеф, Морси А.М.; Маутнер, Франц А.; Эскуэр, Альберт; Висенте, Рамон (3 марта 2000 г.). «Синтез, структурная характеристика и моделирование методом Монте-Карло магнитных свойств трехмерных сложенных сот Csn[{Mn(N3)3}n] и нерегулярной двойной цепи [{N(C2H5)4}n][{Mn2( N3)5(H2O)}n]" . Химия - Европейский журнал . 6 (5): 778–784. doi : 10.1002/(SICI)1521-3765(20000303)6:5<778::AID-CHEM778>3.0.CO;2-P . ISSN 0947-6539 . ПМИД 10826599 .
- ^ Кортес, Роберто; Лезама, Луис; Красный, Теофил; Арриортуа, М. Изабель; Писарро, Дж. Луис; Соланс, Ксавье (3 января 1995 г.). «Переменные ферро- и антиферромагнитные взаимодействия в цепи MnII с чередующимися сквозными и сквозными мостиковыми азидо-лигандами» . Angewandte Chemie International Edition на английском языке . 33 (2324): 2488–2489. дои : 10.1002/anie.199424881 . ISSN 0570-0833 .
- ^ Jump up to: а б с Маутнер, Франц А.; Ханна, Сэми; Вежливый, Роберт; Лезама, Луи; Перила, М. Готцоне; Красный, Теофил (1 октября 1999 г.). «Кристаллическая структура, спектроскопические и магнитные свойства систем азидо-тетраметиламмония марганца (II) и меди (II)» . Неорганическая химия . 38 (21): 4647–4652. дои : 10.1021/ic981373s . ISSN 0020-1669 . ПМИД 11671186 .
- ^ Ма, Ю; Ченг, Ай-Линг; Сунь, Вэй-Вэй; Чжан, Цзян-Юн; Гао, Энь-Цин (1 мая 2009 г.). «Гомолептический слой марганца (II) – азид: синтез, структурная характеристика и магнитные свойства» . Неорганическая химия . 12 (5): 412–416. дои : 10.1016/j.inoche.2009.03.005 . ISSN 1387-7003 .
- ^ Штайнер, Клаус; Желаю, Вольфганг; Мюллер, Ульрих; Денике, Курт (1987). «Азидокомплексы марганца(II) и кобальта(II). Кристаллические структуры (PPh4)2[Mn(N3)4] и (PPh4)2[Co(N3)3Cl]» . Журнал неорганической и общей химии (на немецком языке). 555 (12): 7–15. дои : 10.1002/zaac.19875551202 . ISSN 0044-2313 .
- ^ Маутнер, Франц А.; Кортес, Роберто; Лезама, Луис; Рохо, Теофило (19 января 1996 г.). «[N(CH3)4][Mn(N3)3]: соединение с искаженной структурой перовскита за счет азидо-лигандов» . Angewandte Chemie International Edition на английском языке . 35 (1): 78–80. дои : 10.1002/anie.199600781 . ISSN 0570-0833 .
- ^ Хейгес, Ральф; Бушек, Роберт Дж.; Боатц, Джерри А.; Кристе, Карл О. (28 июля 2014 г.). «Получение первых азидов марганца(III) и марганца(IV)» . Angewandte Chemie, международное издание . 53 (31): 8200–8205. дои : 10.1002/anie.201404735 . ПМИД 25044947 .
- ^ Jump up to: а б Бек, Вольфганг; Фельхаммер, Вольф Питер; Пёлльманн, Питер; Шуйерер, Эрих; Фельдл, Клаус (1967). «Изображение, ИК и электронные спектры азидо-металлокомплексов» . Химические отчеты . 100 (7): 2335–2361. дои : 10.1002/cber.19671000731 . ISSN 0009-2940 .
- ^ Драммонд, Дж.; Вуд, Дж. С. (1969). «Строение пятикоординационного комплекса железа: иона пентаазидо железа(III) Fe(N3)5 2?» . Журнал Химического общества D: Chemical Communications (23): 1373. doi : 10.1039/c29690001373 . ISSN 0577-6171 .
- ^ СУЗУКИ, Акира; ИШИДОЯ, Масахиро; ТАБАТА, Масаеши (1976). «Реакция органоборанов с азидом железа (III) в присутствии перекиси водорода. Новый синтез азидоалканов из алкенов методом гидроборирования» . Синтез . 1976 (10): 687–689. дои : 10.1055/s-1976-24160 . ISSN 0039-7881 .
- ^ Jump up to: а б с д Шмидтке, Ганс-Герберт; Гартхофф, Дитер. (1967). «Электронные спектры азидных комплексов некоторых благородных металлов» . Журнал Американского химического общества . 89 (6): 1317–1321. дои : 10.1021/ja00982a007 . ISSN 0002-7863 .
- ^ Сенизе, Пасчоаль (1959). «О реакции между кобальтом(II) и азид-ионами в водных и водно-органических растворах. 1 Американского Журнал химического общества . 81 (16): 4196–4199. doi : 10.1021/ja01525a020 . ISSN 0002-7863 .
- ^ Сенизе, Пасчоаль (1 сентября 1957 г.). «Точечный тест на сульфиты на основе индуцированного окисления растворов азида кобальта» . Микрохимика Акта . 45 (5): 640–643. дои : 10.1007/BF01236544 . ISSN 1436-5073 . S2CID 98339990 .
- ^ Суд, РК; Ня, А.Е.; Этим, ЕС (1981). «Термическое разложение азида никеля» . Журнал термического анализа . 22 (2): 231–237. дои : 10.1007/bf01915269 . ISSN 0022-5215 . S2CID 95478362 .
- ^ Jump up to: а б Бек, Вольфганг; Фельхаммер, Вольф Питер; Фельдл, Клаус; Клпотке, Томас М.; Крамер, Гернот; Майер, Питер; Пиотровский, Хольгер; Пёлльман, Питер; Пониквар, Уолтер; Шютт, Томас; Шуйерер, Эрих; Фогт, Мартин (2001). <1751::AID-ZAAC1751>3.0.CO;2-5" Кристаллические структуры (PPh3)2Pd(N3)2, (AsPh3)2Pd(N3)2, (2-Хлорпиридин)2Pd(N3)2, [( AsPh4)2][Pd2(N3)4Cl2], [(PNP)2][Pd(N3)4], [(AsPh4)2][Pt(N3)4] · 2H2O и [(AsPh4)2][Pt(N3)6]» . Журнал неорганической и общей химии . 627 (8): 1751–1758. doi : 10.1002/1521-3749(200108)627:8<1751::AID-ZAAC1751>3.0.CO;2-5 . ISSN 0044-2313 .
- ^ Ноймюллер, Бернхард; Шмок, Фритьоф; Плохо, Сабина; Денике, Курт (2000). <1792::AID-ZAAC1792>3.0.CO;2-U «Кристаллические структуры азидоплатинатов (AsPh4)2[Pt(N3)4] и (AsPh4)2[Pt(N3)6]» . Журнал неорганической и общей химии . 626 (8): 1792–1796. doi : 10.1002/1521-3749(200008)626:8<1792::AID-ZAAC1792>3.0.CO;2-U .
- ^ Вильсдорф, Х. (2 июля 1948 г.). «Кристаллическая структура одновалентного азида меди CuN3» . Acta Crystallographica (на немецком языке). 1 (3): 115–118. Бибкод : 1948AcCry...1..115W . дои : 10.1107/S0365110X48000314 . ISSN 0365-110X .
- ^ Гохер, Мохамед А.С.; Абду, Азза Э.Х.; Абу-Юсеф, Морси А.М.; Маутнер, Франц А. (1 февраля 2001 г.). «Бис-(тетраэтиламмоний)[тетраазидокупрат(II)] и катена-ди-μ-1,1-азидо-[ди-μ-1,1-азидо-бис-(2,4-диметилпиридин)димедь(II)] " . Химия переходных металлов . 26 (1): 39–43. дои : 10.1023/А:1007195015645 . ISSN 1572-901X . S2CID 92350747 .
- ^ Шмидт, Карстен Л.; Диннебье, Роберт; Ведиг, Ульрих; Янсен, Мартин (01 февраля 2007 г.). «Кристаллическая структура и химическая связь высокотемпературной фазы AgN 3» . Неорганическая химия . 46 (3): 907–916. дои : 10.1021/ic061963n . ISSN 0020-1669 . ПМИД 17257034 .
- ^ Шульц, Аксель; Виллингер, Александр (08 января 2016 г.). «Бинарные азиды цинка» . Химия - Европейский журнал . 22 (6): 2032–2038. дои : 10.1002/chem.201504524 . ISSN 0947-6539 . ПМИД 26749253 .
- ^ Нокеманн, Питер; Мейер, Герд (2002). <2709::aid-zaac2709>3.0.co;2-p «Образование NH4[Hg3(NH)2](NO3)3 и превращение в [Hg2N](NO3)» . Журнал неорганической и общей химии . 628 (12): 2709–2714. doi : 10.1002/1521-3749(200212)628:12<2709::aid-zaac2709>3.0.co;2-p . ISSN 0044-2313 .
- ^ Jump up to: а б Лунд, Хенрик; Оклер, Оливер; Шредер, Торстен; Шульц, Аксель; Виллингер, Александр (26 августа 2013 г.). «Азиды ртути и азид основания Миллона» . Международное издание «Прикладная химия» . 52 (41): 10900–10904. дои : 10.1002/anie.201305545 . ISSN 1433-7851 . ПМИД 24038779 .
- ^ Карау, Фридрих; Шник, Вольфганг (2005). «Внешний вид и кристаллическая структура азида кадмия Cd(N3)2» . Журнал неорганической и общей химии . 631 (12): 2315–2320. дои : 10.1002/zaac.200500226 . ISSN 0044-2313 .
- ^ Виберг, Эгон; Мишо, Хорст (1 июля 1954 г.). «Примечания: О знаниях о триазиде бора B(N 3 ) 3 » . Журнал естественных исследований Б. 9 (7): 497–499. дои : 10.1515/znb-1954-0715 . ISSN 1865-7117 . S2CID 96674767 .
- ^ Вагнер, Юджин Р. (1973). «Взаимодействие азида алюминия с цианоэфирами. Получение тетразоло[1,5-c]пиримидин-5(6H)-она и тетразоло[1,5-c]хиназолин-5(6H)-она» . Журнал органической химии . 38 (17): 2976–2981. дои : 10.1021/jo00957a012 . ISSN 0022-3263 .
- ^ Линнен, CJ; Макс, Делавэр; Кумб, РД (1 февраля 1997 г.). «Синтез Al(N 3 ) 3 и осаждение тонких пленок AlN» . Журнал физической химии Б. 101 (9): 1602–1608. дои : 10.1021/jp9625873 . ISSN 1520-6106 .
- ^ Jump up to: а б с Суссек, Харальд; Стоуассер, Фрэнк; Прицков, Ганс; Фишер, Роланд А. (2000). <455::aid-ejic455>3.0.co;2-e «Тетраазидокомплексы алюминия, галлия и индия» . Европейский журнал неорганической химии . 2000 (3): 455–461. doi : 10.1002/(sici)1099-0682(199903)2000:3<455::aid-ejic455>3.0.co;2-e . ISSN 1434-1948 .
- ^ Фрэнк, Алисса С.; Стоуассер, Фрэнк; Суссек, Харальд; Прицков, Ганс; Мискис, Клаудио Р.; Амбахер, Оливер; Гирсиг, Майкл; Фишер, Роланд А. (1998). «Детонация азидов галлия: простой путь к гексагональным нанокристаллам GaN» . Журнал Американского химического общества . 120 (14): 3512–3513. дои : 10.1021/ja9738438 .
- ^ Фишер, Рональд А.; Мьер, Александр; Хердтвек, Эберхардт; Мэттнер, Майкл Р.; Амбахер, Оливер; Мецгер, Томас; Борн, Эберхард; Вайнкауф, Севиль; Пулхэм, Колин Р.; Парсонс, Саймон (1996). «Триазидогаллий и его производные: новые предшественники тонких пленок и наночастиц GaN» . Химия – Европейский журнал . 2 (11): 1353–1358. дои : 10.1002/chem.19960021104 .
- ^ Вёлер, Лотар; Мартин, Ф (1917). «Чувствительность азидов» . Прикладная химия . 30 (9): 33–39. Бибкод : 1917АнгЧ..30...33Вт . дои : 10.1002/anie.19170300902 .
- ^ Хасснер, Альфред; Стерн, Меир; Готлиб, Хьюго Э.; Фролоу, Феликс (1990). «Синтетические методы. 33. Применение полимерного азидного реагента в образовании ди- и триазидометана. Их ЯМР-спектры и рентгеновская структура производных триазолов» . Журнал органической химии . 55 (8): 2304–2306. дои : 10.1021/jo00295a014 . ISSN 0022-3263 .
- ^ Банерт, Клаус; Джу, Ён Хёк; Рюффер, Тобиас; Уолфорт, Бернхард; Ланг, Генрих (2007). «Захватывающая химия тетраазидометана» . Angewandte Chemie, международное издание . 46 (7): 1168–1171. дои : 10.1002/anie.200603960 . ПМИД 17143916 .
- ^ Виберг, Эгон; Мишо, Хорст (1 июля 1954 г.). «Примечания: К сведениям о тетразиде кремния Si(N 3 ) 4 » . Журнал естественных исследований Б. 9 (7): 500. doi : 10.1515/znb-1954-0717 . ISSN 1865-7117 . S2CID 98275613 .
- ^ Филиппу, Александр К.; Портиус, Питер; Шнакенбург, Грегор (14 января 2003 г.). «Ион гексаазидосиликата (IV): синтез, свойства и молекулярная структура» . ХимИнформ . 34 (2). дои : 10.1002/chin.200302019 . ISSN 0931-7597 .
- ^ Дрейк, Дж. Э.; Хеммингс, RT (15 января 1973 г.). «Получение и характеристика псевдогалоген(метил)германов и родственных соединений» . Канадский химический журнал . 51 (2): 302–311. дои : 10.1139/v73-043 . ISSN 0008-4042 .
- ^ Филиппу, Александр К.; Портиус, Питер; Нойманн, Дирк У.; Верстедт, Клаус-Дитер (1 декабря 2000 г.). <4333::aid-anie4333>3.0.co;2-s «Ион гексаазидогерманата(IV): синтезы, структуры и реакции» . Ангеванде Хеми . 39 (23): 4333–4336. Бибкод : 2000AngCh..39.4333F . doi : 10.1002/1521-3773(20001201)39:23<4333::aid-anie4333>3.0.co;2-s . ISSN 1433-7851 . ПМИД 29711897 .
- ^ Jump up to: а б Бесподобный, Бенджамин; Кин, Тео; Мейер, Энтони Дж.Х.М.; Портиус, Питер (2015). «Гомолептичные низковалентные полиазиды элементов 14 группы» . Химические коммуникации . 51 (35): 7435–7438. дои : 10.1039/c5cc00259a . ISSN 1359-7345 . ПМИД 25773494 . S2CID 32981384 .
- ^ Кэмпбелл, Рори; Дэвис, Мартин Ф.; Фазакерли, Мэтью; Портиус, Питер (13 ноября 2015 г.). «Укрощение полиазидов олова (IV)» . Химия - Европейский журнал . 21 (51): 18690–18698. дои : 10.1002/chem.201503478 . ISSN 0947-6539 . ПМИД 26767331 .
- ^ Виберг, Эгон; Мишо, Хорст (1 июля 1954 г.). «Примечания: К сведениям о гексазидостаннате натрия Na 2 Sn(N 3 ) 6 » . Журнал естественных исследований Б. 9 (7): 500–501. дои : 10.1515/znb-1954-0718 . ISSN 1865-7117 . S2CID 94917667 .
- ^ Мёллер, Хайнц (1949). «Попытки получения соединений азида свинца (IV)» . Журнал неорганической химии . 260 (4–5): 249–254. дои : 10.1002/zaac.19492600406 . ISSN 0372-7874 .
- ^ Фельхаммер, Вольф Питер; Бек, Вольфганг (2013). «Азидная химия - неорганический взгляд, часть 1 Азиды металлов: обзор, общие тенденции и последние разработки» . Журнал неорганической и общей химии . 639 (7): 1053–1082. дои : 10.1002/zaac.201300162 .
- ^ Jump up to: а б Будер, Вольфганг; Шмидт, Армин (1975). «Фосфоразиды и их колебательные спектры» . Химическая информационная служба . 415 (3): 263–267. дои : 10.1002/chin.197534036 .
- ^ Шульц, Аксель; Виллингер, Александр (5 марта 2012 г.). «Бинарные азиды пниктогена - экспериментальное и теоретическое исследование: [As(N 3 ) 4 ] - , [Sb (N 3 ) 4 ] - и [Bi (N 3 ) 5 (dmso)] 2-» . Химия - Европейский журнал . 18 (10): 2902–2911. дои : 10.1002/chem.201102656 . ПМИД 22337137 .
- ^ Шмидт, Армин (1970). «Представление и ИК-спектры гексахлорантимонатов диметилдиазидо, метилтриазидо и тетраазидофосфония (V)» . Химические отчеты . 103 (12): 3923–3927. дои : 10.1002/cber.19701031223 . ISSN 0009-2940 .
- ^ Jump up to: а б с Хейгес, Ральф; Видж, Ашвани; Боатц, Джерри А.; Шнайдер, Стефан; Шрёр, Торстен; Геркен, Майкл; Кристе, Карл О. (23 января 2004 г.). «Первая структурная характеристика бинарных азидов AsIII и SbIII» . Химия - Европейский журнал . 10 (2): 508–517. дои : 10.1002/chem.200305482 . ISSN 0947-6539 . ПМИД 14735519 .
- ^ Jump up to: а б Гейсслер, Петра; Клапотке, Томас М.; Крот, Хайнц-Юрген (1 июня 1995 г.). «Спектры ЯМР 14N ковалентных галогенов и азидов мышьяка: XN3 (X Cl, Br, I), (CH3)nAs(N3)3−n (n = 0, 1, 2) и [As(N3)4]+ " . Spectrochimica Acta Часть A: Молекулярная и биомолекулярная спектроскопия . 51 (6): 1075–1078. дои : 10.1016/0584-8539(94)01313-6 . ISSN 1386-1425 .
- ^ Jump up to: а б Хейгес, Ральф; Боатц, Джерри А.; Видж, Ашвани; Видж, Вандана; Геркен, Майкл; Шнайдер, Стефан; Шрёр, Торстен; Юсуфуддин, Мухаммед; Кристе, Карл О. (10 декабря 2004 г.). «Химия полиазидов: получение и характеристика As(N3)5, Sb(N3)5 и [P(C6H5)4][Sb(N3)6]» . Angewandte Chemie, международное издание . 43 (48): 6676–6680. дои : 10.1002/anie.200461730 . ISSN 1433-7851 . ПМИД 15593158 .
- ^ Jump up to: а б с Карагиосов, Константин; Клапотке, Томас М.; Крумм, Буркхард; Нёт, Генрих; Шютт, Томас; Сутер, Макс (1 января 2002 г.). «Экспериментальная и теоретическая характеристика катионных, нейтральных и анионных бинарных видов азида мышьяка и сурьмы» . Неорганическая химия . 41 (2): 170–179. дои : 10.1021/ic010463l . ISSN 0020-1669 . ПМИД 11800605 .
- ^ Jump up to: а б Виллингер, Александр; Шульц, Аксель (18 октября 2010 г.). «Бинарные азиды висмута (III): Bi(N3)3, [Bi(N3)4]- и [Bi(N3)6]3-» . Angewandte Chemie, международное издание . 49 (43): 8017–8020. дои : 10.1002/anie.201002179 . ПМИД 20839195 .
- ^ Jump up to: а б с Хейгес, Ральф; Рам, Мартин; Диксон, Дэвид А.; Гарнер, Эдвард Б.; Кристе, Карл О. (16 января 2012 г.). «Бинарные полиазиды группы 15. Структурная характеристика [Bi(N 3 ) 4 ] - , [Bi(N 3 ) 5 ] 2– , [bipy·Bi(N 3 ) 5 ] 2– , [Bi(N 3 ) 6 ] 3– , bipy·As(N 3 ) 3 , bipy·Sb(N 3 ) 3 , и [(bipy) 2 ·Bi(N 3 ) 3 ] 2 и об активации неподеленной пары валентных электронов» . Неорганическая химия . 51 (2): 1127–1141. дои : 10.1021/ic202307a . ISSN 0020-1669 . ПМИД 22221015 .
- ^ Кроуфорд, Маргарет-Джейн; Клапотке, Томас М. (1 июня 1999 г.). «Возможное промежуточное образование циклической закиси азота N 2 O: реакция дифторида кислорода OF 2 с азидом цезия CsN 3» . Неорганическая химия . 38 (12): 3006–3009. дои : 10.1021/ic990240j . ISSN 0020-1669 . ПМИД 11671052 .
- ^ Ван, Ли Цзе; Згерский, Марек З.; Мезей, Пол Г. (1 марта 2003 г.). «Стабильные структуры богатых азотом сульфидов: S(N 3 ) m (m = 1-4)» . Журнал физической химии А. 107 (12): 2080–2084. Бибкод : 2003JPCA..107.2080W . дои : 10.1021/jp022074y . ISSN 1089-5639 .
- ^ Цзэн, Сяоцин; Беккерс, Хельмут; Бернхардт, Эдуард; Виллнер, Хельге (5 сентября 2011 г.). «Синтез и характеристика сульфурилдиазида O 2 S(N 3 ) 2» . Неорганическая химия . 50 (17): 8679–8684. дои : 10.1021/ic201294b . ISSN 0020-1669 . ПМИД 21815651 .
- ^ Клапотке, Томас М.; Крумм, Буркхард; Шерр, Матиас; Хейгес, Ральф; Кристе, Карл О. (19 ноября 2007 г.). «Бинарные азиды селена (IV) Se(N 3 ) 4 , [Se(N 3 ) 5 ] - и [Se(N 3 ) 6 ] 2-» . Международное издание «Прикладная химия» . 46 (45): 8686–8690. дои : 10.1002/anie.200702758 . ПМИД 17935101 .
- ^ Джонсон, Джеймс П.; Маклин, Грегори К.; Пассмор, Джек; Уайт, Питер С. (1 ноября 1989 г.). «Получение и рентгенокристаллическая структура Te(N 3 ) 3 SbF 6 , содержащего катион триазидотеллура(IV), Te(N 3 ) 3 +» . Канадский химический журнал . 67 (11): 1687–1692. дои : 10.1139/v89-259 . ISSN 0008-4042 .
- ^ Хейгес, Ральф; Боатц, Джерри А.; Видж, Ашвани; Геркен, Майкл; Шнайдер, Стефан; Шрёр, Торстен; Кристе, Карл О. (8 декабря 2003 г.). «Химия полиазидов: получение и характеристика Te(N3)4 и [P(C6H5)4]2[Te(N3)6] и доказательства существования [N(CH3)4][Te(N3)5]» . Angewandte Chemie, международное издание . 42 (47): 5847–5851. дои : 10.1002/anie.200352680 . ISSN 1433-7851 . ПМИД 14673915 .
- ^ Бауэр, С.Х. (1947). «Электронографическое исследование структуры дифтордиазина» . Журнал Американского химического общества . 69 (12): 3104–3108. дои : 10.1021/ja01204a053 . ISSN 0002-7863 .
- ^ Миллиган, Дольфус Э.; Джакокс, Мэрилин Э. (1964). «Инфракрасные спектры NF, NCl и NBr» . Журнал химической физики . 40 (9): 2461–2466. Бибкод : 1964ЖЧФ..40.2461М . дои : 10.1063/1.1725547 . ISSN 0021-9606 .
- ^ Jump up to: а б Денике, К. (1967). «Реакции галогеназидов» . Angewandte Chemie International Edition на английском языке . 6 (3): 240–246. дои : 10.1002/anie.196702401 . ISSN 0570-0833 .
- ^ Денике, Курт (1979). «Химия азида йода» . Angewandte Chemie International Edition на английском языке . 18 (7): 507–514. дои : 10.1002/anie.197905071 . ISSN 0570-0833 .
- ^ Хасснер, Альфред; Маринеску, Лавиния; Болс, Микаэль (15 октября 2005 г.), «Азид йода» , в John Wiley & Sons, Ltd. (редактор), Энциклопедия реагентов для органического синтеза , Чичестер: John Wiley & Sons, Ltd, стр. ri007, doi : 10.1002/047084289x.ri007 , ISBN 978-0-471-93623-7 , получено 13 декабря 2022 г.
- ^ Лихс, Бенджамин; Блязер, Дитер; Вёльпер, Кристоф; Шульц, Стефан; Янсен, Георг (14 декабря 2012 г.). «Сравнение твердотельных структур галогеназидов XN 3 (X = Cl, Br, I)» . Международное издание «Прикладная химия» . 51 (51): 12859–12863. дои : 10.1002/anie.201206028 . ПМИД 23143850 .