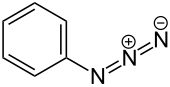
Фенил азид
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC
Они не делают [ 1 ] | |||
| Другие имена
Фенил азид [ 1 ]
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| Chemspider | |||
| Echa Infocard | 100.009.756 | ||
| ЕС номер |
| ||
| Сетка | C014747 | ||
PubChem CID
|
|||
| НЕКОТОРЫЙ | |||
Comptox Dashboard ( EPA )
|
|||
| Характеристики | |||
| C 6 H 5 N 3 | |||
| Молярная масса | 119.127 g·mol −1 | ||
| Появление | Бледно -желтая жидкость | ||
| Точка кипения | От 49 до 50 ° C (от 120 до 122 ° F; от 322 до 323 К) при 5 мм рт. | ||
| не заметно | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности
|
взрывчатка | ||
| Связанные соединения | |||
Связанные соединения
|
Анилин Нитробензол Нитрособензол Фенилгидразин Фенилгидроксиламин Диазоний катион | ||
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |||
Фенил азид - это органическое соединение с формулой C 6 H 5 N 3 . Это один из прототипических органических азидов. Это бледно -желтая масляная жидкость с острым запахом. Структура состоит из линейного азидного заместителя, связанного с фенильной группой. Угол C - N = N составляет приблизительно 120 °. Это было обнаружено в 1864 году Питером Гриессом реакцией аммиака и фенилдиазония . [ 2 ] [ 3 ]
Подготовка
[ редактировать ]готовятся диазотизацией фенилгидразина с Фенил азид азотной кислотой : [ 4 ]
- C 6 H 5 NHNH 2 + HNO 2 → C 6 H 5 N 3 + 2 H 2 O
Арил йодиды, несущие заместители с электронами, подвергаются метатезису азида натрия в присутствии Cu (I), аскорбате натрия и N, N'-диметилтана-1,2-диамина (DMEDA): [ 5 ]
- RC 6 H 4 I + NAN 3 → RC 6 H 4 N 3 + NAI
Он также может быть приготовлен путем конденсации бензондиазония соли толуэенсульфонамидом с последующим гидролизом.
Химические реакции
[ редактировать ]Фенил азид циклических циклов до алкенов и особенно алкинов , особенно тех, которые имеют электроотрицательные заместители. В классическом примере химии щелчка фенил азид и фенилацетилен реагируют с получением дифенилового триазола .
Фенил азид реагирует с трифенилфосфином с обращением реагента Staudinger трифенилфосфин фенилимид (C 6 H 5 NP (C 6 H 5 ) 3 ).
Термолиз индуцирует потерю N 2, чтобы получить высокореактивный фенилнитрон C 6 H 5 N. [ 6 ]
Безопасность
[ редактировать ]Как и во многих других азидах, фенил азид представляет риск взрыва, [ 4 ] Таким образом, защитный взрывной щит рекомендуется во время очистки и обработки. Дистилляции опасны. Органические синтезы рекомендуют вакуум 5 мм рт. [ 4 ] Чистое вещество может храниться в темноте, холодном, и даже тогда срок годности составляет всего недели.
Ссылки
[ редактировать ]- ^ Jump up to: а беременный Номенклатура органической химии: рекомендации IUPAC и предпочтительные названия 2013 (Blue Book) . Кембридж: Королевское химическое общество . 2014. С. 66, 1119. DOI : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Грисс, Джон Петр; Хофманн, Август Вильгельм фон (1864-01-01). «XX. На новом классе соединений, в котором азот заменяется водородом» . Труды Королевского общества Лондона . 13 : 375–384. doi : 10.1098/rspl.1863.0082 . S2CID 94746575 .
- ^ Грисс, Петр (1866). «О новом классе органических соединений, в котором водород представлен азотом» . Анналы химии и фармации (на немецком языке). 137 (1): 39–91. Doi : 10.1002/jlac.18661370105 .
- ^ Jump up to: а беременный в Ро Линдсей и КФХ Аллен (1942). "Фенил азид". Органические синтезы . 22 : 96. doi : 10.15227/orgsyn.022.0096 .
- ^ Андерсен, Джейкоб; Мэдсен, Ульф; Бьорклинг, Фредрик; Лян, Xifu (2005). «Быстрый синтез арил азидов из арилгалогенидов в мягких условиях» . Синлетт 2005 (14): 2209–2213. doi : 10.1055/s-2005-872248 . ISSN 0936-5214 .
- ^ WH Pearson, PS Ramamoorthyin "фенил азид" Энциклопедия реагентов для органического синтеза (Ed: L. Paquette) 2004, J. Wiley & Sons, Нью -Йорк. doi : 10.1002/047084289x .

