Водная модель

В вычислительной химии модель воды используется для моделирования и термодинамического расчета кластеров воды , жидкой воды и водных растворов с явным растворителем. Модели определяются на основе квантовой механики , молекулярной механики , экспериментальных результатов и этих комбинаций. Для имитации специфической природы молекул было разработано множество типов моделей. В целом их можно классифицировать по следующим трем пунктам; (i) количество точек взаимодействия, называемых сайтом , (ii) является ли модель жесткой или гибкой, (iii) включает ли модель поляризации эффекты .
Альтернативой явным моделям воды является использование модели неявной сольватации , также называемой моделью континуума, примером которой может быть модель сольватации COSMO , модель поляризуемого континуума (PCM) или модель гибридной сольватации. [1]
Простые модели воды
[ редактировать ]Жесткие модели считаются простейшими моделями воды и основаны на несвязанных взаимодействиях . В этих моделях связывающие взаимодействия неявно учитываются голономными ограничениями . Электростатическое взаимодействие моделируется с помощью закона Кулона , а силы дисперсии и отталкивания — с помощью потенциала Леннарда-Джонса . [2] [3] Потенциал таких моделей, как TIP3P (переносной межмолекулярный потенциал с 3 точками) и TIP4P представлен
где k C , электростатическая константа , имеет значение 332,1 Å·ккал/(моль · е² ) в единицах, обычно используемых в молекулярном моделировании. [ нужна ссылка ] ; [4] [5] [6] q i и q j — парциальные заряды относительно заряда электрона; r ij — расстояние между двумя атомами или заряженными узлами; A B и — параметры Леннарда-Джонса . Заряженные сайты могут находиться на атомах или на фиктивных сайтах (например, неподеленных парах). В большинстве моделей воды термин Леннарда-Джонса применяется только к взаимодействию между атомами кислорода.
На рисунке ниже показана общая форма моделей воды с 3–6 участками. Точные геометрические параметры (расстояние OH и угол HOH) различаются в зависимости от модели.
2-сайт
[ редактировать ]Было показано, что модель воды с двумя узлами, основанная на знакомой модели SPC с тремя узлами (см. Ниже), позволяет предсказывать диэлектрические свойства воды с использованием теории молекулярной жидкости с перенормировкой узлов. [7]
3-сайт
[ редактировать ]Трехузловые модели имеют три точки взаимодействия, соответствующие трем атомам молекулы воды. Каждый узел имеет точечный заряд, а узел, соответствующий атому кислорода, также имеет параметры Леннарда-Джонса. Поскольку трехсайтовые модели достигают высокой вычислительной эффективности, они широко используются во многих приложениях молекулярно-динамического моделирования. Большинство моделей используют жесткую геометрию, соответствующую геометрии реальных молекул воды. Исключением является модель SPC, которая предполагает идеальную форму тетраэдра (угол HOH 109,47°) вместо наблюдаемого угла 104,5°.
В таблице ниже перечислены параметры для некоторых трехпозиционных моделей.
| СОВЕТЫ [8] | НПЦ [9] | СОВЕТ3P [10] | СПК/Э [11] | |
|---|---|---|---|---|
| р (О), о | 0.9572 | 1.0 | 0.9572 | 1.0 |
| ХОХ, ты | 104.52 | 109.47 | 104.52 | 109.47 |
| А , 10 3 ккал Ой 12 /моль | 580.0 | 629.4 | 582.0 | 629.4 |
| Б , ккал Å 6 /моль | 525.0 | 625.5 | 595.0 | 625.5 |
| д (О) | −0.80 | −0.82 | −0.834 | −0.8476 |
| д (Н) | +0.40 | +0.41 | +0.417 | +0.4238 |
Модель SPC/E добавляет поправку на среднюю поляризацию к функции потенциальной энергии:
где ц — электрический дипольный момент эффективно поляризованной молекулы воды (2,35 Д для модели SPC/E), ц 0 — дипольный момент изолированной молекулы воды (1,85 Д из эксперимента), а α i — константа изотропной поляризуемости , значение 1,608 × 10 −40 Ф ·м 2 . Поскольку заряды в модели постоянны, эта поправка приводит лишь к добавлению 1,25 ккал/моль (5,22 кДж/моль) к общей энергии. Модель SPC/E обеспечивает лучшую плотность и константу диффузии, чем модель SPC.
Модель TIP3P, реализованная в силовом поле CHARMM, представляет собой слегка модифицированную версию оригинала. Разница заключается в параметрах Леннарда-Джонса: в отличие от TIP3P, версия модели CHARMM помещает параметры Леннарда-Джонса также на атомы водорода, помимо параметра кислорода. Начисления не изменяются. [12] Трехместная модель (TIP3P) имеет лучшую производительность при расчете удельных плавок. [13]
Гибкая модель воды SPC
[ редактировать ]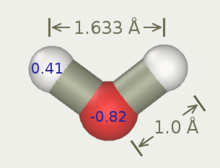
Гибкая простая модель воды с точечным зарядом (или гибкая модель воды SPC) представляет собой повторную параметризацию модели воды SPC с тремя участками. [14] [15] Модель SPC является жесткой, а гибкая модель SPC является гибкой. В модели Тукана и Рахмана растяжение O – H делается ангармоническим, и, таким образом, динамическое поведение хорошо описывается. Это одна из наиболее точных трехцентровых моделей воды без учета поляризации . При моделировании молекулярной динамики это дает правильную плотность и диэлектрическую проницаемость воды. [16]
Гибкая SPC реализована в программах MDynaMix и Abalone .
Другие модели
[ редактировать ]- Фергюсон (гибкий SPC) [17]
- CVFF (гибкий)
- МГ (гибкий и диссоциативный) [18]
- Потенциал ККИ (гибкая модель). [19]
- BLXL (размытие заряженного потенциала). [20]
4-сайт
[ редактировать ]Модели с четырьмя узлами имеют четыре точки взаимодействия за счет добавления одного фиктивного атома рядом с кислородом вдоль биссектрисы угла HOH моделей с тремя узлами (обозначены буквой M на рисунке). Фиктивный атом имеет только отрицательный заряд. Эта модель улучшает электростатическое распределение вокруг молекулы воды. Первой моделью, в которой использовался этот подход, была модель Бернала-Фаулера, опубликованная в 1933 году. [21] что также может быть самой ранней водной моделью. Однако модель БФ плохо воспроизводит объемные свойства воды, такие как плотность и теплота испарения , и поэтому представляет только исторический интерес. Это следствие метода параметризации; более новые модели, разработанные после того, как стали доступны современные компьютеры, были параметризованы путем запуска Metropolis Monte Carlo или моделирования молекулярной динамики и корректировки параметров до тех пор, пока объемные свойства не будут воспроизведены достаточно хорошо.
Модель TIP4P, впервые опубликованная в 1983 году, широко реализована в пакетах программного обеспечения для вычислительной химии и часто используется для моделирования биомолекулярных систем. В дальнейшем были произведены изменения параметров модели TIP4P для конкретных целей: модель TIP4P-Ew для использования с методами суммирования Эвальда; TIP4P/Ice для моделирования твердого водяного льда; TIP4P/2005, общая параметризация для моделирования всей фазовой диаграммы конденсированной воды; и TIP4PQ/2005, аналогичная модель, но предназначенная для точного описания свойств твердой и жидкой воды, когда в моделирование включены квантовые эффекты. [22]
В большинстве моделей воды с четырьмя узлами используются расстояние OH и угол HOH, которые соответствуют углам свободной молекулы воды. Единственным исключением является модель OPC, в которой не налагается никаких геометрических ограничений, кроме фундаментальной C 2v молекулярной симметрии молекулы воды. Вместо этого точечные заряды и их положения оптимизируются для лучшего описания электростатики молекулы воды. OPC воспроизводит полный набор объемных свойств более точно, чем некоторые из широко используемых моделей воды с жесткими n -участками. Модель OPC реализована в силовом поле AMBER .
| лучший друг [21] | СОВЕТЫ2 [23] | СОВЕТ4P [10] | TIP4P-Фу [24] | TIP4P/Лед [25] | ТИП4П/2005 [26] | ОПК [27] | ТИП4П-Д [28] | |
|---|---|---|---|---|---|---|---|---|
| р (О), о | 0.96 | 0.9572 | 0.9572 | 0.9572 | 0.9572 | 0.9572 | 0.8724 | 0.9572 |
| ХОХ, ты | 105.7 | 104.52 | 104.52 | 104.52 | 104.52 | 104.52 | 103.6 | 104.52 |
| r (ОМ), Å | 0.15 | 0.15 | 0.15 | 0.125 | 0.1577 | 0.1546 | 0.1594 | 0.1546 |
| А , 10 3 ккал Ой 12 /моль | 560.4 | 695.0 | 600.0 | 656.1 | 857.9 | 731.3 | 865.1 | 904.7 |
| Б , ккал Å 6 /моль | 837.0 | 600.0 | 610.0 | 653.5 | 850.5 | 736.0 | 858.1 | 900.0 |
| д (М) | −0.98 | −1.07 | −1.04 | −1.04844 | −1.1794 | −1.1128 | −1.3582 | −1.16 |
| д (Н) | +0.49 | +0.535 | +0.52 | +0.52422 | +0.5897 | +0.5564 | +0.6791 | +0.58 |
Другие:
5-сайт
[ редактировать ]Модели с 5 узлами помещают отрицательный заряд на фиктивные атомы (обозначенные L ), представляющие неподеленные пары атома кислорода с геометрией, напоминающей тетраэдр. Ранней моделью этого типа была модель BNS Бен-Наима и Стиллингера, предложенная в 1971 году. [ нужна ссылка ] вскоре на смену ей пришла модель ST2 Стиллингера и Рахмана в 1974 году. [31] В основном из-за более высоких вычислительных затрат модели с пятью площадками не получили широкого развития до 2000 года, когда была опубликована модель TIP5P Махони и Йоргенсена. [32] По сравнению с более ранними моделями модель TIP5P приводит к улучшению геометрии димера воды , более «тетраэдрической» структуре воды, которая лучше воспроизводит экспериментальные функции радиального распределения по дифракции нейтронов и температуре максимальной плотности воды. Модель TIP5P-E представляет собой перепараметризацию TIP5P для использования с суммами Эвальда .
| БНС [31] | СТ2 [31] | СОВЕТ5P [32] | ТИП5P-E [33] | |
|---|---|---|---|---|
| р (О), о | 1.0 | 1.0 | 0.9572 | 0.9572 |
| ХОХ, ты | 109.47 | 109.47 | 104.52 | 104.52 |
| r (ОЛ), Å | 1.0 | 0.8 | 0.70 | 0.70 |
| лол, ты | 109.47 | 109.47 | 109.47 | 109.47 |
| А , 10 3 ккал Ой 12 /моль | 77.4 | 238.7 | 544.5 | 554.3 |
| Б , ккал Å 6 /моль | 153.8 | 268.9 | 590.3 | 628.2 |
| д (л) | −0.19562 | −0.2357 | −0.241 | −0.241 |
| д (Н) | +0.19562 | +0.2357 | +0.241 | +0.241 |
| Р Л , Å | 2.0379 | 2.0160 | ||
| Р У , Å | 3.1877 | 3.1287 |
Обратите внимание, однако, что модели BNS и ST2 не используют закон Кулона для электростатических членов напрямую, а используют его модифицированную версию, масштаб которой уменьшается на коротких расстояниях путем умножения на функцию переключения S ( r ):
образом, параметры RL Таким и RU применимы только к BNS и ST2.
6-сайт
[ редактировать ]Первоначально предназначенная для изучения систем вода/лед, Нада и ван дер Эрден разработали модель из 6 участков, которая объединяет все участки моделей из 4 и 5 участков. [34] Так как у него была очень высокая температура плавления. [35] при использовании в периодических электростатических условиях (суммирование Эвальда), позже была опубликована модифицированная версия. [36] оптимизирован с использованием метода Эвальда для оценки кулоновского взаимодействия.
Другой
[ редактировать ]- Влияние явной модели растворенного вещества на поведение растворенного вещества в биомолекулярном моделировании также широко изучалось. Было показано, что явные модели воды влияют на специфическую сольватацию и динамику развернутых пептидов, в то время как конформационное поведение и гибкость свернутых пептидов остаются неизменными. [37]
- Модель МБ. Более абстрактная модель, напоминающая логотип Mercedes-Benz , воспроизводящая некоторые особенности воды в двухмерных системах. Он не используется как таковой для моделирования «реальных» (т. е. трехмерных) систем, но полезен для качественных исследований и в образовательных целях. [38]
- Крупнозернистые модели. Также разработаны одно- и двухсайтовые модели воды. [39] В крупнозернистых моделях каждый участок может представлять несколько молекул воды.
- Многокорпусные модели. Модели воды, построенные с использованием конфигураций обучающего набора, решенных квантово-механически, которые затем используют протоколы машинного обучения для извлечения поверхностей с потенциальной энергией. Эти поверхности потенциальной энергии используются в МД-моделировании с беспрецедентной степенью точности при расчете физических свойств конденсированных фазовых систем. [40]
Стоимость вычислений
[ редактировать ]Вычислительные затраты на моделирование воды увеличиваются с увеличением количества мест взаимодействия в модели воды. Время процессора примерно пропорционально количеству межатомных расстояний, которые необходимо вычислить. Для трехузловой модели для каждой пары молекул воды требуется 9 расстояний (каждый атом одной молекулы против каждого атома другой молекулы, или 3 × 3). Для 4-узловой модели требуется 10 расстояний (каждый заряженный узел с каждым заряженным узлом плюс взаимодействие О–О, или 3 × 3 + 1). Для 5-сайтовой модели необходимо 17 расстояний (4×4+1). Наконец, для модели с 6 площадками требуется 26 расстояний (5×5+1).
При использовании моделей жесткой воды в молекулярной динамике возникают дополнительные затраты, связанные с сохранением структуры ограниченной с использованием алгоритмов ограничений (хотя при ограничении длин связей часто можно увеличить шаг по времени).
См. также
[ редактировать ]- Вода (свойства)
- Вода (страница данных)
- Водный димер
- Силовое поле (химия)
- Сравнение реализаций силового поля
- Молекулярная механика
- Молекулярное моделирование
- Сравнение программного обеспечения для моделирования молекулярной механики
- Модели растворителей
Ссылки
[ редактировать ]- ^ Скайнер Р.Э., МакДонах Дж.Л., Грум С.Р., ван Мурик Т., Митчелл Дж.Б. (март 2015 г.). «Обзор методов расчета свободных энергий растворов и моделирования систем в растворе» (PDF) . Физическая химия Химическая физика . 17 (9): 6174–91. Бибкод : 2015PCCP...17.6174S . дои : 10.1039/C5CP00288E . ПМИД 25660403 .
- ^ Аллен, член парламента, диджей Тилдесли (1989). Компьютерное моделирование жидкостей . Кларендон Пресс. ISBN 978-0-19-855645-9 .
- ^ Кирби Би Джей. Микро- и наномеханика жидкости: транспорт в микрофлюидных устройствах .
- ^ Суэйлс Дж. М., Ройтберг А. Е. (2013). «Файл prmtop {A}mber» (PDF) .
- ^ Суэйлс Дж. М. (2013). Моделирование сложных биологических систем на основе свободной энергии при постоянном pH (PDF) . Университет Флориды.
- ^ Дело Д.А., Уокер Р.К., Читэм III Т.Э., Зиммерлинг К.Л., Ройтберг А., Мерц К.М. и др. (апрель 2019 г.). «Справочное руководство Amber 2019 (охватывает Amber18 и AmberTools19)» (PDF) .
- ^ Дайер К.М., Перкинс Дж.С., Стелл Дж., Петтитт Б.М. (2009). «Теория молекулярной жидкости с перенормировкой сайта: о полезности двухсайтовой модели воды» . Молекулярная физика . 107 (4–6): 423–431. Бибкод : 2009МолФ.107..423Д . дои : 10.1080/00268970902845313 . ПМЦ 2777734 . ПМИД 19920881 .
- ^ Йоргенсен, Уильям Л. (1981). «Квантово-статистико-механические исследования жидкостей. 10. Переносные межмолекулярные потенциальные функции для воды, спиртов и простых эфиров. Приложение к жидкой воде». Журнал Американского химического общества . 103 (2). Американское химическое общество (ACS): 335–340. дои : 10.1021/ja00392a016 . ISSN 0002-7863 .
- ^ HJC Berendsen, JPM Postma, WF van Gunsteren и J. Hermans, In Intermolecular Forces , под редакцией Б. Пулмана.(Рейдель, Дордрехт, 1981 ), с. 331.
- ^ Перейти обратно: а б Йоргенсен В.Л., Чандрасекхар Дж., Мадура Дж.Д., Импи Р.В., Кляйн М.Л. (1983). «Сравнение простых потенциальных функций для моделирования жидкой воды». Журнал химической физики . 79 (2): 926–935. Бибкод : 1983JЧФ..79..926J . дои : 10.1063/1.445869 .
- ^ Берендсен Х.Дж. , Григера Дж.Р., Страатсма Т.П. (1987). «Недостающий член в эффективных парных потенциалах». Журнал физической химии . 91 (24): 6269–6271. дои : 10.1021/j100308a038 .
- ^ МакКерелл А.Д., Башфорд Д., Беллотт М., Данбрек Р.Л., Эвансек Дж.Д., Филд М.Дж. и др. (апрель 1998 г.). «Полноатомный эмпирический потенциал для молекулярного моделирования и исследования динамики белков». Журнал физической химии Б. 102 (18): 3586–616. дои : 10.1021/jp973084f . ПМИД 24889800 .
- ^ Мао Ю, Чжан Ю (2012). «Теплопроводность, сдвиговая вязкость и теплоемкость моделей жесткой воды». Письма по химической физике . 542 : 37–41. Бибкод : 2012CPL...542...37M . дои : 10.1016/j.cplett.2012.05.044 .
- ^ Тукан К., Рахман А. (март 1985 г.). «Молекулярно-динамическое исследование движения атомов в воде». Физический обзор B . 31 (5): 2643–2648. Бибкод : 1985PhRvB..31.2643T . дои : 10.1103/PhysRevB.31.2643 . ПМИД 9936106 .
- ^ Берендсен Х.Дж., Григера Дж.Р., Страатсма Т.П. (1987). «Недостающий член в эффективных парных потенциалах». Журнал физической химии . 91 (24): 6269–6271. дои : 10.1021/j100308a038 .
- ^ Прапротник М., Янезич Д., Маври Дж. (2004). «Температурная зависимость колебательного спектра воды: исследование методом молекулярной динамики». Журнал физической химии А. 108 (50): 11056–11062. Бибкод : 2004JPCA..10811056P . дои : 10.1021/jp046158d .
- ^ Фергюсон, Дэвид М. (апрель 1995 г.). «Параметризация и оценка гибкой модели воды» . Журнал вычислительной химии . 16 (4): 501–511. дои : 10.1002/jcc.540160413 . S2CID 206038409 . Проверено 28 июля 2021 г.
- ^ Модель MG. Архивировано 4 марта 2016 г. в Wayback Machine .
- ^ Кумагай Н., Кавамура К., Ёкокава Т. (1994). «Межатомная потенциальная модель H2O: применение к полиморфам воды и льда». Молекулярное моделирование . 12 (3–6). Информа UK Limited: 177–186. дои : 10.1080/08927029408023028 . ISSN 0892-7022 .
- ^ Бернхэм Си Джей, Ли Джей, Ксантеас С.С., Лесли М. (1999). «Параметризация полноатомной поляризуемой модели воды типа Толе из первых принципов и ее применение к исследованию кластеров воды (n = 2–21) и фононного спектра льда Ih». Журнал химической физики . 110 (9): 4566–4581. Бибкод : 1999JChPh.110.4566B . дои : 10.1063/1.478797 .
- ^ Перейти обратно: а б Бернал Дж. Д., Фаулер Р. Х. (1933). «Теория воды и ионных растворов с особым упором на ионы водорода и гидроксила». Журнал химической физики . 1 (8): 515. Бибкод : 1933ЖЧФ...1..515Б . дои : 10.1063/1.1749327 .
- ^ Макбрайд, К.; Вега, К.; Нойя, Е.Г.; Рамирес, Р.; Сесе, Л.М. (2009). «Квантовый вклад в ледяные фазы: путь к новой эмпирической модели воды — TIP4PQ/2005». Дж. Хим. Физ . 131 (2): 024506. arXiv : 0906.3967 . Бибкод : 2009JChPh.131b4506M . дои : 10.1063/1.3175694 . ПМИД 19604003 . S2CID 15505037 .
- ^ Йоргенсен (1982). «Пересмотренные СОВЕТЫ для моделирования жидкой воды и водных растворов» . Журнал химической физики . 77 (8): 4156–4163. Бибкод : 1982JChPh..77.4156J . дои : 10.1063/1.444325 .
- ^ Хорн Х.В., Своп В.К., Питера Дж.В., Мадура Дж.Д., Дик Т.Дж., Хура Г.Л., Хед-Гордон Т. (май 2004 г.). «Разработка улучшенной модели воды с четырьмя участками для биомолекулярного моделирования: TIP4P-Ew». Журнал химической физики . 120 (20): 9665–78. Бибкод : 2004JChPh.120.9665H . дои : 10.1063/1.1683075 . ПМИД 15267980 . S2CID 39545298 .
- ^ Абаскаль Х.Л., Санс Э., Гарсиа Фернандес Р., Вега С. (июнь 2005 г.). «Потенциальная модель для изучения льдов и аморфной воды: TIP4P/Ice». Журнал химической физики . 122 (23): 234511. Бибкод : 2005JChPh.122w4511A . дои : 10.1063/1.1931662 . ПМИД 16008466 . S2CID 8382245 .
- ^ Абаскаль Дж.Л., Вега С (декабрь 2005 г.). «Общая модель конденсированных фаз воды: TIP4P/2005». Журнал химической физики . 123 (23): 234505. Бибкод : 2005JChPh.123w4505A . дои : 10.1063/1.2121687 . ПМИД 16392929 . S2CID 9757894 .
- ^ Изади С., Анандакришнан Р., Онуфриев А.В. (ноябрь 2014 г.). «Построение водных моделей: другой подход» . Журнал физической химии . 5 (21): 3863–3871. arXiv : 1408.1679 . Бибкод : 2014arXiv1408.1679I . дои : 10.1021/jz501780a . ПМК 4226301 . ПМИД 25400877 .
- ^ Пиана С., Дончев А.Г., Робустелли П., Шоу Д.Е. (апрель 2015 г.). «Водно-дисперсионные взаимодействия сильно влияют на моделируемые структурные свойства неупорядоченных состояний белка» . Журнал физической химии Б. 119 (16): 5113–23. дои : 10.1021/jp508971m . ПМИД 25764013 .
- ^ Хабершон, С.; Маркланд, штат Теннесси; Манолопулос, Делавэр (2009). «Конкурирующие квантовые эффекты в динамике гибкой модели воды». Дж. Хим. Физ . 131 (2): 024501. arXiv : 1011.1047 . Бибкод : 2009JChPh.131b4501H . дои : 10.1063/1.3167790 . ПМИД 19603998 . S2CID 9095938 .
- ^ Гонсалес, Массачусетс; Абаскаль, JJF (2011). «Гибкая модель воды на основе TIP4P/2005». Дж. Хим. Физ . 135 (22): 224516. Бибкод : 2011JChPh.135v4516G . дои : 10.1063/1.3663219 . ПМИД 22168712 .
- ^ Перейти обратно: а б с Стиллингер Ф.Х., Рахман А. (1974). «Улучшенное моделирование жидкой воды методом молекулярной динамики». Журнал химической физики . 60 (4): 1545–1557. Бибкод : 1974ЖЧФ..60.1545С . дои : 10.1063/1.1681229 . S2CID 96035805 .
- ^ Перейти обратно: а б Махони М.В., Йоргенсен В.Л. (2000). «Пятиузловая модель жидкой воды и воспроизведение аномалии плотности жесткими неполяризуемыми потенциальными функциями». Журнал химической физики . 112 (20): 8910–8922. Бибкод : 2000JChPh.112.8910M . дои : 10.1063/1.481505 . S2CID 16367148 .
- ^ Рик С.В. (апрель 2004 г.). «Повторная оптимизация водного потенциала пяти объектов (TIP5P) для использования с суммами Эвальда» . Журнал химической физики . 120 (13): 6085–93. Бибкод : 2004JChPh.120.6085R . дои : 10.1063/1.1652434 . ПМИД 15267492 .
- ^ Нада, Х. (2003). с шестью участками «Модель межмолекулярного потенциала для моделирования льда и воды вблизи точки плавления: модель H 2 O ». Журнал химической физики . 118 (16): 7401. Бибкод : 2003JChPh.118.7401N . дои : 10.1063/1.1562610 .
- ^ Абаскаль Х.Л., Фернандес Р.Г., Вега С., Кариньяно М.А. (октябрь 2006 г.). «Температура плавления шестизонной потенциальной модели воды». Журнал химической физики . 125 (16): 166101. Бибкод : 2006JChPh.125p6101A . дои : 10.1063/1.2360276 . ПМИД 17092145 . S2CID 33883071 .
- ^ Нада Х (декабрь 2016 г.). «2O и моделирование молекулярной динамики». Журнал химической физики . 145 (24): 244706. Бибкод : 2016JChPh.145x4706N . дои : 10.1063/1.4973000 . ПМИД 28049310 .
- ^ Флорова П., Скленовский П., Банаш П., Отепка М. (ноябрь 2010 г.). «Явные модели воды влияют на специфическую сольватацию и динамику развернутых пептидов, в то время как конформационное поведение и гибкость свернутых пептидов остаются неизменными» . Журнал химической теории и вычислений . 6 (11): 3569–79. дои : 10.1021/ct1003687 . ПМИД 26617103 .
- ^ Сильверстайн К.А., Хаймет А.Д., Дилл К.А. (1998). «Простая модель воды и гидрофобный эффект». Журнал Американского химического общества . 120 (13): 3166–3175. дои : 10.1021/ja973029k .
- ^ Извеков С., Вот Г.А. (октябрь 2005 г.). «Многомасштабное грубое определение жидкостных систем». Журнал химической физики . 123 (13). Издательство АИП: 134105. Бибкод : 2005JChPh.123m4105I . дои : 10.1063/1.2038787 . ПМИД 16223273 .
- ^ Меддерс Г.Р., Паэсани Ф. (март 2015 г.). «Инфракрасная и рамановская спектроскопия жидкой воды с помощью «первых принципов» молекулярной динамики многих тел». Журнал химической теории и вычислений . 11 (3): 1145–54. дои : 10.1021/ct501131j . ПМИД 26579763 .
- ^ Сиснерос Г.А., Викфельдт К.Т., Оямяэ Л., Лу Дж., Сюй Ю., Торабифард Х. и др. (июль 2016 г.). «Моделирование молекулярных взаимодействий в воде: от парных к функциям потенциальной энергии многих тел» . Химические обзоры . 116 (13): 7501–28. doi : 10.1021/acs.chemrev.5b00644 . ПМЦ 5450669 . ПМИД 27186804 .
- ^ Викфельдт К.Т., Батиста Э.Р., Вила Ф.Д., Йонссон Х. (октябрь 2013 г.). «Передаваемый потенциал взаимодействия H2O, основанный на расширении одного центрального мультиполя: SCME». Физическая химия Химическая физика . 15 (39): 16542–56. arXiv : 1306.0327 . Бибкод : 2013PCCP...1516542W . дои : 10.1039/c3cp52097h . ПМИД 23949215 . S2CID 15215071 .




