Кукурбитурил

В химии «гость-хозяин» состоящие кукурбитурилы представляют собой макроциклические молекулы, из гликолурила ( =C 4 H 2 N 4 O 2 = ) мономеры, связанные метиленовыми мостиками ( −CH 2 − ). Атомы кислорода расположены по краям зоны и наклонены внутрь, образуя частично закрытую полость ( кавитанд ). Название происходит от сходства этой молекулы с тыквой семейства Cucurbitaceae .
Кукурбитурилы обычно обозначаются как кукурбит[ n ]урил , где n — количество гликолуриловых единиц. Двумя распространенными сокращениями являются CB[ n ] или просто CB n .
Эти соединения особенно интересны химикам, поскольку они являются подходящими хозяевами для множества нейтральных и катионных частиц. Считается, что способ связывания происходит за счет гидрофобных взаимодействий, а в случае катионных гостей также за счет катион-дипольных взаимодействий. Размеры кукурбитурилов обычно составляют ~ 10 Å . Например, полость кукурбит[6]урила имеет высоту ~9,1 Å, внешний диаметр ~5,8 Å и внутренний диаметр ~3,9 Å. [1]
Кукурбитурилы были впервые синтезированы в 1905 году Робертом Берендом путем конденсации гликолурила с формальдегидом . [2] но их структура не была выяснена до 1981 года. [3] Область расширилась, когда CB5, CB7 и CB8 были обнаружены и выделены Ким Кимуном в 2000 году. [4] На сегодняшний день все кукурбитурилы, состоящие из 5, 6, 7, 8, 10 и 14 повторяющихся единиц, [5] [6] которые имеют объемы внутренней полости 82, 164, 279, 479 и 870 Å. 3 соответственно. Кукурбитурил, состоящий из 9 повторяющихся единиц, еще не выделен (по состоянию на 2009 г.). Другие распространенные молекулярные капсулы, которые имеют сходную с кукурбитурилами молекулярную форму, включают циклодекстрины , каликсарены и столбарены .
Синтез
[ редактировать ]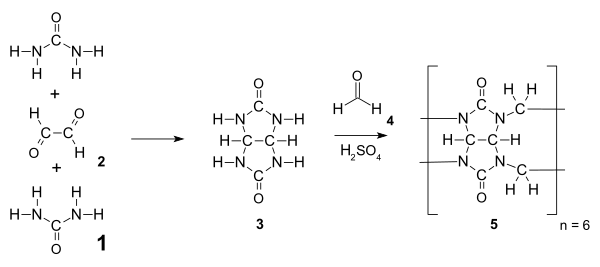
Кукурбитурилы являются амидалами (точнее аминалями ) и синтезируются из мочевины 1 и диальдегида (например, глиоксаля 2 ) посредством нуклеофильного присоединения с образованием промежуточного гликолурила 3 . Это промежуточное соединение конденсируется с формальдегидом с образованием гексамера кукурбит[6]урила при температуре выше 110 °C. Обычно многофункциональные мономеры, такие как 3, подвергаются ступенчатой полимеризации , которая приводит к распределению продуктов, но из-за благоприятной деформации и обилия водородных связей гексамер является единственным продуктом реакции, выделяемым после осаждения. [5]
Снижение температуры реакции до 75–90 ° C можно использовать для доступа к кукурбитурилам других размеров, включая CB[5], CB[7], CB[8] и CB[10]. CB[6] по-прежнему остается основным продуктом; кольца других размеров образуются с меньшими выходами. Выделение размеров, отличных от CB[6], требует фракционной кристаллизации и растворения. CB[5], CB[6], CB[7] и CB[8] в настоящее время коммерчески доступны. Большие размеры являются особенно активной областью исследований, поскольку они могут связывать более крупные и интересные гостевые молекулы, расширяя тем самым их потенциальное применение.

Кукурбит[10]урил особенно трудно выделить. Впервые он был обнаружен Дэй и его коллегами в 2002 году как комплекс включения, содержащий CB[5] путем фракционной кристаллизации реакционной смеси кукурбитурила. [7] CB[10]·CB[5] был однозначно идентифицирован с помощью рентгеноструктурного анализа монокристалла, который показал, что комплекс напоминает молекулярный гироскоп . В этом случае свободное вращение CB[5] внутри полости CB[10] имитирует независимое вращение маховика внутри корпуса гироскопа.
Выделение чистого CB[10] не могло быть осуществлено методами прямого разделения, поскольку соединение имеет очень высокое сродство к CB[5]. Сильное сродство связывания с CB[5] можно понять, поскольку он имеет размер и форму, дополняющие полость CB[10]. Чистый CB[10] был выделен Айзексом и его коллегами в 2005 году путем введения более прочно связывающегося гостя меламин- диамина, который способен вытеснять CB[5]. [8] Затем меламин-диамин отделяли от CB[10] реакцией с уксусным ангидридом , которая превращала положительно заряженные аминогруппы в нейтрально заряженные амиды. Кукурбитурилы прочно связывают катионных гостей, но удаление положительного заряда с гостя меламин-диамин снижает константу ассоциации до такой степени, что ее можно удалить промыванием метанолом , ДМСО и водой. CB[10] имеет необычно большую полость (870 Å). 3 ), который свободен и способен связывать чрезвычайно крупные гости, включая катионный каликс[4]арен .
Приложения
[ редактировать ]Кукурбитурилы использовались химиками для различных целей, включая доставку лекарств, асимметричный синтез, молекулярное переключение и настройку красителей.
Супрамолекулярные молекулы-хозяева
[ редактировать ]
Кукурбитурилы являются эффективными молекулами-хозяевами в молекулярном распознавании и обладают особенно высоким сродством к положительно заряженным или катионным соединениям. Высокие константы ассоциации с положительно заряженными молекулами объясняются карбонильными группами, которые выстилают каждый конец полости и могут взаимодействовать с катионами аналогично краун-эфирам. Сродство кукурбитурилов может быть очень высоким. Например, константа равновесия сродства кукурбит[7]урила с положительно заряженным гидрохлоридом 1-аминоадамантана экспериментально определена при 4,23*10. 12 . [10]
Взаимодействие с гостем-хозяином также существенно влияет на растворимость кукурбитурилов. Кукурбит[6]урил плохо растворяется практически в любом растворителе, но растворимость значительно улучшается в растворе гидроксида калия или в кислом растворе. Кавитанд . образует положительно заряженное соединение включения с ионом калия или ионом гидроксония соответственно, которое имеет гораздо большую растворимость, чем нейтральная молекула без комплекса [11]
CB[10] достаточно велик, чтобы удерживать другие молекулярные хозяева, такие как молекула каликсарена . С гостем каликсарена различные химические конформации (конус, 1,2-альтернативный, 1,3-альтернативный) находятся в быстром равновесии. Аллостерический контроль обеспечивается, когда молекула адамантана вызывает конформацию конформации с комплексом включения каликсарен-адамантан внутри молекулы CB[10].
Ротаксановые макроциклы
[ редактировать ]Учитывая их высокое сродство к образованию комплексов включения, кукурбитурилы были использованы в качестве макроциклического компонента ротаксана . После образования супрамолекулярной сборки или нитевого комплекса с молекулой-гостем, такой как гексаметилендиамин, два конца гостя могут вступить в реакцию с объемистыми группами, которые затем будут действовать как стопоры, предотвращающие диссоциацию двух отдельных молекул. [12]
В другой ротаксановой системе с колесом CB[7] ось представляет собой 4,4'-бипиридиний или виологеновую субъединицу с двумя алифатическими N-заместителями на конце карбоновой кислоты на обоих концах. [13] В воде при концентрации выше 0,5 мМ комплексообразование происходит количественно без необходимости использования пробок. При pH карбоксильные = 2 концевые группы протонируются, и колесо перемещается между ними взад и вперед, о чем свидетельствует присутствие всего двух протонов ароматического виологена в спектре протонного ЯМР . При pH = 9 колесо блокируется вокруг виологенного центра. В последнее время ротаксан [14] с колесом CB[8]. Этот ротаксан может связывать нейтральные молекулы гостя.
Средства доставки лекарств
[ редактировать ]Свойства «хозяин-гость» кукурбитурила были исследованы на предмет использования средств доставки лекарств. [15] Потенциал этого применения был изучен с использованием кукурбит[7]урила, который образует соединение включения с важным противораковым препаратом оксалиплатином . CB[7] был использован, несмотря на то, что его труднее изолировать, поскольку он гораздо лучше растворяется в воде, а его полости большего размера могут вместить молекулу лекарственного средства. Было обнаружено, что полученный комплекс обладает повышенной стабильностью и большей селективностью, что может привести к меньшему количеству побочных эффектов. [16]
Супрамолекулярные катализаторы
[ редактировать ]Кукурбитурилы также исследовались в качестве супрамолекулярных катализаторов . Более крупные кукурбитурилы, такие как кукурбит[8]урил, могут связывать несколько молекул гостя. CB[8] образует комплекс 2:1 (гость:хозяин) с (E)-диаминостильбендигидрохлоридом, который удерживается за счет большего внутреннего диаметра CB[8] - 8,8 ангстрем и высоты 9,1 ангстрем . [17] Непосредственная близость и оптимальная ориентация гостевых молекул внутри полости увеличивает скорость фотохимической циклизации с образованием циклобутана димера со стереоселективностью 19:1 для син-конфигурации при связывании с CB[8]. В отсутствие CB[8] реакция циклизации не протекает, а только изомеризация транс-изомера в цис-изомер . наблюдается [18] [19]
Тюнинг красителя
[ редактировать ]Возможности кукурбитурилов по настройке красителей были изучены исследователями в последние годы. [20] [21] [22] [23] В целом было обнаружено, что ограниченная среда с низкой полярностью, обеспечиваемая кукурбитурилами, приводит к повышенной яркости, повышенной фотостабильности, увеличению времени жизни флуоресценции и сольватохромии , что соответствует переходу в среду с более низкой полярностью.
Родственные соединения
[ редактировать ]Инвертированные кукурбитурилы или i CB[x] представляют собой аналоги CB с одной инвертированной повторяющейся единицей гликолурила . [24] В этом устройстве метиновые протоны фактически направлены внутрь полости, и это делает полость менее просторной. Инвертированные кукурбитурилы образуются в качестве побочного продукта в реакциях образования CB с выходами от 2 до 0,4%. Выделение этого типа соединений ХБ возможно, поскольку сложнее образовать соединения включения, которые обычно образуются с обычными ХБ. Инвертированные кукурбитурилы считаются кинетически контролируемыми продуктами реакции, поскольку при нагревании i CB[6] в кислой среде образуется смесь CB[5], CB[6] и CB[7] в соотношении 24:13:1. .
Кукурбитурил, разрезанный пополам по экватору, называется гемикукурбитурилом .
Систематическое название
[ редактировать ]кукурбит[6]урила Систематическое название — додекагидро-1H,4H,14H,17H-2,16:3,15-диметано-5H,6H,7H,8H,9H,10H,11H,12H,13H,18H,19H, 20H,21H,22H,23H,24H,25H,26H-2,3,4а,5а,6а,7а,8а,9а,10а,11а,12а,13а,15,16,17а,18а,19а,20а, 21a,22a,23a,24a,25a,26a-тетракозаазабиспенталено[1''',6''':5'',6'',7'']циклооктил[1'',2'',3'': 3',4']пенталено(1',6':5,6,7)-циклоокта(1,2,3-gh:1',2',3'-g'h')циклоокта(1,2 ,3-cd:5,6,7-c'd')дипентален-1,4,6,8,10,12,14,17,19,21,23,25-додекон. [25] [26]
Ссылки
[ редактировать ]- ^ Обзор: Семья тыквенных [n]uril Джейсон Лагона, Притам Мукхопадхьяй, Шрипарна Чакрабарти, Лайл Айзекс Ангевандте Chemie, международное издание , том 44, выпуск 31, страницы 4844–4870, 2005 г. Аннотация
- ^ О продуктах конденсации гликолурила и формальдегида , Роберт Беренд, Эберхард Мейер, Франц Руше, Анналы химии Юстуса Либиха 1905 , 339, 1–37. два : 10.1002/jlac.19053390102
- ^ Кукурбитурил В.А. Фриман, В.Л. Мок и Нью-Йорк. Ши Дж. Ам. Ткань. Соц. , 1981 , 103, 7367. Статья
- ^ Ким, Джахон; Юнг, Ин-Сан; Ким, Су-Янг; Ли, Ынсон; Канг, Джин-Ку; Сакамото, Сигеру; Ямагучи, Кентаро; Ким, Кимун (2000). «Новые гомологи кукурбитурила: синтез, выделение, характеристика и рентгеновские кристаллические структуры кукурбита [n] урила (n = 5, 7 и 8)». Журнал Американского химического общества . 122 (3): 540–541. дои : 10.1021/ja993376p .
- ^ Jump up to: а б Гомологи и производные кукурбитурила: новые возможности в супрамолекулярной химии. хим. Рез., 36 (8), 621–630, 2003. Ссылка.
- ^ Ченг, Сяо-Цзе и др. «Витой тыквенный[14]урил». Angewandte Chemie International Edition 52.28 (2013): 7252–7255. Веб. два : 10.1002/ange.201210267
- ^ Jump up to: а б Гироскан на основе кукурбитурила: новая супрамолекулярная форма AnthonyI. Дэй, Родни Дж. Бланч, Алан П. Арнольд, Сьюзан Лоренцо, Гарет Р. Льюис и Ян Дэнс Энджью. хим. Межд. Эд. ; 2002 год ; 41(2), стр. 275–277.
- ^ Cucurbit[10]урил Симин Лю, Питер Ю. Завалидж и Лайл Айзекс Дж. Ам. Ткань. Соц. ; 2005 г .; 127(48) стр. 16798 – 16799; (Коммуникация) doi : 10.1021/ja056287n Аннотация
- ^ Фриман, Уэйд А. (1984). «Структуры аддуктов п -ксилилендиаммония хлорида и гидросульфата кальция кавитанда 'кукурбитурила', C 36 H 36 N 24 O 12 ». Акта Кристаллогр Б. 40 (4): 382–387. дои : 10.1107/S0108768184002354 .
- ^ Лю, Симин; Руспич, христианин; Мукхопадьяй, Притам; Чакрабарти, Шрипарна; Завалий, Питер Ю.; Айзекс, Лайл (2005). «Семейство тыквенных [н]урилов: основные компоненты для самосортирующихся систем». Журнал Американского химического общества . 127 (45): 15959–67. дои : 10.1021/ja055013x . ПМИД 16277540 .
- ^ Патент США 6 365 734.
- ^ Комплексообразование a,w-дикарбоновых кислот и a,w-диолов с кукурбитурилом и a-циклодекстрином. первый шаг к образованию ротаксанов и полиротаксенов полиэфирного типа Ханс-Юрген Бушманн, Клаус Янсен, Экхард Шольмейер Acta Chim. Слав. 1999 , 46(3), стр. 405-411. Статья заархивирована 16 июля 2012 г. в Wayback Machine.
- ^ Синделар, Владимир; Сильви, Серена; Кайфер, Анхель Э. (2006). «Включение и выключение молекулярного челнока: простые псевдоротаксаны с контролируемым pH на основе кукурбита [7]урила». Химические коммуникации (20): 2185–7. дои : 10.1039/b601959e . ПМИД 16703149 . S2CID 8649596 .
- ^ В. Рамалингам и А.Р. Урбах, Org. Письма., 2011, 13, 4898.
- ^ Гу, Алиса; Уит, Ниал (2021). «Макроциклы как вспомогательные вещества, усиливающие действие лекарственных препаратов, в фармацевтических препаратах». Журнал явлений включения и макроциклической химии . 100 (1–2): 55–69. дои : 10.1007/s10847-021-01055-9 . S2CID 233139034 .
- ^ Пшеница, Ниал; Лиманторо, Кристина (2016). «Кукурбит[ н ]урилы как вспомогательные вещества в фармацевтических лекарственных формах». Супрамолекулярная химия . 28 (9–10): 849–856. дои : 10.1080/10610278.2016.1178746 . hdl : 2123/15770 . S2CID 102258565 .
- ^ Простая стереоселективная [2 + 2] фотореакция, опосредованная кукурбитом[8]урилом Сан Ён Джон, Ён Хо Ко, Сан Хён Пак, Хи-Джун Ким и Кимун Ким Chemical Communications , 2001 , (19), 1938–1939 DOI Абстрактный
- ^ Матричная направленная фотодимеризация транс-1,2-бис(н-пиридил)этиленов и стильбазолов в воде Махеш Паттабираман, Арункумар Натараджан, Раджа Калиаппан, Джоэл Т. Мэг и В. Рамамурти Chemical Communications , 2005 , (36), 4542 - 4544 DOI Аннотация Полная статья
- ^ Маддипатла, Мурти ВСН; Каанумалле, Лакшми С.; Натараджан, Арункумар; Паттабираман, Махеш; Рамамурти, В. (2007). «Предварительная ориентация олефинов к одному фотодимеру: фотодимеризация протонированных азастильбенов в воде, опосредованная кукурбитурилом». Ленгмюр . 23 (14): 7545–54. дои : 10.1021/la700803k . ПМИД 17539667 .
- ^ Koner L. et al., Supramolec. Chem. 2007 , 19, 55-66.
- ^ Нау WM и др., Int. Дж. Фотоэнергетика 2005 , 7, 133-141.
- ^ Монтес-Наваяс П. и др., Chem. Физ. хим. 2008 , 9, 713-720.
- ^ Шейх Дж. и др., Photochem. и фотобиол. наук. 2008 , 7, 408-414.
- ^ Айзекс, Лайл; Пак, Сан-Кю; Лю, Симин; Ко, Ён Хо; Сельвапалам, Нараянан; Ким, Ёнгук; Ким, Хёнук; Завалий, Питер Ю.; и др. (2005). «Семейство перевернутых тыквенных[н]урилов» . Журнал Американского химического общества . 127 (51): 18000–1. дои : 10.1021/ja056988k . ПМИД 16366540 .
- ^ Моно-, олиго- и полиротаксаны с кукурбитурилом и смешанные полиротаксаны с кукурбитурилом и альфа-циклодекстрином посредством самосборки Клаудия Мешке 1999 Интернет, немецкий язык
- ^ «Тыквенный[6]урил» . pubchem.ncbi.nlm.nih.gov .