Диастереомер
Эта статья требует дополнительных цитат для проверки . ( сентябрь 2021 г. ) |
| Диастереомеры, которые также являются эпимерами | |
|---|---|
|
|

|

|
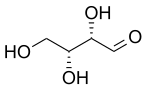
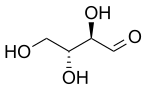
| D -threose | D -Erythrose |
В стереохимии диастереомеры диастереоизомерами (иногда называемые стереоизомера являются типом ) . [ 1 ] Диастереомеры определяются как немирроровое изображение, недентичные стереоизомеры. Следовательно, они встречаются, когда два или более стереоизомеры соединения имеют разные конфигурации на одном или нескольких (но не всех) эквивалентных (связанных) стереоцентеров и не являются зеркальными изображениями друг друга. [ 2 ] Когда два диастереоизомера отличаются друг от друга только в одном стереоцентре, они являются эпимерами . Каждый стереоцентр дает две разные конфигурации и, следовательно, обычно увеличивает количество стереоизомеров в два раза.
Диастереомеры отличаются от энантиомеров тем, что последние представляют собой пары стереоизомеров, которые отличаются во всех стереоцентрах и, следовательно, являются зеркальными изображениями друг друга. [ 3 ] Энантиомеры соединения с более чем одним стереоцентрором также являются диастереомерами других стереоизомеров этого соединения, которые не являются их зеркальным изображением (то есть за исключением противоположного энантиомера). Диастереомеры обладают разными физическими свойствами (в отличие от большинства аспектов энантиомеров) и часто различной химической реактивности .
Диастереомеры отличаются не только физическими свойствами, но и в химической реактивности - как соединение реагирует с другими. глюкоза и галактоза Например, являются диастереомерами. Несмотря на то, что они имеют одинаковый молярный вес, глюкоза более стабильна, чем галактоза. Эта разница в стабильности заставляет галактозу впитывать немного быстрее, чем глюкоза в организме человека. [ 4 ] [ 5 ]
Диастереоселективность является предпочтением образования одного или более одного диастереомера над другим в органической реакции . В целом, стереоселективность объясняется крутящими и стерическими взаимодействиями в стереоцентре, возникающих в результате электрофилов , приближающихся к стереоцентру. реакции [ 6 ]
Син / анти
[ редактировать ]Когда единственная связь между двумя центрами может вращаться, дескрипторы CIS/Trans становятся недействительными. Два широко принятых префикса, используемых для различения диастереомеров на SP³-гибридизированных связях в молекуле с открытой цепью, являются Syn и анти . Masamune предложила дескрипторы, которые работают, даже если группы не прикреплены к соседним атомам углерода. Это также работает независимо от приоритетов CIP . SYN описывает группы на одном и том же лицом, в то время как анти -анти описывает группы на противоположных лицах. Концепция относится только к проекции зигзагообразной. Дескрипторы описывают только относительную стереохимию, а не абсолютную стереохимию. Все изомеры одинаковы.
Эритро / Трео
[ редактировать ]Два более старых префикса, которые все еще обычно используются для различения диастереомеров, - это три и эритро . В случае сахаридов, когда в проекции Фишере, эритро -изомер, имеет два идентичных заместителя на одной и той же стороне, а Изомер Трео имеет их на противоположных сторонах. [ 7 ] При нарисовании в виде зигзагообразного цепи, эритро-изомер имеет два идентичных заместителя на разных сторонах плоскости (анти). Названия получены из диастереомерных четырехуглеродных альдоз эритроза и троса . Эти префиксы не рекомендуются для использования за пределами царства сахаридов, поскольку их определения могут привести к противоречивым интерпретациям. [ 8 ]
Другим тройным соединением является треонин , один из незаменимых аминокислот. Эритро аллотреонином -диастереомер его является .
  |
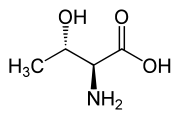
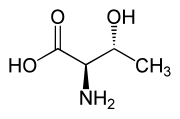
| L -Threonine (2 с , 3 r ) и d -troonine (2 r , 3 с ) |
  |
| L -Allothreonine (2 S , 3 S ) и D - Allothreonine (2 r , 3 r ) |
Несколько стереоцентров
[ редактировать ]Если молекула содержит два асимметричных центра, существует до четырех возможных конфигураций, и все они не могут быть не поддающимися суперпозируемым зеркальным изображениям друг друга. Возможности для разных изомеров продолжают умножаться, поскольку в молекулу добавляют больше стереоцентеров. В целом, количество стереоизомеров молекулы может быть определено путем расчета 2 не , где n = количество хиральных центров в молекуле. Это верно, за исключением случаев, когда молекула имеет мезо форм. Эти мезо соединения являются молекулами, которые содержат стереоцентеры , но обладают внутренней плоскостью симметрии, позволяющей быть суперпозированы на зеркальном изображении. Эти эквивалентные конфигурации не могут рассматриваться как диастереомеры. [ 9 ]
Для n = 3 есть восемь стереоизомеров. Среди них есть четыре пары энантиомеров: R, R, R и S, S, S; R, R, S и S, S, R; R, S, S и S, R, R; и R, S, R и S, R, S. Существует еще много пар диастереомеров, потому что каждая из этих конфигураций является диастереомером по отношению к любой другой конфигурации, за исключением собственного энантиомера (например, R, R, R - диастереомер R, R, S; R, S, R, R, R, R - диастереомер R, R, S; R, S, R, R, R, R ; и r, s, s). Для n = 4 существует шестнадцать стереоизомеров или восемь пар энантиомеров. Четыре энантиомерные пары альдопентозов и восемь энантиомерных пар альдогексозов (подмножества пяти- и шестиуглеродных сахаров) являются примерами наборов соединений, которые различаются таким образом.
Диастереомеризм в двойной связи
[ редактировать ]Изомеры двойной связи всегда считаются диастереомерами, а не энантиомерами. Диастереомеризм также может происходить в двойной связи , где цис - транс- положения заместителей относительные дают два несерповируемых изомеров. Многие конформационные изомеры также являются диастереомерами.
В случае диастереомеризма, возникающей в двойной связи, или Entgegen и Zusammen (немецкий) используется для уведомления номенклатуры алкенов EZ . [ 10 ]
Приложения
[ редактировать ]Как указывалось ранее, у двух диастереомеров не будет идентичных химических свойств. Это знание используется в хиральном синтезе , чтобы разделить смесь энантиомеров. Это принцип хирального разрешения . После подготовки диастереомеров они разделены хроматографией или рекристаллизацией . Обратите внимание также на пример стереохимии кетонизации enols и enolates .
Смотрите также
[ редактировать ]- CAHN -ENGOLD -PRELOG Правила приоритета для номенклатуры.
Ссылки
[ редактировать ]- ^ IUPAC "Золотая книга" Диастереоизомеризм два : 10.1351/goldbook.d01679
- ^ Гарретт, RH; Гришам, CM (2005), Биохимия 3 -е изд. , Белмонт, Калифорния: Томсон, с. 205, ISBN 0-534-41020-0 .
- ^ Iupac "Золотая книга" Enantiomer doi : 10.1351/goldbook.e02069
- ^ МакКанс, Роберт Александр; Мэддерс, Кейт (1930). «Сравнительные показатели поглощения сахаров из кишечника человека» . Биохимический журнал . 24 (3): 795–804. doi : 10.1042/bj0240795 . ISSN 0264-6021 . PMC 1254520 . PMID 16744419 .
- ^ Chao, Hsi-chun; Mcluckey, Scott A. (2020-10-06). «Дифференциация и количественная оценка диастереомерных пар гликосфинголипидов с использованием химии газофазного ионов» . Аналитическая химия . 92 (19): 13387–13395. doi : 10.1021/acs.analchem.0c02755 . ISSN 0003-2700 . PMC 7544660 . PMID 32883073 .
- ^ Лавинда, Ольга; Витт, Коллин Х.; Woerpel, Ka (2022-03-28). «Происхождение высокой диастереоселективности в реакциях эйнолятов из семи членов кольца» . Angewandte Chemie International Edition на английском языке . 61 (14): E202114183. doi : 10.1002/anie.202114183 . ISSN 1521-3773 . PMC 8940697 . PMID 35076978 .
- ^ Современная физическая органическая химия Эрик В. Анслин, Деннис А. Догерти 2006
- ^ Iupac , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « Erythro, Threo ». два : 10.1351/goldbook.e02212
- ^ Мерад, Иори; Кенди, Матье; Понс, Жан-Марк; Брэсси, Кирилл (май 2017 г.). «Каталитическая энантиоселективная десимметризация мезо соединений в полном синтезе натуральных продуктов: к экономике хиральных реагентов» . Синтез . 49 (9): 1938–1954. doi : 10.1055/s-0036-1589493 . ISSN 0039-7881 . S2CID 99010495 .
- ^ Браун, Уильям (2018). Органическая химия (8 -е изд.). Соединенные Штаты: Cengage Learning. С. 138–142. ISBN 9781305580350 .