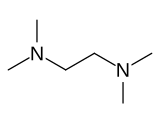
Тетраметилэтилендиамин
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК N , N , N ', N' -Тетраметилэтан-1,2-диамин [1] | |
| Идентификаторы | |
3D model ( JSmol ) | |
| Сокращения | ТМЕДА, ИХ |
| 1732991 | |
| ЧЭБИ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.003.405 |
| Номер ЕС |
|
| 2707 | |
| МеШ | N,N,N',N'-тетраметилэтилендиамин |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 2372 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 6 Ч 16 Н 2 | |
| Молярная масса | 116.208 g·mol −1 |
| Появление | Бесцветная жидкость |
| Запах | Рыбный, аммиачный |
| Плотность | 0,7765 г мл −1 (при 20 °С) |
| Температура плавления | −58,6 °С; −73,6 ° F; 214,5 К |
| Точка кипения | 121,1 °С; 249,9 ° F; 394,2 К |
| смешивается | |
| Кислотность ( pKa ) | 8.97 |
| Основность (p K b ) | 5.85 |
Показатель преломления ( n D ) | 1,4179 (20 °С) [2] |
| Опасности | |
| СГС Маркировка : | |
   | |
| Опасность | |
| Х225 , Х302 , Х314 , Х332 | |
| П210 , П280 , П305+П351+П338 , П310 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 20 ° C (68 ° F; 293 К) |
| Взрывоопасные пределы | 0.98–9.08% |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза ) |
|
| Родственные соединения | |
Родственные амины | Триэтилентетрамин |
Родственные соединения | |
| Страница дополнительных данных | |
| Тетраметилэтилендиамин (страница данных) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Тетраметилэтилендиамин ( ТМЭДА или ТЕМЕД ) представляет собой химическое соединение формулы (CH 3 ) 2 NCH 2 CH 2 N(CH 3 ) 2 . Этот вид получается из этилендиамина путем замены четырех атомов амина водорода четырьмя метильными группами. Это бесцветная жидкость, хотя старые образцы часто кажутся желтыми. Его запах похож на запах гниющей рыбы. [4]
В качестве реагента в синтезе
[ редактировать ]ТМЭДА широко используется в качестве лиганда ионов металлов. Он образует стабильные комплексы со многими галогенидами металлов, например, с хлоридом цинка и йодидом меди (I) , образуя комплексы, растворимые в органических растворителях. В таких комплексах ТМЕДА служит бидентатным лигандом .
TMEDA имеет сродство к ионам лития . [4] При смешивании с н -бутиллитием атомы азота TMEDA координируются с литием, образуя кластер с более высокой реакционной способностью, чем тетрамер или гексамер, который н обычно принимает -бутиллитий. BuLi/TMEDA способен металлировать или даже дважды металлировать многие субстраты, включая бензол , фуран , тиофен , N - алкилпирролы и ферроцен . [4] Многие анионные металлоорганические комплексы были выделены в виде их [Li(tmeda) 2 ] + комплексы. [5] В таких комплексах [Li(tmeda) 2 ] + ведет себя как соль четвертичного аммония , такая как [NEt 4 ] + .

Аддукт TMEDA бис(триметилсилил)амида лития. Обратите внимание, что диамин является бидентатным лигандом. [6]
втор-бутиллитий /TMEDA представляет собой полезную комбинацию в органическом синтезе, когда аналог н -бутила присоединяется к субстрату. TMEDA в этом случае все еще способна образовывать металлокомплекс с Li, как упоминалось выше.
Другое использование
[ редактировать ]Комплексы (ТМЕДА)Ni(CH 3 ) 2 и [(ТМЕДА)Ni( о -толил)Cl] иллюстрируют использование тмеды для стабилизации гомогенных катализаторов. [7] [8]

Изомеры
[ редактировать ]Тетраметилэтилендиамин также может относиться к 2,3-диметил-2,3-диаминобутану, ЧАС 2 NCMe 2 -CMe 2 NH 2 . [9]
Ссылки
[ редактировать ]- ^ « N , N , N ', N' -тетраметилэтилендиамин – Краткое описание соединений» . Пабхим соединение . США: Национальный центр биотехнологической информации. 16 сентября 2004 года . Проверено 30 июня 2012 г.
- ^ Лиде, Дэвид Р., изд. (2009). Справочник CRC по химии и физике (90-е изд.). Бока-Ратон, Флорида : CRC Press . ISBN 978-1-4200-9084-0 .
- ^ «Паспорт безопасности» (PDF) . [ постоянная мертвая ссылка ]
- ^ Перейти обратно: а б с Хейнс, РК; Фонвиллер, Южная Каролина; Людерер, MR (2006). «N,N,N',N'-тетраметилэтилендиамин». В Пакетте, Л. (ред.). N , N , N ', N' -Тетраметилэтилендиамин . Энциклопедия реагентов для органического синтеза . Нью-Йорк: Дж. Уайли и сыновья. дои : 10.1002/047084289X.rt064.pub2 . ISBN 0471936235 .
- ^ Морс, премьер-министр; Джиролами, GS (1989). "Являются ли 0 Комплексы ML 6 всегда октаэдрические? Рентгеновская структура тригонально-призматического [Li(tmed)] 2 [ZrMe 6 ]». Журнал Американского химического общества . 111 (11): 4114–4116. doi : 10.1021/ja00193a061 .
- ^ Хендерсон, КВ; Дориго, А.Е.; Лю, К.-Л.; Уилльярд, PG (1997). «Влияние полидентатных донорных молекул на агрегацию гексаметилдисилазида лития: рентгенокристаллографическое и комбинированное полуэмпирическое PM3 / одноточечное теоретическое исследование ab Initio». Дж. Ам. хим. Соц . 119 (49): 11855. дои : 10.1021/ja971920t .
- ^ Шилдс, Джейсон Д.; Грей, Эрин Э.; Дойл, Эбигейл Г. (01 мая 2015 г.). «Модульный, устойчивый на воздухе никелевый прекатализатор» . Органические письма . 17 (9): 2166–2169. doi : 10.1021/acs.orglett.5b00766 . ПМЦ 4719147 . ПМИД 25886092 .
- ^ Магано, Хавьер; Монфетт, Себастьян (17 апреля 2015 г.). «Разработка стабильного на воздухе и широко применимого источника никеля для катализируемого никелем кросс-сочетания». АКС-катализ . 5 (5): 3120–3123. дои : 10.1021/acscatal.5b00498 .
- ^ Джексон, В.Грегори; Рахман, А.Ф.Мохлесур; Вонг, М. Энтони (2004). «Обмен растворителем, обмен растворителем, акватация и реакции изомеризации цис- и транс- [Co(tmen) 2 (NCMe) 2 ] 3+ в воде Me 2 SO и MeCN: кинетика и стереохимия». Inorganica Chimica Acta . 357 (3): 665–676. doi : 10.1016/j.ica.2003.05.010 .

