Реакция Цудзи-Троста
Реакция Цуджи-Троста (также называемая аллильным алкилированием Троста или аллильным алкилированием ) представляет собой реакцию палладием катализируемую замещения с участием субстрата, который содержит уходящую группу в аллильном положении. Палладиевый катализатор сначала координируется с аллильной группой, а затем подвергается окислительному присоединению , образуя π -аллильный комплекс. Этот аллильный комплекс затем может быть атакован нуклеофилом , что приводит к образованию замещенного продукта. [ 1 ]

Эту работу впервые предложил Дзиро Цудзи в 1965 году. [ 2 ] и позже адаптирован Барри Тростом в 1973 году с введением фосфиновых лигандов. [ 3 ] Область применения этой реакции была расширена до множества различных нуклеофилов на основе углерода, азота и кислорода, множества различных уходящих групп, множества различных лигандов на основе фосфора, азота и серы, а также множества различных металлов (хотя палладий по-прежнему предпочтителен). [ 4 ] Введение фосфиновых лигандов привело к улучшению реакционной способности и многочисленным стратегиям асимметричного аллильного алкилирования. Многие из этих стратегий обусловлены появлением хиральных лигандов , которые часто способны обеспечивать высокую энантиоселективность и высокую диастереоселективность в мягких условиях. Эта модификация значительно расширяет возможности этой реакции для множества различных синтетических применений. Способность образовывать в этих условиях связи углерод-углерод, углерод-азот и углерод-кислород делает эту реакцию очень привлекательной для областей как медицинской химии, так и синтеза натуральных продуктов.
История
[ редактировать ]В 1962 году Смидт опубликовал работу по катализируемому палладием окислению алкенов до карбонильных групп. В этой работе было установлено, что палладиевый катализатор активирует алкен для нуклеофильной атаки гидроксида . [ 5 ] Получив представление от этой работы, Цудзи предположил, что подобная активация может иметь место для образования углерод-углеродных связей. В 1965 году Цудзи сообщил о работе, подтвердившей его гипотезу. хлорида аллилпалладия Путем взаимодействия димера с натриевой солью диэтилмалоната группа смогла образовать смесь моноалкилированного и диалкилированного продукта. [ 6 ]
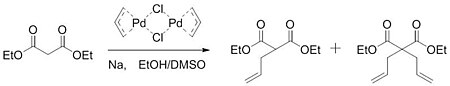
Объем реакции расширялся лишь постепенно, пока Трост не обнаружил следующий большой прорыв в 1973 году. Пытаясь синтезировать гомологи ациклических сесквитерпенов, Трост столкнулся с проблемами с начальной процедурой и не смог алкилировать свои субстраты. Эти проблемы были преодолены добавлением трифенилфосфина в реакционную смесь .

Эти условия затем были проверены на других субстратах, и некоторые из них привели к «практически мгновенной реакции при комнатной температуре». Вскоре после этого он разработал способ использования этих лигандов для асимметричного синтеза. [ 7 ] Неудивительно, что это стимулировало множество других исследований этой реакции и привело к той важной роли, которую эта реакция теперь играет в синтетической химии.
Механизм
[ редактировать ]Начиная с нульвалентной разновидности палладия и субстрата, содержащего уходящую группу в аллильном положении, реакция Цуджи-Троста протекает через каталитический цикл , описанный ниже.

Во-первых, палладий координируется с алкеном, образуя η 2 π -аллил- Pd 0 П комплекс . Следующим шагом является окислительное присоединение , при котором уходящая группа удаляется с инверсией конфигурации и образуется η 3 π -аллил- Pd. II создается (также называемая ионизацией). Затем нуклеофил присоединяется к аллильной группе, регенерируя η 2 π -аллил-Pd. 0 сложный. По завершении реакции палладий отрывается от алкена и может снова начать каталитический цикл . [ 8 ]
«Жесткие» и «мягкие» нуклеофилы
[ редактировать ]Используемые нуклеофилы обычно образуются из предшественников (пронуклеофилов) in situ после их депротонирования основанием. [ 9 ] Эти нуклеофилы затем подразделяются на «жесткие» и «мягкие» нуклеофилы, используя парадигму описания нуклеофилов, которая в значительной степени основана на pKas их сопряженных кислот . «Жесткие» нуклеофилы обычно имеют сопряженные кислоты с pKas более 25, тогда как «мягкие» нуклеофилы обычно имеют сопряженные кислоты с pKas менее 25. [ 10 ] Этот дескриптор важен из-за влияния этих нуклеофилов на стереоселективность продукта. Стабилизированные или «мягкие» нуклеофилы инвертируют стереохимию -аллильного комплекса π . Эта инверсия в сочетании с инверсией стереохимии, связанной с окислительным добавлением палладия, приводит к чистому сохранению стереохимии. С другой стороны, нестабилизированные или «жесткие» нуклеофилы сохраняют стереохимию π -аллильного комплекса, что приводит к чистой инверсии стереохимии. [ 11 ]

Эта тенденция объясняется изучением механизмов нуклеофильной атаки. «Мягкие» нуклеофилы атакуют углерод аллильной группы, а «жесткие» нуклеофилы атакуют металлцентр с последующим восстановительным элиминированием. [ 12 ]
Фосфиновые лиганды
[ редактировать ]Фосфиновые лиганды, такие как трифенилфосфин или лиганд Троста , использовались для значительного расширения области действия реакции Цуджи-Троста. Эти лиганды могут модулировать свойства палладиевого катализатора, такие как стерический объем , а также электронные свойства. Важно отметить, что эти лиганды также могут придавать хиральность конечному продукту, что позволяет проводить эти реакции асимметрично, как показано ниже.
Аллильное асимметричное замещение
[ редактировать ]Энантиоселективная версия реакции Цуджи-Троста называется асимметричным аллильным алкилированием Троста (Трост ААА) или просто асимметричным аллильным алкилированием (ААА). Эти реакции часто используются в асимметричном синтезе. [ 13 ] [ 14 ] [ 15 ] Первоначально реакция была разработана с использованием палладиевого катализатора, поддерживаемого лигандом Троста , хотя с тех пор подходящие условия значительно расширились. Энантиоселективность можно придать реакции на любом из этапов, кроме декомплексообразования палладия из алкена, поскольку стереоцентр уже установлен в этой точке. Были концептуализированы пять основных способов использования этих стадий и создания условий энантиоселективной реакции. Эти методы энантиодискриминации ранее были рассмотрены Тростом:
- Преимущественная ионизация посредством энантиоселективного комплексообразования олефинов.
- Энантиотопическая ионизация уходящих групп
- Атака энантиотопических концов аллильного комплекса.
- Энантиофациальный обмен в π -аллильном комплексе
- Дифференциация прохиральных граней нуклеофила
Предпочтительный метод энантиодискриминации во многом зависит от интересующего субстрата, а в некоторых случаях на энантиоселективность могут влиять некоторые из этих факторов.
Объем
[ редактировать ]Нуклеофилы
[ редактировать ]Сообщалось, что в этой реакции эффективны многие различные нуклеофилы. Некоторые из наиболее распространенных нуклеофилов включают малонаты , еноляты , первичные алкоксиды , карбоксилаты , феноксиды , амины , азиды , сульфонамиды , имиды и сульфоны .
Выход из групп
[ редактировать ]Объем уходящих групп также был расширен за счет включения ряда различных уходящих групп, хотя карбонаты , фенолы , фосфаты , галогениды и карбоксилаты наиболее широко используются .
«Жесткие» и «мягкие» нуклеофилы.
[ редактировать ]Недавние работы показали, что круг «мягких» нуклеофилов можно расширить, включив в него некоторых пронуклеофилов, у которых pKs намного выше ~ 25. Некоторые из этих «мягких» нуклеофилов имеют pKa вплоть до 32, [ 16 ] и было показано, что даже более основные пронуклеофилы (~ 44) действуют как мягкие нуклеофилы с добавлением кислот Льюиса , которые помогают облегчить депротонирование. [ 17 ] Улучшенный диапазон pKa «мягких» нуклеофилов имеет решающее значение, поскольку эти нуклеофилы — единственные, которые были исследованы. [ 18 ] [ 19 ] для энантиоселективных реакций до недавнего времени [ 20 ] (хотя уже давно известны неэнантиоселективные реакции «жестких» нуклеофилов [ 21 ] ). Увеличивая количество пронуклеофилов, которые действуют как «мягкие» нуклеофилы, эти субстраты также можно включать в энантиоселективные реакции с использованием ранее описанных и хорошо изученных методов.
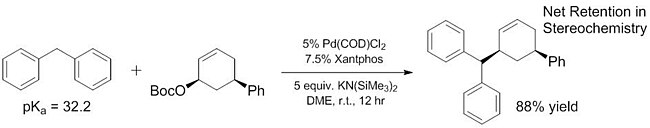
Лиганды
[ редактировать ]Основываясь на реакционной способности трифенилфосфинового лиганда, структура лигандов, используемых в реакции Цуджи-Троста, быстро стала более сложной. Сегодня эти лиганды могут содержать фосфор, серу, азот или некоторую комбинацию этих элементов, но большинство исследований сосредоточено на моно- и дифосфиновых лигандах. Эти лиганды можно дополнительно классифицировать в зависимости от характера их хиральности: некоторые лиганды содержат центральную хиральность атомов фосфора или углерода, некоторые содержат биарильную аксиальную хиральность , а другие содержат плоскую хиральность . Дифосфиновые лиганды с центральной хиральностью стали эффективным типом лигандов (особенно для процедур асимметричного аллильного алкилирования), одним из таких примеров является лиганд Трост. [ 22 ] Лиганды фосфинооксазолинов (PHOX) использовались в ААА, особенно с нуклеофилами на основе углерода. [ 23 ]
Дополнительные подложки
[ редактировать ]Субстрат реакции также был распространен на аллены . В этом специфическом расширении кольца реакция ААА также сопровождается перегруппировкой Вагнера-Меервейна : [ 24 ] [ 25 ]
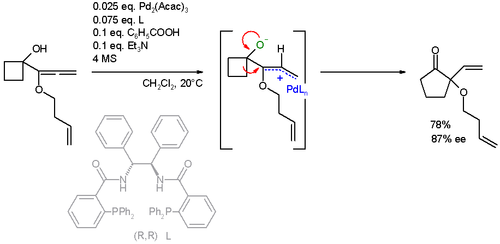
Приложения
[ редактировать ]Синтез фармацевтических/натуральных продуктов
[ редактировать ]Способность энантиоселективно образовывать связи углерод-углерод, углерод-азот и углерод-кислород в мягких условиях делает асимметрическое аллильное алкилирование Троста чрезвычайно привлекательным для синтеза сложных молекул.
Примером этой реакции является синтез промежуточного продукта в совместном общем синтезе галантамина и морфина. [ 26 ] с 1 мол.% [димера хлорида пи-аллилпалладия], 3 мол.% ( S,S ) лиганда Трост и триэтиламина в дихлорметане при комнатной температуре . Эти условия приводят к образованию (-)-энантиомера арилового эфира с химическим выходом 72% и энантиомерным избытком 88% .
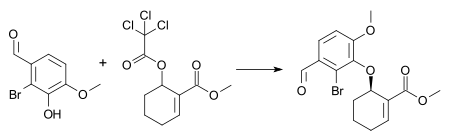
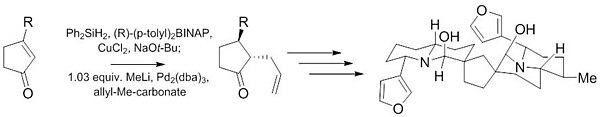
Другая реакция Цуджи-Троста использовалась на начальных этапах синтеза (-)- неотиобинуфаридина . Эта недавняя работа демонстрирует способность этой реакции давать высокодиастереоселективные (10:1) и энантиоселективные (97,5:2,5) продукты из ахирального исходного материала только с небольшим количеством катализатора ( 1% ). [ 27 ]
Обнаружение палладия
[ редактировать ]Помимо практического применения этой реакции в медицинской химии и синтезе натуральных продуктов, в недавних работах реакция Цуджи-Троста также использовалась для обнаружения палладия в различных системах. Эта система обнаружения основана на нефлуоресцентном датчике на основе флуоресцеина (недавно были разработаны более длинноволновые датчики для других применений). [ 28 ] ), который становится флуоресцентным только в присутствии палладия или платины. Эта способность восприятия палладия/платины обусловлена реакцией Цудзи-Троста. Сенсор содержит аллильную группу, а уходящей группой является флуоресцеин. Образуется π - аллильный комплекс, и после атаки нуклеофила высвобождается флуоресцеин, что приводит к резкому увеличению флуоресценции. [ 29 ] [ 30 ]

Этот простой и высокопроизводительный метод обнаружения палладия путем мониторинга флуоресценции оказался полезным для мониторинга уровня палладия в металлических рудах . [ 31 ] фармацевтическая продукция , [ 32 ] и даже в живых клетках . [ 33 ] Учитывая постоянно растущую популярность палладиевого катализа , этот тип быстрого обнаружения должен быть очень полезен для снижения загрязнения фармацевтической продукции и предотвращения загрязнения окружающей среды палладием и платиной.
Ссылки
[ редактировать ]- ^ Стратегическое применение названных реакций в органическом синтезе (мягкая обложка) , Ласло Курти, Барбара Чако ISBN 0-12-429785-4
- ^ Цудзи, Дзиро; Такахаси, Хидэтака; Морикава, Масанобу (1965). «Органические синтезы с помощью соединений благородных металлов XVII. Реакция хлорида π-аллилпалладия с нуклеофилами». Буквы тетраэдра . 6 (49). Эльзевир Б.В.: 4387–4388. дои : 10.1016/s0040-4039(00)71674-1 . ISSN 0040-4039 .
- ^ Трост, Б.М .; Фуллертон, Т.Дж. «Новые синтетические реакции. Аллиловое алкилирование». Дж. Ам. хим. Соц. 1973 , 95 , 292–294. два : 10.1021/ja00782a080 .
- ^ Риос, Ицель Герреро; Росас-Эрнандес, Алонсо; Мартин, Эрика; «Последние достижения в применении хиральных фосфиновых лигандов в Pd-катализируемом асимметричном аллильном алкилировании». Молекулы, 2011, 16 970–1010. дои : 10.3390/molecules16010970
- ^ Смидт Дж., Хафнер В., Джира Р., Зибер Р., Седлмайер Дж. и Сабель А. (1962), Окисление олефинов с помощью катализаторов на основе хлорида палладия . Прикладная химия, 74: 93–102. два : 10.1002/ange.19620740302
- ^ Органические синтезы с помощью соединений благородных металлов XVII. Реакция хлорида π -аллилпалладия с нуклеофилами Tetrahedron Letters , Том 6, Выпуск 49, 1965, страницы 4387–4388 Дзиро Цудзи, Хидетака Такахаши, Масанобу Морикава два : 10.1016/S0040-4039(00)71674-1
- ^ Асимметричное аллильное алкилирование, катализируемое переходными металлами Барри М. Трост Дэвид Л. Ван Вранкен Chem. Ред., 1996, 96 (1), стр. 395–422. два : 10.1021/cr9409804
- ^ Трост, Барри М.; Чжан, Тин; Зибер, Джошуа Д. (2010). «Каталитическое асимметрическое аллильное алкилирование с использованием гетероатомных нуклеофилов: мощный метод образования связи C–X». Химическая наука . 1 (4). Королевское химическое общество (RSC): 427. doi : 10.1039/c0sc00234h . ISSN 2041-6520 .
- ^ Стратегическое применение названных реакций в органическом синтезе (мягкая обложка) , Ласло Курти, Барбара Чако ISBN 0-12-429785-4
- ^ Трост, Барри М.; Тайсривонгс, Дэвид А. (1 октября 2008 г.). «Стратегия использования нестабилизированных нуклеофилов в катализируемых палладием асимметричных аллильных алкилированиях». Журнал Американского химического общества . 130 (43). Американское химическое общество (ACS): 14092–14093. дои : 10.1021/ja806781u . ISSN 0002-7863 . ПМИД 18826305 .
- ^ Лупария, Марко; Оливейра, Мария Тереза; Аудизио, Давиде; Фребо, Фредерик; Годдард, Ричард; Маулид, Нуно (4 ноября 2011 г.). «Каталитическая асимметричная диастереодивергентная дерацемизация». Angewandte Chemie, международное издание . 50 (52). Уайли: 12631–12635. дои : 10.1002/anie.201106321 . ISSN 1433-7851 . ПМИД 22058047 .
- ^ Б. М. Трост, Т. Р. Верховен, Дж. М. Фортунак, Тетраэдр Летт. 1979, 20, 2301 – 2304 гг.
- ^ Трост, Б.М .; Дитч, Т.Дж. «Новые синтетические реакции. Асимметричная индукция при аллильном алкилировании». Дж. Ам. хим. Соц. 1973 , 95 , 8200–8201. два : 10.1021/ja00805a056 .
- ^ Трост, Б.М .; Стреге, Ч.Е. «Асимметричная индукция каталитического аллильного алкилирования». Дж. Ам. хим. Соц. 1977 , 99 , 1649–1651. два : 10.1021/ja00447a064 .
- ^ Асимметричное аллильное алкилирование, катализируемое переходными металлами: применение в полном синтезе Trost, BM; Кроули, ML Chem. Преподобный ; (Обзор); 2003 год ; 103(8); 2921–2944. два : 10.1021/cr020027w
- ^ Ша, Шэн-Чун; Чжан, Цзяди; Кэрролл, Патрик Дж.; Уолш, Патрик Дж.; «Повышение предела pKa «мягких» нуклеофилов в катализируемых палладием аллильных замещениях: применение диарилметановых пронуклеофилов». ДЖАКС. 2013, 135, 17602–17609. дои: 10.1021/ja409511n
- ^ Чжан, Цзяди; Станчу, Корнелиу; Ван, Бэйбэй; Хусейн, Махмуд М.; Да, Чао-Шань; Кэрролл, Патрик Дж.; Дреер, Спенсер Д.; Уолш, Патрик Дж. (29 ноября 2011 г.). «Катализируемое палладием аллильное замещение нуклеофилами на основе (η6-арена – CH2Z)Cr(CO)3» . Журнал Американского химического общества . 133 (50). Американское химическое общество (ACS): 20552–20560. дои : 10.1021/ja208935u . ISSN 0002-7863 . ПМК 3241867 . ПМИД 22047504 .
- ^ Трост, Б.М.; Тосте, Флорида (30 апреля 1999 г.). «Регио- и энантиоселективное аллильное алкилирование несимметричного субстрата: рабочая модель». Журнал Американского химического общества . 121 (19). Американское химическое общество (ACS): 4545–4554. дои : 10.1021/ja9828713 . ISSN 0002-7863 .
- ^ Трост, Барри М.; Мачачек, Мишель Р.; Апоник, Аарон (26 июля 2006 г.). «Прогнозирование стереохимии реакций асимметричного аллильного алкилирования на основе дифенилфосфинобензойной кислоты (DPPBA) на основе палладия: рабочая модель». Отчеты о химических исследованиях . 39 (10). Американское химическое общество (ACS): 747–760. дои : 10.1021/ar040063c . ISSN 0001-4842 . ПМИД 17042475 .
- ^ Ли, Сяо-Хуэй; Чжэн, Бао-Хуэй; Дин, Чан-Хуа; Хоу, Сюэ-Лонг (8 ноября 2013 г.). «Энантиоселективный синтез 2,3-дизамещенных инданонов посредством Pd-катализируемого внутримолекулярного асимметричного аллильного алкилирования кетонов». Органические письма . 15 (23). Американское химическое общество (ACS): 6086–6089. дои : 10.1021/ol402980v . ISSN 1523-7060 . ПМИД 24206052 .
- ^ Кастанье, Ю.; Смолл, Ф. Тетраэдр Летт. 1979, 20, 3221.
- ^ Лу, Жан; Ма, Шэнмин (2008). «Энантиоселективное аллилирование, катализируемое металлами, в асимметричном синтезе» . Angewandte Chemie, международное издание . 47 (2). Уайли: 258–297. дои : 10.1002/anie.200605113 . ISSN 1433-7851 . ПМИД 17968865 .
- ^ Бехенна, Дуглас К.; Штольц, Брайан М. (28 октября 2004 г.). «Энантиоселективное аллилирование Цудзи». Журнал Американского химического общества . 126 (46). Американское химическое общество (ACS): 15044–15045. дои : 10.1021/ja044812x . ISSN 0002-7863 . ПМИД 15547998 .
- ^ Трост, Б.М .; Се, Дж. «Асимметричное расширение кольца алленилциклобутанолов, катализируемое палладием: асимметричный сдвиг Вагнера – Меервейна». Дж. Ам. хим. Соц. 2006 , 128 , 6044–6045. два : 10.1021/ja0602501 .
- ^ Сокатализаторы: бензойная кислота и триэтиламин . Молекулярные сита (МС) предотвращают гидролиз.
- ^ Трост, Б.М .; Тан, В.; Тосте, Ф.Д. «Дивергентный энантиоселективный синтез (-)-галантамина и (-)-морфина». Дж. Ам. хим. Соц. 2005 , 127 , 14785–14803. два : 10.1021/ja054449+ .
- ^ Янсен, Дэниел Дж.; Шенви, Райан А. (11 января 2013 г.). «Синтез (-)-неотиобинуфаридина». Журнал Американского химического общества . 135 (4). Американское химическое общество (ACS): 1209–1212. дои : 10.1021/ja310778t . ISSN 0002-7863 . ПМИД 23298203 .
- ^ Ван, Чжифэй; Чжэн, Шуан; Цай, Джин; Ван, Пэн; Фэн, Цзе; Ян, Ся; Чжан, Лиминг; Джи, Мин; Ву, Фуген; Он, Нонгюэ; Ван, Ненг (20 ноября 2013 г.). «Флуоресцентная искусственная система иммуноферментного анализа на основе нанокатализатора Pd/C и флуоресцентного химиодозиметра». Аналитическая химия . 85 (23). Американское химическое общество (ACS): 11602–11609. дои : 10.1021/ac403001y . ISSN 0003-2700 . ПМИД 24160777 .
- ^ Гарнер, Аманда Л.; Койде, Кадзунори (2009). «Исследование флуорогенного зонда на палладий и платину, ведущее к созданию метода обнаружения, специфичного для палладия». хим. Коммун. (1). Королевское химическое общество (RSC): 86–88. дои : 10.1039/b814197e . ISSN 1359-7345 . ПМИД 19082007 .
- ^ Сун, Фэнлин; Гарнер, Аманда Л.; Койде, Кадзунори (21 сентября 2007 г.). «Высокочувствительный флуоресцентный датчик палладия на основе механизма аллильного окислительного внедрения». Журнал Американского химического общества . 129 (41). Американское химическое общество (ACS): 12354–12355. дои : 10.1021/ja073910q . ISSN 0002-7863 . ПМИД 17887672 .
- ^ Уильямс, Джессика М.; Койде, Кадзунори (18 июня 2013 г.). «Высокопроизводительный метод обнаружения палладия в рудах». Исследования в области промышленной и инженерной химии . 52 (25). Американское химическое общество (ACS): 8612–8615. дои : 10.1021/ie400959z . ISSN 0888-5885 .
- ^ Бу, Сяодун; Койде, Кадзунори; Кардер, Эван Дж.; Уэлч, Кристофер Дж. (28 декабря 2012 г.). «Быстрый анализ остаточного палладия при разработке фармацевтических препаратов с использованием флуорометрического метода на основе катализа». Исследования и разработки органических процессов . 17 (1). Американское химическое общество (ACS): 108–113. дои : 10.1021/op3003008 . ISSN 1083-6160 .
- ^ Чжу, Баокун; Гао, Чжао, Лю, Цайюнь; Вэй, Цинь; Чжан, Сяолин (2011). визуализация палладия в живых клетках». Chemical Communications . 47 (30). Королевское химическое общество (RSC): 8656–8658 doi : / c1cc13215f ISSN 1359-7345 . PMID 21725576 10.1039
Внешние ссылки
[ редактировать ]- Орг. Синтез. 1989, 67, 105
- Орг. Синтез. 2009, 86, 47
- пример реакции цуджи-трост при полном синтезе см.: http://www.biocis.u-psud.fr/IMG/pdf/consized_total_synthesis_of_Minfiensine.pdf, вторую реакцию можно найти на веб-сайте команды biocis: http://www.biocis .u-psud.fr/spip.php?article332