Диастереомер
Эта статья нуждается в дополнительных цитатах для проверки . ( сентябрь 2021 г. ) |
| Диастереомеры, которые также являются эпимерами | |
|---|---|
|
|

|

|
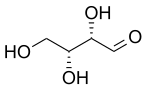
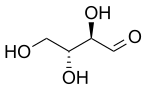
| Д -треоза | D -эритроза |
В стереохимии диастереомеры ) представляют собой (иногда называемые диастереоизомерами разновидность стереоизомеров . [ 1 ] Диастереомеры определяются как незеркальные, неидентичные стереоизомеры. Следовательно, они возникают, когда два или более стереоизомеров соединения имеют разные конфигурации в одном или нескольких (но не во всех) эквивалентных (родственных) стереоцентрах и не являются зеркальными отражениями друг друга. [ 2 ] Когда два диастереоизомера отличаются друг от друга только одним стереоцентром, они являются эпимерами . Каждый стереоцентр дает начало двум различным конфигурациям и, таким образом, обычно увеличивает количество стереоизомеров в два раза.
Диастереомеры отличаются от энантиомеров тем, что последние представляют собой пары стереоизомеров, которые различаются всеми стереоцентрами и, следовательно, являются зеркальными отражениями друг друга. [ 3 ] Энантиомеры соединения с более чем одним стереоцентром также являются диастереомерами других стереоизомеров этого соединения, которые не являются их зеркальным отражением (то есть исключая противоположный энантиомер). Диастереомеры имеют разные физические свойства (в отличие от большинства аспектов энантиомеров) и часто разную химическую активность .
Диастереомеры различаются не только физическими свойствами, но и химической реакционной способностью — тем, как одно соединение реагирует с другими. глюкоза и галактоза Например, являются диастереомерами. Несмотря на то, что они имеют одинаковую молярную массу, глюкоза более стабильна, чем галактоза. Эта разница в стабильности приводит к тому, что галактоза всасывается в организме человека немного быстрее, чем глюкоза. [ 4 ] [ 5 ]
Диастереоселективность — это предпочтение образования одного или нескольких диастереомеров перед другим в органической реакции . В общем, стереоселективность объясняется крутильными и стерическими взаимодействиями в стереоцентре, возникающими в результате электрофилов , приближающихся к стереоцентру. реакции [ 6 ]
Син/анти
[ редактировать ]Когда одинарная связь между двумя центрами может свободно вращаться, цис/транс-дескрипторы становятся недействительными. Двумя широко распространенными префиксами, используемыми для различения диастереомеров по sp3-гибридным связям в молекуле с открытой цепью, являются син и анти . Масамунэ предложил дескрипторы, которые работают, даже если группы не присоединены к соседним атомам углерода. Это также работает независимо от приоритетов CIP . Син описывает группы на одном лице, а анти описывает группы на противоположных лицах. Концепция применима только к проекции Зигзаг. Дескрипторы описывают только относительную стереохимию, а не абсолютную стереохимию. Все изомеры одинаковы.
Эритро/трео
[ редактировать ]Два старых префикса, которые до сих пор широко используются для различения диастереомеров, — это трео и эритро . В случае сахаридов, если их нарисовать в проекции Фишера, эритроизомер имеет два одинаковых заместителя на одной стороне, а трео-изомер - на противоположных сторонах. [ 7 ] Если нарисовать зигзагообразную цепочку, эритроизомер имеет два одинаковых заместителя по разные стороны плоскости (анти). Названия происходят от диастереомерных четырехуглеродных альдоз эритрозы и треозы . Эти префиксы не рекомендуется использовать за пределами сахаридов, поскольку их определения могут привести к противоречивым интерпретациям. [ 8 ]
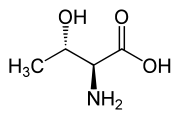
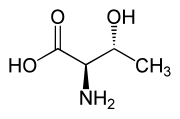
Еще одно треосоединение — треонин , одна из незаменимых аминокислот. Эритродиастереомером его является аллотреонин .
  |
| L -треонин (2S , 3R ) и D -треонин ( 2R , 3S ) |
  |
| L -аллотреонин (2S , 3S ) и D - аллотреонин ( 2R , 3R ) |
Множественные стереоцентры
[ редактировать ]Если молекула содержит два асимметричных центра, существует до четырех возможных конфигураций, и все они не могут быть несуперпозитивными зеркальными отражениями друг друга. Возможности для различных изомеров продолжают увеличиваться по мере того, как к молекуле добавляется больше стереоцентров. В общем случае количество стереоизомеров молекулы можно определить, рассчитав 2 н , где n = количество хиральных центров в молекуле. Это справедливо, за исключением случаев, когда молекула имеет мезоформы . Эти мезосоединения представляют собой молекулы, которые содержат стереоцентры , но обладают внутренней плоскостью симметрии, позволяющей накладывать их на свое зеркальное изображение. Эти эквивалентные конфигурации нельзя считать диастереомерами. [ 9 ]
Для n = 3 имеется восемь стереоизомеров. Среди них четыре пары энантиомеров: R,R,R и S,S,S; Р,Р,С и С,С,Р; Р,С,С и С,Р,Р; и Р,С,Р и С,Р,С. Существует гораздо больше пар диастереомеров, поскольку каждая из этих конфигураций является диастереомером по отношению к любой другой конфигурации, за исключением своего собственного энантиомера (например, R,R,R является диастереомером R,R,S; R,S,R ; и Р,С,С). Для n = 4 существует шестнадцать стереоизомеров или восемь пар энантиомеров. Четыре энантиомерные пары альдопентоз и восемь энантиомерных пар альдогексоз (подмножества пяти- и шестиуглеродных сахаров) являются примерами наборов соединений, которые различаются таким образом.
Диастереомерия по двойной связи
[ редактировать ]Изомеры двойной связи всегда считаются диастереомерами, а не энантиомерами. Диастереомерия также может возникать по двойной связи , где цис- и транс- относительные положения дают заместителей два несуперпозиционных изомера. Многие конформационные изомеры также являются диастереомерами.
В случае диастереомерии, происходящей по двойной связи, EZ используется обозначениях номенклатуры алкенов в , или entgegen и zusammen (нем.) . [ 10 ]
Приложения
[ редактировать ]Как указывалось ранее, два диастереомера не будут иметь одинаковые химические свойства. Эти знания используются в хиральном синтезе для разделения смеси энантиомеров. Это принцип хирального разрешения . После получения диастереомеров их разделяют хроматографией или перекристаллизацией . Отметим также пример стереохимии кетонизации енолов и енолятов .
См. также
[ редактировать ]- Правила приоритета Кана – Ингольда – Прелога для номенклатуры.
Ссылки
[ редактировать ]- ^ "Золотой книги" ИЮПАК. Диастереоизомерия два : 10.1351/goldbook.D01679
- ^ Гарретт, Р.Х.; Гришэм, CM (2005), Биохимия, 3-е изд. , Бельмонт, Калифорния: Томсон, с. 205, ISBN 0-534-41020-0 .
- ^ ИЮПАК "Золотой книги" Энантиомер дои : 10.1351/goldbook.E02069
- ^ Макканс, Роберт Александр; Мэддерс, Кейт (1930). «Сравнительные скорости всасывания сахаров из кишечника человека» . Биохимический журнал . 24 (3): 795–804. дои : 10.1042/bj0240795 . ISSN 0264-6021 . ПМЦ 1254520 . ПМИД 16744419 .
- ^ Чао, Си-Чунь; Маклаки, Скотт А. (06 октября 2020 г.). «Дифференциация и количественная оценка диастереомерных пар гликосфинголипидов с использованием ионной химии газовой фазы» . Аналитическая химия . 92 (19): 13387–13395. дои : 10.1021/acs.analchem.0c02755 . ISSN 0003-2700 . ПМЦ 7544660 . ПМИД 32883073 .
- ^ Лавинда, Ольга; Витт, Коллин Х.; Верпель, Калифорния (28 марта 2022 г.). «Происхождение высокой диастереоселективности в реакциях семичленных енолятов» . Angewandte Chemie International Edition на английском языке . 61 (14): e202114183. дои : 10.1002/anie.202114183 . ISSN 1521-3773 . ПМЦ 8940697 . ПМИД 35076978 .
- ^ Современная физическая органическая химия Эрик В. Анслин, Деннис А. Догерти 2006
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « эритро, трео ». дои : 10.1351/goldbook.E02212
- ^ Мерад, Жереми; Кэнди, Матье; Понс, Жан-Марк; Бресси, Сирил (май 2017 г.). «Каталитическая энантиоселективная десимметризация мезосоединений в полном синтезе натуральных продуктов: на пути к экономии хиральных реагентов» . Синтез . 49 (9): 1938–1954. дои : 10.1055/s-0036-1589493 . ISSN 0039-7881 . S2CID 99010495 .
- ^ Браун, Уильям (2018). Органическая химия (8-е изд.). США: Cengage Learning. стр. 138–142. ISBN 9781305580350 .