β-бутиролактон

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
4-Метилоксетан-2-он | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.019.392 |
| Номер ЕС |
|
| КЕГГ | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
| Число | 1993 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 4 Н 6 О 2 | |
| Молярная масса | 86.090 g·mol −1 |
| Появление | Бесцветная или светло-желтая жидкость [ 1 ] |
| Точка кипения | 71–73 ° C (160–163 ° F; 344–346 К) 39 ч Па [ 2 ] |
| 268 г·л −1 [ 1 ] | |
| Растворимость | Растворим в различных органических растворителях. [ 1 ] |
| Опасности | |
| СГС Маркировка : | |
  
| |
| Предупреждение | |
| Х226 , Х315 , Х319 , Х351 | |
| P201 , P202 , P210 , P233 , P240 , P241 , P242 , P243 , P264 , P280 , P281 , P302+P352 , P303+P361+P353 , P305+P351+P338 , P308+P313 , P321 , P332+P313 , P337+P313 , P362 , P370+P378 , P403+P235 , P405 , P501 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
β-Бутиролактон представляет собой внутримолекулярный эфир карбоновой кислоты ( лактон ) оптически активной 3-гидроксибутановой кислоты . Он образуется в ходе химического синтеза в виде рацемата . β-Бутиролактон пригоден в качестве мономера для производства биоразлагаемого полигидроксиалканоата поли(3-гидроксибутирата) (ПГБ). Полимеризация рацемического ( RS )-β-бутиролактона дает ( RS )-полигидроксимасляную кислоту, которая, однако, уступает по основным свойствам (например, прочности или характеристикам разложения) ( R )-поли-3-гидроксибутирату природного происхождения. [ 3 ]
Производство
[ редактировать ]β-Бутиролактон получают с выходом 63% добавлением этаналя к этенону ( кетену) в присутствии глинистого минерала монтмориллонита . [ 4 ]

также можно получить на месте путем дегидробромирования ацетилбромида Для этой цели этенон основанием Хюнига диизопропилэтиламином . В присутствии хирального комплекса алюминия этенон энантиоселективно реагирует с ( S )-β-бутиролактоном с выходом 92% с энантиомерным избытком ee более 98%. [ 5 ]

Гидрирование дикетена . на палладиевом контактном катализаторе дает β-бутиролактон с выходом 93% [ 6 ]

асимметричное гидрирование дикетена с помощью рутениевого катализатора BINAP до оптически активного ( R )-β-бутиролактона с селективностью 97% и энантиомерным избытком 92%. Описано также [ 7 ]
При 50 °C и ок. Давление CO 60 бар, (R)-2-метилоксиран ( оксид пропилена ) карбонилируется до (R)-β-бутиролактона при сохранении конфигурации с выходом 95%, [ 8 ] если гомогенный катализатор карбонилирования [(сальф)Al(THF) 2 ][Co(CO) 4 ] по Джеффри Коутсу [ 9 ] используется (доступен из модифицированного алюмосаленового комплекса [(сальф)AlCl и тетракарбонилкобальтата натрия NaCo(CO) 4 ]).

Карбонилирование 2- метилоксирана в присутствии гомогенных порфирин-карбонилкобальтатных катализаторов в тетрагидрофуране проходит также при ок. 14 бар монооксида углерода Парциальное давление и дает β-бутиролактон с выходом 97%. [ 10 ]
Из-за проблем с разделением и переработкой гомогенных катализаторов карбонилирования недавно были также исследованы гетерогенные полимерные аналоги, которые обеспечивают столь же высокие выходы (до 96%) при давлении CO 60 бар. Однако эти катализаторы пока не кажутся многообещающими кандидатами для промышленного применения, поскольку они демонстрируют значительно более низкую каталитическую активность в лабораторных партиях с молярной плотностью 50 мм. [ 11 ]
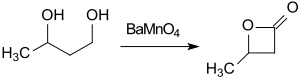
Дешевый исходный бутан-1,3-диол можно превратить с помощью окислителя манганата бария (BaMnO 4 ) в ацетонитриле под воздействием микроволнового излучения в течение 1 часа в β-бутиролактон (выход 74%). [ 12 ]
Характеристики
[ редактировать ]β-Бутиролактон представляет собой прозрачную жидкость с запахом ацетона или мяты. [ 1 ] Он смешивается с водой и растворим во многих органических растворителях. По классификации IARC β-бутиролактон отнесен к группе 2В: «вероятно канцерогенный».
Использовать
[ редактировать ]( R )-β-бутиролактон реагирует в толуоле при температуре ок. Давление CO 14 бар и 55 °C в присутствии саленового комплекса в течение 24 ч с инверсией конфигурации с выходом 94% до оптически чистого (>99% ее) ( S )-метилянтарного ангидрида. [ 13 ]

Гомо- и сополимеры β-бутиролактона
[ редактировать ]Коммерциализация полигидроксимасляной кислоты (ПГБ) или гомо- и сополимеров полигидроксиалканоатов в качестве аэробно-биоразлагаемых термопластов, выделенных из бактерий, под торговой маркой Biopol компании Imperial Chemical Industries (ICI) в 1983 году стала отправной точкой для поиска синтетических альтернатив, которые должны были избежать недостатков ПОБ, таких как хрупкость и жесткость, термическое разложение при температурах чуть выше температуры плавления (175 - 180 °C) и, в частности, неконкурентоспособные затраты. [ 14 ] из-за дорогостоящей ферментации, выделения и очистки.
( Полимеризацией с раскрытием цикла S ) -β-бутиролактона с диэтилцинком ZnEt 2 /водой образуется поли-( S )-3-гидроксибутират с ее > 97% при сохранении конфигурации при хиральном атоме углерода: [ 15 ]
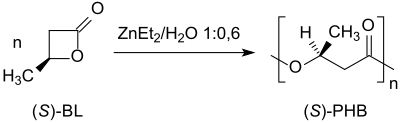
При использовании соединений олова ( дистанноксанов ) в качестве катализаторов полимеризация ( R )-β-бутиролактона также приводит к образованию высокомолекулярных (M n > 100 000) синтетических (R)-полигидроксибутиратов с удерживанием, которые напоминают природные полигидроксиалканоаты. [ 16 ]
Анионная полимеризация оптически активного β-бутиролактона приводит к образованию кристаллических изотактических полигидроксибутиратов при инверсии, низкая полидисперсность которых M w /M n ≈ 1,2 указывает на живую полимеризацию . [ 17 ] [ 18 ]

Также сильные основания, такие как диазабициклоундецен (DBU), 1,5,7-триазабицикло(4.4.0)дек-5-ен (TBD) и фосфазен BEMP, способны катализировать полимеризацию с раскрытием цикла β-бутиролактона в веществе при 60 °C с получением низкомолекулярных ПГБ (M n < 21,000) с узким молекулярно-массовым распределением. [ 19 ]
Катионная полимеризация β-бутиролактона с раскрытием цикла с сильными кислотами, такими как трифторметансульфоновая кислота, приводит к низкомолекулярным ПОБ (M n < 8200) с живыми концами гидроксильных цепей, с которыми, например, капролактона . блоки могут сополимеризоваться [ 20 ]

С помощью иттрия катализаторов на основе рацемический β-бутиролактон можно превратить в (в основном) синдиотактический ПОБ с узким молекулярно-массовым распределением. [ 21 ] [ 22 ]
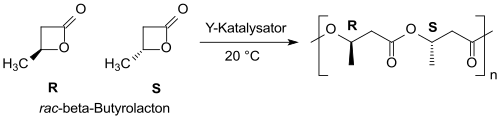
N-гетероциклические карбены (NHC) имидазол-2-илиденового типа являются сильными нуклеофилами и также подходят в качестве инициаторов полимеризации с раскрытием цикла лактонов, таких как β-бутиролактон. [ 23 ]
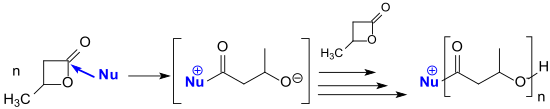
Синтетические варианты ПОБ, разработанные в виде гомополимеров β-бутиролактона или сополимеров с другими лактонами, пока не смогли компенсировать недостатки биогенного материала – в частности, неблагоприятные механические и термические свойства и высокую цену. Вместо этого возникли новые проблемы, связанные с токсичными тяжелыми металлами в катализаторах (например, оловом, кобальтом или хромом) и атактическими полимерными компонентами (жидкими и трудно отделяемыми) с нежелательными свойствами материала. Даже спустя более 30 лет после выхода на рынок экономический успех биополимера Биопол® и его (био)синтетических аналогов все еще остается скромным, несмотря на амбициозные цели по производству (фактические мировые мощности по производству полигидроксиалканоатов в 2018 году: около 30 000 тонн). [ 24 ] ) продажи пока сильно отстают от оптимистичных прогнозов производителей.
Ссылки
[ редактировать ]- ^ Jump up to: а б с д Запись о β-бутиролактоне из TCI Europe, полученная 20 декабря 2018 г.
- ^ Sigma-Aldrich Co. , β-бутиролактон .
- ^ Х. Абэ; И. Мацубара; Ю. Дой; Ю. Хори; А. Ямагучи (1994). «Физические свойства и ферментативная разлагаемость стереоизомеров поли(3-гидроксибутирата) с различной стереорегулярностью». Макромолекулы . 27 (21). стр. 6018–6025. Бибкод : 1994МаМол..27.6018А . дои : 10.1021/ma00099a013 .
- ^ US 2580714 , Ф.Г. Янг, Дж.Т. Фитцпатрик, «Производство лактонов бета-гидроксикарбоновых кислот из кетена и альдегида с использованием глинистого катализатора», выдан 1952-1-1, передан Union Carbide and Carbon Corp.
- ^ С.Г. Нельсон; WS Cheung; Эй Джей Кэссик; М. А. Хилфикер (2002). «Энантиоселективный полный синтез (-)-лаулималида de novo». Дж. Хим. Сок. 124 (46). стр. 13654–13655. дои : 10.1021/ja028019k . ПМИД 12431077 .
- ^ Патент США 2763664 , Дж. Сикст, «Способ производства β-бутиролактона из дикетена», выдан 18 сентября 1956 г., передан компании Wacker-Chemie GmbH.
- ^ Т. Охта; Т. Мияке; Х. Такая (1992). «Эффективный синтез оптически активного 4-метилоксетан-2-она: асимметричное гидрирование дикетена, катализируемое комплексами бинап-рутений (II) [бинап = 2,2'-бис(дифенилфосфино)-1,1'-бинафтил]». Дж. Хим. Соц., хим. Коммун. (23). стр. 1725–1726. дои : 10.1039/C39920001725 .
- ^ ЙДИЛ Гетцлер; В. Махадеван; Е.Б. Лобковский; Г.В. Коутс (2002). «Синтез β-лактонов: высокоактивный и селективный катализатор карбонилирования эпоксидов». Дж. Ам. хим. Соц . 124 (7). стр. 1174–1175. дои : 10.1021/ja017434u . ПМИД 11841278 .
- ^ «Катализаторы карбонилирования» . Олдрич ChemFiles 2007, 7.5, 3 . Сигма Олдрич. 2007 . Проверено 20 декабря 2018 г.
- ^ US 2012123137 , SD Allen, RR Valente, H. Lee, AE Cherian, DL Bunning, NA Clinton, OS Fruchey, BD Dombek, «Процесс производства бета-лактона», выдан 17 мая 2012 г., передан компании Novomer, Inc.
- ^ Дж. Цзян; С. Юн (2018). «Металированный пористый порфириновый полимер с [Co(CO) 4 ] − Анион как эффективный гетерогенный катализатор карбонилирования с расширением кольца» . Scientific Reports . 8 (13243). Стр. 1–6. : 2018NatSR ...813243J . doi : 10.1038/s41598-018-31475-6 . PMC 6125460. Bibcode PMID 30185794 .
- ^ MC Бэгли; З. Лин; диджей Филлипс; А.Э. Грэм (2009). «Манганат бария в реакциях микроволнового окисления: синтез лактонов реакциями окислительной циклизации». Тетраэдр Летт. 50 (49). стр. 6823–6825. дои : 10.1016/j.tetlet.2009.09.117 .
- ^ ЙДИЛ Гетцлер; В. Кунднани; Е.Б. Лобковский; Г.В. Коутс (2004). «Каталитическое карбонилирование β-лактонов до янтарных ангидридов». Дж. Ам. хим. Соц . 126 (22). стр. 6842–6843. дои : 10.1021/ja048946m . ПМИД 15174834 .
- ^ «ICI снижает затраты и увеличивает мощность «Биопола»» . ИКИС. 22 сентября 1991 г. Проверено 20 декабря 2018 г.
- ^ Ю. Чжан; Р.А. Гросс; Р.В. Ленц (1990). «Стереохимия полимеризации с раскрытием цикла ( S )-β-бутиролактона». Макромолекулы . 23 (13). стр. 3206–3212. Бибкод : 1990МаМол..23.3206Z . дои : 10.1021/ma00215a002 .
- ^ Ю. Хори; М. Сузуки; А. Ямагучи; Т. Нисишита (1993). «Полимеризация с раскрытием цикла оптически активного β-бутиролактона с использованием дистанноксановых катализаторов: синтез высокомолекулярного поли(3-гидроксибутирата)». Макромолекулы . 26 (20). стр. 5533–5534. Бибкод : 1993МаМол..26.5533H . дои : 10.1021/ma00072a037 .
- ^ З. Едлинский; П. Курчак (1998). «Первый простой синтез биомиметического поли( R )-3-гидроксибутирата посредством региоселективной анионной полимеризации ( S )-β-бутиролактона». Макромолекулы . 31 (19). стр. 6718–6720. Бибкод : 1998MaMol..31.6718J . дои : 10.1021/ma980663p .
- ^ Р. Курчак; М. Смига; З. Едлински (2002). «Полимеризация β-бутиролактона, инициированная карбоксилатами тетрабутиламмония: новый подход к биомиметическому синтезу полиэфиров» . Дж. Полим. Sci., Часть А: Полим. Хим . 40 (13). стр. 2184–2189. Бибкод : 2002JPoSA..40.2184K . дои : 10.1002/pola.10285 .
- ^ К.Г. Джаффредо; Ж.-Ф. Карпентьер; СМ Гийом (2012). «Контролируемая ОВП β-бутиролактона, просто опосредованная органокатализаторами амидин, гуанидин и фофазен». Макромол. Быстрое общение . 33 (22). стр. 1938–1944. дои : 10.1002/marc.201200410 . ПМИД 22887774 .
- ^ А. Коуффен; Б. Мартин-Вака; Д. Буриссу; К. Наварро (2014). «Селективное раскрытие O-ацильного кольца β-бутиролактона, катализируемое трифторметансульфоновой кислотой: применение для получения четко определенных блок-сополимеров». Полим. хим. 5 (1). стр. 161–168. дои : 10.1039/C3PY00935A .
- ^ А. Амгун; КМ Томас; С. Иллинка; Т. Руанель; Ж.-Ф. Карпентье (2006). «Высокоактивные, продуктивные и синдиоспецифичные иттриевые инициаторы полимеризации рацемического β-бутиролактона» . Энджью. хим. Межд. Эд. 45 (17). стр. 2782–2784. дои : 10.1002/anie.200600058 . ПМИД 16548028 .
- ^ Ж.-Ф. Карпентье (2010). «Дискретные металлические катализаторы для стереоселективной полимеризации с раскрытием цикла хиральных рацемических β-лактонов». Макромол. Быстрая коммуникация. 31 (19). стр. 1696–1705. дои : 10.1002/marc.201000114 . ПМИД 21567583 .
- ^ В. Н. Отту; Х. Сардон; Д. Месеррис; Ж. Виньоль; Д. Татон (2016). «Обновленная информация и проблемы в реакциях органоопосредованной полимеризации» (PDF) . Прогресс в науке о полимерах . 56 . стр. 64–115. doi : 10.1016/j.progpolymsci.2015.12.001 .
- ^ Датирование рынка биопластиков , данные получены 20 декабря 2018 г.