Циклогексенон
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Циклогекс-2-ен-1-он | |||
| Другие имена
1-Циклогекс-2-енон
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| 3DMeet | |||
| 1280477 | |||
| КЭБ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.012.021 | ||
| Номер ЕС |
| ||
| 2792 | |||
| КЕГГ | |||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 6 Н 8 О | |||
| Молярная масса | 96.129 g·mol −1 | ||
| Появление | Прозрачная бесцветная жидкость | ||
| Плотность | 0,993 г/мл [ 1 ] | ||
| Температура плавления | -53 ° C (-63 ° F; 220 К) [ 1 ] | ||
| Точка кипения | От 171 до 173 ° C (от 340 до 343 ° F; от 444 до 446 К) [ 1 ] | ||
| 41,3 г/л (25 °С) | |||
| Опасности | |||
| СГС Маркировка : | |||
  
| |||
| Опасность | |||
| Х226 , Х301 , Х310 , Х319 , Х330 , Х331 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P260 , P261 , P262 , P264 , P270 , P271 , P280 , P284 , P301+P310 , P302+P350 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P311 , P320 , P321 , P322 , P330 , P337+P313 , P361 , P363 , P370+P378 , П403+П233 , П403+П235 , П405 , П501 | |||
| NFPA 704 (огненный алмаз) | |||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза )
|
220 мг кг −1 (крыса, орально) | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Циклогексенон — органическое соединение , которое представляет собой универсальный промежуточный продукт, используемый в синтезе различных химических продуктов, таких как фармацевтические препараты и ароматизаторы. [ 2 ] Это бесцветная жидкость, но коммерческие образцы часто имеют желтый цвет.
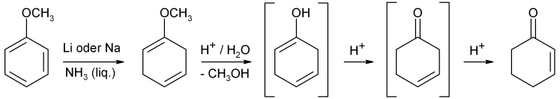
В промышленности циклогексенон получают из фенола восстановлением по Берчу . [ 3 ]
Циклогексенон представляет собой кетон или, точнее, енон . Общие реакции включают присоединение нуклеофильного конъюгата с медьорганическими реагентами , реакции Михаэля и кольца Робинсона . [ 4 ] [ 5 ]
Синтез
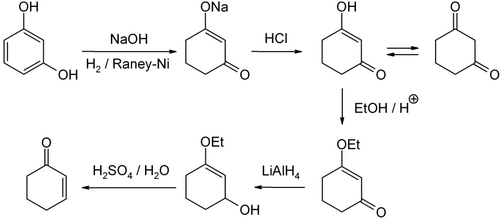
[ редактировать ]Существует несколько маршрутов производства циклогексенона. В лабораторных масштабах его можно получить из резорцина через 1,3-циклогександион. [ 6 ]
Циклогексенон получают Берчу восстановлением анизола по с последующим кислотным гидролизом.
Его можно получить из циклогексанона путем α-бромирования с последующей обработкой основанием. Еще одним путем является гидролиз 3-хлорциклогексена с последующим окислением циклогексенола.
Циклогексенон получают в промышленности путем каталитического окисления циклогексена, например, с помощью перекиси водорода и ванадиевых катализаторов. В нескольких патентах описаны различные окислители и катализаторы.
Реакции
[ редактировать ]Циклогексенон является широко используемым строительным блоком в химии органического синтеза, поскольку он предлагает множество различных способов расширения молекулярных структур.
Как енон , циклогексенон легко адаптируется к присоединению по Михаэлю с нуклеофилами (такими как еноляты или эфиры силиленола) или его можно использовать с помощью реакции Дильса-Альдера , богатыми электронами с диенами . Кроме того, это соединение реагирует с медьорганическими соединениями по 1,4-присоединению (присоединение Михаэля) или с реактивами Гриньяра по 1,2-присоединению, т. е. с атакой нуклеофила по карбонильному атому углерода. Циклогексенон также используется в многостадийном синтезе при создании полициклических натуральных продуктов. Это прохирально.
У сильных оснований позиции 4 и 6 (две СН 2 -группы карбонильной группы и соседняя двойная связь СС) депротонируются.
Циклогексенон является катализатором in vitro относительно мягкого декарбоксилирования альфа -аминокислот . [ 7 ] [ 8 ]
Родственные соединения
[ редактировать ]- циклопропенон
- циклобутенон [ 9 ]
- циклопентенон
- циклогептенон [ 10 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с Циклогексенон в Sigma-Aldrich
- ^ Подразе, KF Org. Подготов. Продолж. Межд. , 1991, 23, с. 217.
- ^ Органические строительные блоки химической промышленности , Гарри Х. Шмант, ISBN 978-0-471-85545-3
- ^ Майкл Г. Орган и Пол Андерсон (1996). «Карбонильные и конъюгатные добавки к циклогексенону: эксперименты, иллюстрирующие селективность реагентов». Журнал химического образования . 73 (12): 1193. doi : 10.1021/ed073p1193 .
- ^ Тетраэдр Летт. 34, 3881, (1993)
- ^ Р.Б. Томпсон (1947). «Дигидрорезорцин». Органические синтезы . 27:21 . дои : 10.15227/orgsyn.027.0021 .
- ^ Исследователи из Японии пытались использовать трет-бутилпероксид в качестве катализатора декарбоксилирования, используя растворитель циклогексанола . Любопытно, что они обнаружили, что когда они использовали циклогексанол более низкой чистоты (например, техническая чистота, 98%), реакция протекала в 4 раза быстрее по сравнению с тем, когда они использовали относительно чистый циклогексанол (>99,3%). Они обнаружили, что циклогексанол содержит циклогексенон в качестве естественной примеси, которого в циклогексеноне технического качества в три раза больше, чем в более очищенном циклогексаноле (~0,3% против ~0,1%). Дальнейшие исследования показали, что 1% циклогексенон в циклогексаноле декарбоксилирует большинство альфа-аминокислот, в том числе нестандартные, с выходом 80-95% в течение нескольких часов. Исключением являются некоторые аминокислоты, такие как гистидин , на который, как сообщается, требуется более 26 часов, и полиаминокислоты, которые не могут декарбоксилироваться с использованием 2-циклогексенона, и вместо этого необходимо найти другой путь. Хасимото, М; Эда, Ю; Ясутомо, О; Тошиаки, я; Аоки, С (1986). «Новое декарбоксилирование АЛЬФА-аминокислот. Простой метод декарбоксилирования с использованием 2-циклогексен-1-она в качестве катализатора» . Химические письма . 15 (6): 893–896. дои : 10.1246/кл.1986.893 . Проверено 4 января 2016 г.
- ^ Лаваль, Г; Голдинг, Б. (2003). «Однопоточная последовательность декарбоксилирования α-аминокислот» . Синлетт (4): 542–546. дои : 10.1055/s-2003-37512 . Проверено 4 января 2016 г.
- ^ А.Г. Росс, К. Ли, С.Дж. Данишефский (2012). «Приготовление циклобутенона» . Органические синтезы . 89 : 491. дои : 10.15227/orgsyn.089.0491 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Ю. Ито, С. Фуджи, М. Накатуска, Ф. Кавамото, Т. Саэгуса (1979). «Расширение одноуглеродного кольца циклоалканонов до сопряженных циклоалкенонов: 2-циклогептен-1-один». Органические синтезы . 59 : 113. дои : 10.15227/orgsyn.059.0113 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )