Свободнорадикальная теория старения
Эта статья нуждается в более надежных медицинских ссылках для проверки или слишком сильно полагается на первоисточники . ( май 2015 г. ) |  |
Свободнорадикальная теория старения утверждает, что организмы стареют , потому что клетки свободными радикалами . со временем накапливают повреждения, вызванные [1] Свободный радикал – это любой атом или молекула, имеющая один неспаренный электрон во внешней оболочке. [2] Хотя некоторые свободные радикалы, такие как меланин, не являются химически активными , большинство биологически значимых свободных радикалов обладают высокой реакционной способностью. [3] Для большинства биологических структур повреждение свободными радикалами тесно связано с окислительным повреждением. Антиоксиданты являются восстановителями и ограничивают окислительное повреждение биологических структур, пассивируя их от свободных радикалов. [4]
Строго говоря, теория свободных радикалов касается только свободных радикалов, таких как супероксид ( O 2 − ), но с тех пор оно было расширено и теперь включает окислительное повреждение от других активных форм кислорода (АФК), таких как перекись водорода (H 2 O 2 ) или пероксинитрит (OONO − ). [4]
Денэм Харман впервые предложил свободнорадикальную теорию старения в 1950-х годах. [5] а в 1970-х годах расширили идею, включив в нее митохондриальное производство АФК. [6]
У некоторых модельных организмов, таких как дрожжи и дрозофилы , есть доказательства того, что уменьшение окислительного повреждения может продлить продолжительность жизни. [7] Однако у мышей только одно из 18 генетических изменений (делеция SOD-1), которые блокируют антиоксидантную защиту, сокращает продолжительность жизни. [8] у круглых червей ( Caenorhabditis elegans ) блокирование выработки природного антиоксиданта супероксиддисмутазы Аналогично, было показано, что увеличивает продолжительность жизни. [9] Достаточно ли снижения окислительного повреждения ниже нормального уровня для продления жизни, остается открытым и спорным вопросом.
Фон
[ редактировать ]Свободнорадикальная теория старения была предложена Денэмом Харманом в 1950-х годах, когда преобладающее научное мнение считало, что свободные радикалы слишком нестабильны, чтобы существовать в биологических системах. [10] Это было еще до того, как кто-то назвал свободные радикалы причиной дегенеративных заболеваний. [11] Два источника вдохновили Хармана: 1) теория скорости жизни , которая утверждает, что продолжительность жизни является обратной функцией скорости метаболизма, которая, в свою очередь, пропорциональна потреблению кислорода, и 2) Ребеки Гершман наблюдение о том, что гипербарическая кислородная токсичность и радиационная токсичность могут быть объясняется тем же основным явлением: свободными радикалами кислорода. [10] [12] Отметив, что радиация вызывает «мутацию, рак и старение», Харман утверждал, что свободные радикалы кислорода, образующиеся при нормальном дыхании, вызывают кумулятивный ущерб, который в конечном итоге приведет к потере функциональности организма и, в конечном итоге, к смерти. [10] [12]
В последующие годы теория свободных радикалов была расширена и теперь включает не только старение как таковое , но и возрастные заболевания. [11] Повреждение клеток свободными радикалами связано с рядом заболеваний, включая рак , артрит , атеросклероз , болезнь Альцгеймера и диабет . [13] Имеются некоторые доказательства того, что свободные радикалы и некоторые активные формы азота запускают и усиливают механизмы гибели клеток в организме, такие как апоптоз и, в крайних случаях, некроз . [14]
В 1972 году Харман модифицировал свою первоначальную теорию. [11] В своей нынешней форме эта теория предполагает, что активные формы кислорода (АФК), которые производятся в митохондриях , вызывают повреждение определенных макромолекул, включая липиды , белки и, что наиболее важно, митохондриальную ДНК. [15] Это повреждение затем вызывает мутации, которые приводят к увеличению производства АФК и значительно усиливают накопление свободных радикалов внутри клеток. [15] Эта митохондриальная теория получила более широкое признание и утверждает, что она может играть важную роль в процессе старения. [16]
С тех пор, как Харман впервые предложил свободнорадикальную теорию старения, его первоначальная теория постоянно модифицировалась и расширялась. [16]
Процессы
[ редактировать ]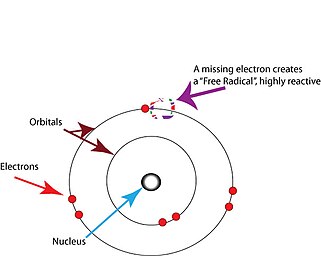
Свободные радикалы — это атомы или молекулы, содержащие неспаренные электроны. [2] Электроны обычно существуют парами на определенных орбиталях в атомах или молекулах. [17] Свободные радикалы, которые содержат только один электрон на любой орбитали, обычно нестабильны по отношению к потере или захвату дополнительного электрона, поэтому все электроны в атоме или молекуле будут спарены. [17]
Неспаренный электрон не подразумевает заряда; Свободные радикалы могут быть положительно заряженными, отрицательно заряженными или нейтральными.
Повреждение происходит, когда свободный радикал сталкивается с другой молекулой и пытается найти другой электрон, чтобы спарить свой неспаренный электрон. Свободный радикал часто отрывает электрон от соседней молекулы, в результате чего пораженная молекула сама становится свободным радикалом. Затем новый свободный радикал может оторвать электрон от следующей молекулы, и происходит химическая цепная реакция образования радикалов. [18] Свободные радикалы, образующиеся в таких реакциях, часто прекращают свое действие, удаляя электрон из молекулы, которая изменяется или не может функционировать без него, особенно в биологии. Такое событие вызывает повреждение молекулы и, следовательно, клетки, которая ее содержит (поскольку молекула часто становится дисфункциональной).
Цепная реакция, вызванная свободными радикалами, может привести к сшиванию атомных структур. В тех случаях, когда цепная реакция, вызванная свободными радикалами, затрагивает молекулы пар оснований в цепи ДНК, ДНК может стать сшитой. [19]
Окислительные свободные радикалы, такие как гидроксильный радикал и супероксидный радикал, могут вызывать повреждения ДНК , и предполагается, что такие повреждения играют ключевую роль в старении важнейших тканей. [20] Повреждение ДНК может привести к снижению экспрессии генов , гибели клеток и, в конечном итоге, к дисфункции тканей. [20]
Сшивка ДНК, в свою очередь, может привести к различным последствиям старения, особенно к раку . [21] могут возникать и другие перекрестные связи Между молекулами жира и белка , что приводит к образованию морщин. [22] Свободные радикалы могут окислять ЛПНП , и это ключевой момент в образовании бляшек в артериях, что приводит к болезням сердца и инсульту . [23] Это примеры того, как свободнорадикальная теория старения использовалась для аккуратного «объяснения» происхождения многих хронических заболеваний . [24]
Свободные радикалы, которые, как считается, участвуют в процессе старения, включают супероксид и оксид азота . [25] В частности, увеличение количества супероксида влияет на старение, тогда как снижение образования оксида азота или его биодоступности влияет на то же самое. [25]
Антиоксиданты полезны в уменьшении и предотвращении повреждений, вызванных свободнорадикальными реакциями, поскольку они способны отдавать электроны, которые нейтрализуют радикал, не образуя другого. Витамин С , например, может отдать электрон свободному радикалу и сам оставаться стабильным, передавая свой нестабильный электрон вокруг молекулы антиоксиданта. [ нужна ссылка ]
Модификации теории
[ редактировать ]Одна из основных критических замечаний в адрес свободнорадикальной теории старения направлена на предположение, что свободные радикалы ответственны за повреждение биомолекул и , таким образом, являются основной причиной клеточного старения и старения организма. [26] : 81 Было предложено несколько модификаций для интеграции текущих исследований в общую теорию.
Митохондрии
[ редактировать ]
Митохондриальная теория старения была впервые предложена в 1978 году. [27] [28] а два года спустя была представлена митохондриальная свободнорадикальная теория старения. [29] Теория предполагает, что митохондрии являются основной мишенью радикального повреждения, поскольку существует известный химический механизм, с помощью которого митохондрии могут производить АФК, митохондриальные компоненты, такие как мтДНК, не так хорошо защищены, как ядерная ДНК, а исследования, сравнивающие повреждение ядра и мтДНК, которые демонстрируют более высокие уровни радикального повреждения молекул митохондрий. [30] Электроны могут ускользать из метаболических процессов в митохондриях, таких как цепь переноса электронов , и эти электроны, в свою очередь, могут реагировать с водой с образованием АФК, таких как супероксидный радикал , или косвенным путем - гидроксильный радикал . Эти радикалы затем повреждают ДНК и белки митохондрий, а эти повреждающие компоненты, в свою очередь, более склонны к образованию побочных продуктов АФК. Таким образом петля положительной обратной связи окислительного стресса, которая со временем может привести к ухудшению состояния клеток, а затем органов и всего тела. устанавливается [26]
Эта теория широко обсуждалась [31] и до сих пор неясно, как развиваются мутации мтДНК, индуцированные АФК. [26] Конте и др. предполагают, что железозамещенные цинковые пальцы могут генерировать свободные радикалы из-за близости цинковых пальцев к ДНК и, таким образом, приводить к повреждению ДНК. [32]
Афанасьев предполагает, что активность CuZnSOD по супероксидной дисмутации демонстрирует важную связь между продолжительностью жизни и свободными радикалами. [33] Связь между CuZnSOD и продолжительностью жизни была продемонстрирована Perez et al. которые указали, что на продолжительность жизни мышей повлияла делеция гена Sod1, который кодирует CuZnSOD. [34]
Вопреки обычно наблюдаемой связи между митохондриальными АФК (мтАФК) и снижением продолжительности жизни, Yee et al. недавно наблюдалось увеличение продолжительности жизни, опосредованное передачей сигналов mtROS по пути апоптоза. Это подтверждает возможность того, что наблюдаемые корреляции между повреждением АФК и старением не обязательно указывают на причинное участие АФК в процессе старения, а, скорее, связаны с их модуляцией путей передачи сигналов, которые являются частью клеточных ответов на процесс старения. [35]
Эпигенетический окислительный окислительно-восстановительный сдвиг
[ редактировать ]Брюэр предложил теорию, которая объединяет свободнорадикальную теорию старения с сигнальными эффектами инсулина при старении. [36] Теория Брюэра предполагает, что «сидячий образ жизни, связанный с возрастом, вызывает окисленный окислительно-восстановительный сдвиг и нарушение функции митохондрий». [36] Это митохондриальное нарушение приводит к более малоподвижному поведению и ускорению старения. [36]
Метаболическая стабильность
[ редактировать ]Теория метаболической стабильности старения предполагает, что именно способность клеток поддерживать стабильную концентрацию АФК является основным фактором, определяющим продолжительность жизни. [37] Эта теория критикует теорию свободных радикалов, поскольку она игнорирует тот факт, что АФК представляют собой специфические сигнальные молекулы, необходимые для поддержания нормальных функций клеток. [37]
Митогормезис
[ редактировать ]Окислительный стресс может увеличить продолжительность жизни Caenorhabditis elegans , вызывая вторичную реакцию на первоначально повышенный уровень АФК. [38] У млекопитающих вопрос о суммарном влиянии активных форм кислорода на старение еще менее ясен. [39] [40] [41] Недавние эпидемиологические данные подтверждают процесс митогормезиса у людей и даже предполагают, что прием экзогенных антиоксидантов может увеличить распространенность заболеваний у людей (согласно теории, поскольку они предотвращают стимуляцию естественного ответа организма на окислительные соединения, которые не только нейтрализуют их, но дает и другие преимущества). [42]
Проблемы
[ редактировать ]Птицы
[ редактировать ]Среди птиц попугаи живут примерно в пять раз дольше, чем перепела . Было обнаружено, что выработка АФК в сердце, скелетных мышцах, печени и интактных эритроцитах одинакова у попугаев и перепелов и не обнаруживает соответствия с разницей в продолжительности жизни. [43] Было сделано заключение, что эти результаты ставят под сомнение надежность теории старения, основанной на окислительном стрессе. [43]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Хекими С., Лапуант Дж., Вэнь Ю. «Хороший» взгляд на свободные радикалы в процессе старения. Тенденции в клеточной биологии. 2011;21(10) 569-76.
- ^ Перейти обратно: а б Эрбас М., Секерчи Х. «Важность свободных радикалов, возникающих во время обработки пищевых продуктов». Serbest Radïkallerïn Onemï Ve Gida Ïsleme Sirasinda Olusumu. 2011: 36(6) 349–56.
- ^ Херрлинг Т., Юнг К., Фукс Дж. (2008). «Роль меланина как защитника от свободных радикалов в коже и его роль индикатора свободных радикалов в волосах». Spectrochimica Acta Часть A: Молекулярная и биомолекулярная спектроскопия . 69 (5): 1429–35. Бибкод : 2008AcSpA..69.1429H . дои : 10.1016/j.saa.2007.09.030 . ПМИД 17988942 .
- ^ Перейти обратно: а б Холливелл Б. (2012). «Свободные радикалы и антиоксиданты: обновление личного взгляда» . Обзоры питания . 70 (5): 257–65. дои : 10.1111/j.1753-4887.2012.00476.x . ПМИД 22537212 .
- ^ Харман, Д. (1956). «Старение: теория, основанная на свободнорадикальной и радиационной химии». Журнал геронтологии . 11 (3): 298–300. дои : 10.1093/geronj/11.3.298 . hdl : 2027/mdp.39015086547422 . ПМИД 13332224 .
- ^ Харман, Д. (1972). «Биологические часы: митохондрии?». Журнал Американского гериатрического общества . 20 (4): 145–147. дои : 10.1111/j.1532-5415.1972.tb00787.x . ПМИД 5016631 . S2CID 396830 .
- ^ Фонтана, Луиджи; Партридж, Линда; Лонго, Вальтер Д. (16 апреля 2010 г.). «Продление продолжительности здоровой жизни — от дрожжей к человеку» . Наука . 328 (5976): 321–326. Бибкод : 2010Sci...328..321F . дои : 10.1126/science.1172539 . ПМЦ 3607354 . ПМИД 20395504 .
- ^ Перес В.И., Боков А., Реммен Х.В., Меле Дж., Ран К., Икено Ю. и др. (2009). «Является ли теория старения окислительного стресса мертвой?» . Biochimica et Biophysical Acta (BBA) – Общие предметы . 1790 (10): 1005–14. дои : 10.1016/j.bbagen.2009.06.003 . ПМЦ 2789432 . ПМИД 19524016 .
- ^ Ван Раммсдонк, Джереми М.; Хекими, Зигфрид (2009). Ким, Стюарт К. (ред.). «Удаление митохондриальной супероксиддисмутазы sod-2 продлевает продолжительность жизни Caenorhabditis elegans » . ПЛОС Генетика . 5 (2): e1000361. дои : 10.1371/journal.pgen.1000361 . ПМЦ 2628729 . ПМИД 19197346 .
- ^ Перейти обратно: а б с Харман Д. (июль 1956 г.). «Старение: теория, основанная на свободнорадикальной и радиационной химии». Дж. Геронтол . 11 (3): 298–300. дои : 10.1093/geronj/11.3.298 . hdl : 2027/mdp.39015086547422 . ПМИД 13332224 .
- ^ Перейти обратно: а б с Харман Д. (2009). «Происхождение и эволюция свободнорадикальной теории старения: краткая личная история, 1954–2009». Биогеронтология . 10 (6): 773–81. дои : 10.1007/s10522-009-9234-2 . ПМИД 19466577 . S2CID 13512659 .
- ^ Перейти обратно: а б Спикмен-младший, Селман С. (2011). «Теория повреждения свободными радикалами: накопление доказательств против простой связи окислительного стресса со старением и продолжительностью жизни». Биоэссе . 33 (4): 255–9. doi : 10.1002/bies.201000132 . ПМИД 21290398 . S2CID 13720843 .
- ^ Клэнси Д., Бердсолл Дж. Мухи, черви и свободнорадикальная теория старения. Обзоры исследований старения. (0).
- ^ Чаттерджи С., Лардинуа О., Бхаттачарджи С., Такер Дж., Корбетт Дж., Детердинг Л. и др. (2011). «Окислительный стресс индуцирует образование радикалов белка и ДНК в фолликулярных дендритных клетках зародышевого центра и модулирует структуру гибели клеток при позднем сепсисе» . Свободнорадикальная биология и медицина . 50 (8): 988–99. doi : 10.1016/j.freeradbiomed.2010.12.037 . ПМК 3051032 . ПМИД 21215311 .
- ^ Перейти обратно: а б Джанг Ю.К., Реммен Х.В. (2009). «Митохондриальная теория старения: данные моделей трансгенных и нокаутных мышей». Экспериментальная геронтология . 44 (4): 256–60. дои : 10.1016/j.exger.2008.12.006 . ПМИД 19171187 . S2CID 19815246 .
- ^ Перейти обратно: а б Грубер Дж., Шаффер С., Холливелл Б. (2008). «Митохондриальная свободнорадикальная теория старения – где мы находимся?» . Границы бионауки . 13 (13): 6554–79. дои : 10.2741/3174 . ПМИД 18508680 .
- ^ Перейти обратно: а б Орчин М., Макомбер Р.С., Пинхас А., Уилсон Р.М., редакторы. Словарь и понятия органической химии. 2-е изд.: Джон Уайли и сыновья; 2005.
- ^ Цуй Ханг; Конг Яхуэй; Чжан Хун (2011). «Окислительный стресс, митохондриальная дисфункция и старение» . Журнал передачи сигналов . 2012 : 646354. doi : 10.1155/2012/646354 . ПМК 3184498 . ПМИД 21977319 .
- ^ Крин С., Геацинтов Н.Е., Шафирович В. (2008). «Внутрицепочечные ГУ-поперечные связи, образующиеся в результате окисления гуанина в 5'-d(GCU) и 5'-r(GCU)» . Свободнорадикальная биология и медицина . 45 (8): 1125–34. doi : 10.1016/j.freeradbiomed.2008.07.008 . ПМЦ 2577587 . ПМИД 18692567 .
- ^ Перейти обратно: а б Генслер Х.Л., Холл Дж.Дж. и Бернштейн Х. (1987). Гипотеза старения о повреждении ДНК: важность окислительного повреждения. В «Обзоре биологических исследований старения». Том. 3 (М. Ротштейн, ред.), стр. 451–465. Алан Р. Лисс, Нью-Йорк
- ^ Диздароглу М., Яруга П. Механизмы повреждения ДНК, вызванного свободными радикалами. Свободные радикальные исследования. [Статья]. 2012;46(4) 382–419.
- ^ Пейджон Х., Асселино Д. Подход in vitro к хронологическому старению кожи путем гликирования коллагена: биологическое воздействие гликирования на реконструированную модель кожи» Анналы Нью-Йоркской академии наук 2005; 1043 (1) 529- 32.
- ^ Бамм В.В., Цемахович В.А., Шаклай Н. Окисление липопротеинов низкой плотности гемоглобином-гемихромом. Международный журнал биохимии и клеточной биологии. 2003;35(3) 349-58.
- ^ К. Рихтер, Дж. В. Парк, Б. Н. Эймс «Обычное окислительное повреждение митохондриальной и ядерной ДНК обширно» «PNAS», 1988.
- ^ Перейти обратно: а б Афанасьев И.Б. (2005). «Свободнорадикальные механизмы процессов старения в физиологических условиях». Биогеронтология . 6 (4): 283–90. дои : 10.1007/s10522-005-2626-z . ПМИД 16333762 . S2CID 7661778 .
- ^ Перейти обратно: а б с Афанасьев I (2010). «Сигнальные и повреждающие функции свободных радикалов в теории старения, гормезисе и TOR» . Старение и болезни . 1 (2): 75–88. ПМК 3295029 . ПМИД 22396858 .
- ^ Lobachev A.N. Роль митохондриальных процессов в развитии и старении организма. Старение и рак (PDF) , Рефераты по химии. 1979 т. 91 N 25 91:208561т. Депонируется док., ВИНИТИ 2172-78, 1978, с. 48
- ^ Lobachev A.N. Биогенез митохондрий при клеточной дифференцировке и старении (PDF) , депонированный Doc. ВИНИТИ 19.09.85, №6756-В85, 1985, с. 28
- ^ Микель Дж., Economos AC, Флеминг Дж. и др. Роль митохондрий в клеточном старении , Exp Gerontol, 15, 1980, стр. 575–591.
- ^ Вайндрух, Ричард (январь 1996 г.). «Ограничение калорий и старение». Научный Американ : 49–52.
- ^ Пуватингал С.К., Грубер Дж., Холливелл Б., Гунаван Р. (2009). «Стохастический дрейф точечных мутаций митохондриальной ДНК: новая перспектива ex silico» . PLOS Вычислительная биология . 5 (11): e1000572. Бибкод : 2009PLSCB...5E0572P . дои : 10.1371/journal.pcbi.1000572 . ПМЦ 2771766 . ПМИД 19936024 .
- ^ Конте Д., Нариндрасорасак С., Саркар Б. (1996). « in vivo и in vitro Железозамененный цинковый палец генерирует свободные радикалы и вызывает повреждение ДНК» . Журнал биологической химии . 271 (9): 5125–30. дои : 10.1074/jbc.271.9.5125 . ПМИД 8617792 .
- ^ Афанасьев И. Сигнальные и повреждающие функции свободных радикалов в теории старения, гормезисе и TOR. Старение и болезни. 2010;1(2) 75–88.
- ^ Перес В.И., Боков А., Ван Реммен Х., Меле Дж., Ран К., Икено Ю. и др. (2009). «Является ли теория старения окислительного стресса мертвой?» . Biochimica et Biophysical Acta (BBA) – Общие предметы . 1790 (10): 1005–14. дои : 10.1016/j.bbagen.2009.06.003 . ПМЦ 2789432 . ПМИД 19524016 .
- ^ Йи С., Ян В., Хекими С. (2014). «Внутренний путь апоптоза опосредует реакцию продления жизни на митохондриальные АФК у C. elegans» . Клетка . 157 (4): 897–909. дои : 10.1016/j.cell.2014.02.055 . ПМЦ 4454526 . ПМИД 24813612 .
- ^ Перейти обратно: а б с Брюэр Дж.Дж. (2010). «Теория старения эпигенетического окислительно-восстановительного сдвига (EORS) объединяет теории передачи сигналов свободных радикалов и инсулина» . Экспериментальная геронтология . 45 (3): 173–9. дои : 10.1016/j.exger.2009.11.007 . ПМК 2826600 . ПМИД 19945522 .
- ^ Перейти обратно: а б Бринк Т.С., Деметриус Л., Лерах Х., Аджай Дж. (2009). «Возрастные транскрипционные изменения в экспрессии генов в различных органах мышей подтверждают теорию метаболической стабильности старения» . Биогеронтология . 10 (5): 549–64. дои : 10.1007/s10522-008-9197-8 . ПМК 2730443 . ПМИД 19031007 .
- ^ Шульц Т.Дж., Зарс К., Фойгт А., Урбан Н., Бирринджер М., Ристоу М. (2007). «Ограничение глюкозы продлевает продолжительность жизни Caenorhabditis elegans, индуцируя митохондриальное дыхание и усиливая окислительный стресс» . Клеточный метаболизм . 6 (4): 280–93. дои : 10.1016/j.cmet.2007.08.011 . ПМИД 17908557 .
- ^ Сохал Р., Мокетт Р., Орр В. (2002). «Механизмы старения: оценка гипотезы окислительного стресса». Свободный Радик Биол Мед . 33 (5): 575–86. дои : 10.1016/S0891-5849(02)00886-9 . ПМИД 12208343 .
- ^ Сохал Р. (2002). «Роль окислительного стресса и окисления белков в процессе старения». Свободный Радик Биол Мед . 33 (1): 37–44. дои : 10.1016/S0891-5849(02)00856-0 . ПМИД 12086680 .
- ^ Ротанг С (2006). «Теории биологического старения: гены, белки и свободные радикалы». Свободный радикал Res . 40 (12): 1230–8. дои : 10.1080/10715760600911303 . ПМИД 17090411 . S2CID 11125090 .
- ^ Белакович Г., Николова Д., Глууд Л.Л., Симонетти Р.Г., Глууд С. (2007). «Смертность в рандомизированных исследованиях антиоксидантных добавок для первичной и вторичной профилактики: систематический обзор и метаанализ». Журнал Американской медицинской ассоциации . 297 (8): 842–57. дои : 10.1001/jama.297.8.842 . ПМИД 17327526 . .
- ^ Перейти обратно: а б Монтгомери М.К., Халберт А.Дж., Баттемер В.А. (2012). «Объясняет ли теория старения окислительного стресса различия в продолжительности жизни у птиц? I. Производство митохондриальных АФК». Эксп. Геронтол . 47 (3): 203–10. дои : 10.1016/j.exger.2011.11.006 . ПМИД 22123429 . S2CID 984298 .