Lutetium ( 177 Лу) Озодотрит
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Lutathera |
| AHFS / Drugs.com | Монография |
| Данные лицензии | |
| Маршруты администрация | Внутривенно |
| Класс наркотиков | соматостатина Аналог |
| Код ATC | |
| Юридический статус | |
| Юридический статус | |
| Идентификаторы | |
| Номер CAS | |
| PubChem CID | |
| Наркоман | |
| НЕКОТОРЫЙ | |
| Кегг | |
| Comptox Dashboard ( EPA ) | |
| Химические и физические данные | |
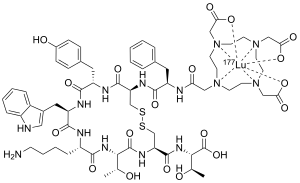
| Формула | C 65 H 87 LU N 14 O 19 S 2 |
| Молярная масса | 1 607 .58 g·mol −1 |
| 3D model ( JSmol ) | |
Lutetium ( 177 Лу) оксодотроотид ( гостиница ) или 177 Lu Dotatate бренда Lutatera , является хелатированным комплексом радиоизотопа название элемента , Lutetium с дотататом , используемым в терапии радионуклидом пептидного рецептора . В частности, он используется при лечении раковых заболеваний , которые экспрессируют рецепторы соматостатина . [ 5 ] Это аналог соматостатина. [ 3 ] [ 6 ] [ 7 ]
Альтернативы 177 Lu-Dotatate включает в себя yttrium-90 Dotatate или Dotatoc . Более длительный диапазон бета -частиц, испускаемых 90 Y, который обеспечивает терапевтический эффект, может сделать его более подходящим для больших опухолей с 177 Лу зарезервирован для меньших объемов [ 8 ] [ 9 ]
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) рассматривает 177 Лу дотатат является первым в своем классе лекарства . [ 10 ]
Медицинское использование
[ редактировать ]В США, 177 Дотатат LU показан для лечения соматостатиновых рецептор-позитивных гастроэнтеропанкреатических нейроэндокринных опухолей (GEP-сети), включая опухоли с надписью, средней кишкой и нейроэндокринной нейроэндокрины у взрослых. [ 3 ] [ 6 ] [ 7 ]
В футболе, Lutetium ( 177 LU) оксодотротид показан для лечения неоперабельной или метастатической, прогрессирующей, хорошо дифференцированной (G1 и G2), рецептора соматостатина, положительного гастроэнтеропанкреатического нейроэндокринных опухолей (GEP-сети) у взрослых. [ 4 ]
Неблагоприятные эффекты
[ редактировать ]Терапевтический эффект 177 Лу вытекает из ионизирующего бета -излучения , которую он излучает, однако это также может быть вредным для здоровых тканей и органов. Почки особенно подвержены риску , так как они помогают удалить 177 Лу дотатат из тела. [ 11 ] Чтобы защитить их, раствор аминокислот ( аргинин/лизин ) вводится медленной инфузией , начиная с радиоактивного введения и обычно продолжая в течение нескольких часов после этого. [ 9 ] [ 12 ] [ 13 ]
История
[ редактировать ]Европейская комиссия одобрила Lutetium ( 177 Lu) oxodotreotide (название бренда Lutathera) «Для лечения неоперабельного или метастатического, прогрессирующего, хорошо дифференцированного (G1 и G2), рецептора соматостатина, положительных гастроэнтеропанкреатических нейроэндокринных опухолей (GEP-сети) у взрослых» в сентябре 2017 года. [ 14 ] [ 4 ]
177 Lu Dotatate был одобрен в Соединенных Штатах для лечения SSTR-положительных гастроэнтеропанкреатических нейроэндокринных опухолей (GEP-сети), включая вырегирование, среднюю кишку и нейроэндокринные опухоли у взрослых в январе 2018 года. [ 3 ] [ 6 ] [ 7 ] Это был первый раз, когда был одобрен радиофармацевтическим препаратом для лечения GEP-сети в Соединенных Штатах. [ 6 ]
США Управление Управления по санитарному надзору за продуктами и лекарствами (FDA) 177 Lu Dotatate основан, главным образом, на доказательствах одного клинического исследования, Netter-1 из 229 участников с положительными сети соматостатина-рецептор в средней кишке GEP. [ 15 ] У зачисленных участников были опухоли, которые не могли быть удалены хирургически и ухудшались при получении лечения октреотидом. [ 15 ]
Участники были случайным образом назначены для получения любого 177 Лутатат с октреотидом длительного действия или октреотида длительного действия, в одном только более высокой дозе. [ 15 ] 177 Lu Dotatate вводили через вену, а октреотид длительного действия вводили в мышцу. [ 15 ] И участники, и поставщики медицинских услуг знали, какое лечение было проведено. [ 15 ] Преимущество 177 Lu Dotatate оценивали путем измерения продолжительности времени, когда опухоли не растут после лечения, и сравнивали его с контрольной группой (выживаемость без прогрессирования). [ 15 ]
FDA рассмотрел дополнительные данные из второго исследования, основанного на данных от 1214 участников с рецепторными рецепторными опухолями соматостатина, в том числе GEP-сети, которые получили 177 Лу дотатат на одном месте в Нидерландах, Erasmus MC . [ 6 ] [ 15 ] Все участники получили 177 Лу дотатат с октреотидом. [ 15 ] Участники и поставщики медицинских услуг знали, какое лечение было дано. [ 15 ] Преимущество 177 Lu Dotatate оценивали путем измерения, если и сколько размер опухоли изменился во время лечения (общая частота ответа). [ 15 ] Полная или частичная усадка опухоли была зарегистрирована в 16 процентах от подмножества из 360 участников с GEP-сетьями, которые были оценены для ответа FDA. [ 6 ] Участники первоначально зарегистрировались в полученном исследовании 177 Лу дотатат как часть расширенной программы доступа. [ 6 ]
FDA подало заявление на 177 Lu Dotatate Priority Review и обозначения лекарств для сирот . [ 6 ] FDA предоставило одобрение Lutathera для усовершенствованных заявок на ускоритель . [ 6 ]
В апреле 2024 года FDA одобрило 177 Lu Dotatate для лечения детей в возрасте 12 лет и старше соматостатиновой рецептор-положительной (SSTR)-позитивных гастроэнтеропанкреатических нейроэндокринных опухолей (GEP-сети), включая опухоли нейроэндокрин-нейроэндокрина. [ 16 ] [ 17 ] Он был утвержден для взрослых в 2018 году. [ 16 ] Это первое одобрение FDA радиоактивного препарата или радиофармацевтического препарата для детей в возрасте двенадцатилетнего возраста и старше SSTR-позитивных гастроэнтеропанкреатических нейроэндокринных опухолей. [ 16 ]
Одобрение детей в возрасте 12 лет и старше было основано на данных фармакокинетических, дозиметрии и безопасности от Netter-P (NCT04711135), непрерывного международного, многоцентрового, открытого, одноручного исследования Lutetium Lu 177 Dotatatate в подростках. с локально продвинутыми/неоперабельными или метастатическими SSTR-позитивными гастроэнтеропанкреатическими нейроэндокринными опухолями или феохромоцитомой/параганглиомой. [ 16 ] Одобрение было также основано на экстраполяции результатов эффективности, наблюдаемых в Netter-1 (NCT01578239), рандомизированном многоцентровом, открытом январе, активном контролируемом исследовании у 229 участников с локально продвинутыми/необратимыми или метастатическими SSTR-положительными карциноидами, которые локально развитые/необратимые или метастатические SSTR-положительные CAPCINOID, которые локально развитые или метастатические SSTR-положительные CARCINOID, которые локально усовершенствован Поддержал первоначальное одобрение Lutetium Lu 177 Dotatate у взрослых. [ 16 ]
Безопасность была оценена у девяти педиатрических участников в Netter-P, в том числе четырех участников с гастроэнтеропанкреатическими нейроэндокринными опухолями. [ 16 ] Основными показателями исхода были поглощенные дозы радиации в органах -мишенях и частота побочных реакций после первого цикла лечения. [ 16 ] Дополнительные показатели результата включали кратковременные побочные реакции после лечения Lutetium Lu 177 Dotatate. [ 16 ] Побочный профиль реакции, наблюдаемый в Netter-P, был аналогичен тем, что наблюдается у взрослых. [ 16 ]
Ссылки
[ редактировать ]- ^ «Сводная основа решения (SBD) для Lutathera» . Здравоохранение Канада . 23 октября 2014 года. Архивировано с оригинала 31 мая 2022 года . Получено 29 мая 2022 года .
- ^ «Lutathera 370 MBQ/мл Решение для инфузии - Сводка характеристик продукта (SMPC)» . (EMC) . Архивировано из оригинала 9 июля 2021 года . Получено 9 июля 2021 года .
- ^ Jump up to: а беременный в дюймовый «Lutathera-Lutetium lu 177 Dotatate Incement» . Йиляйм . 4 мая 2020 года. Архивировано с оригинала 16 ноября 2020 года . Получено 8 ноября 2020 года .
- ^ Jump up to: а беременный в "Lutathera Epar" . Европейское агентство по лекарственным средствам (EMA) . 17 сентября 2018 года. Архивировано с оригинала 11 декабря 2019 года . Получено 11 декабря 2019 года .
- ^ Wang L, Tang K, Zhang Q, Li H, Wen Z, Zhang H, et al. (2013). «Молекулярная визуализация на основе соматостатина на основе рецептора и терапия нейроэндокринных опухолей» . Biomed Research International . 2013 : 102819. DOI : 10.1155/2013/102819 . PMC 3784148 . PMID 24106690 .
- ^ Jump up to: а беременный в дюймовый и фон глин час я «FDA одобряет новую обработку для определенных раков пищеварительного тракта» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс -релиз). 26 января 2018 года. Архивировано с оригинала 11 декабря 2019 года . Получено 11 декабря 2019 года .
 Эта статья включает текст из этого источника, который находится в общественном доступе .
Эта статья включает текст из этого источника, который находится в общественном доступе .
- ^ Jump up to: а беременный в «FDA одобряет Lutetium lu 177 Dotatate для лечения GEP-сети» . США Управление по контролю за продуктами и лекарствами (FDA) (пресс -релиз). 26 января 2018 года. Архивировано с оригинала 11 декабря 2019 года . Получено 11 декабря 2019 года .
 Эта статья включает текст из этого источника, который находится в общественном доступе .
Эта статья включает текст из этого источника, который находится в общественном доступе .
- ^ Radage JK, Ahmed A, Ardill J, Bax N, Breen DJ, Caplin ME, et al. (Январь 2012 г.). «Руководство по лечению гастроэнтеропанкреатических нейроэндокринных (включая карциноидные) опухоли (NETS)» . Кишечник 61 (1): 6–32. doi : 10.1136/gutjnl-2011-300831 . PMC 3280861 . PMID 22052063 .
- ^ Jump up to: а беременный Bodei L, Mueller-Brand J, Baum RP, Pavel ME, Hörsch D, O'Dorisio MS, et al. (Май 2013). «Практическое практическое руководство в суставах МАГАТЭ, EANM и SNMMI по радионуклидной терапии пептидного рецептора (PRRNT) в нейроэндокринных опухолях» . Европейский журнал ядерной медицины и молекулярной визуализации . 40 (5): 800–16. doi : 10.1007/s00259-012-2330-6 . PMC 3622744 . PMID 23389427 .
- ^ Новая лекарственная терапия утверждает 2018 (PDF) . США Управление по контролю за продуктами и лекарствами (FDA) (отчет). Январь 2019 года. Архивировано с оригинала 17 сентября 2020 года . Получено 16 сентября 2020 года .
- ^ Томпсон Л (7 февраля 2019 г.). «Значение раствора аминокислот с Lutetium lu 177 Dotatate» . Онкологический консультант медсестры . Архивировано из оригинала 17 октября 2021 года . Получено 2 ноября 2020 года .
- ^ "Lysakare Epar" . Европейское агентство по лекарственным средствам (EMA) . 24 мая 2019 года. Архивировано с оригинала 23 июля 2020 года . Получено 22 июля 2020 года .
- ^ Volterrani D, Erba PA, Carrió I, Strauss HW, Mariani G (10 августа 2019 г.). Учебник по ядерной медицине: методология и клинические применения . Спрингер. п. 782. ISBN 978-3-319-95564-3 Полем Архивировано из оригинала 10 января 2023 года . Получено 7 ноября 2020 года .
- ^ «Европейское одобрение Lutetium oxodotreotide для гастроэнтеропанкреатических нейроэндокринных (GEP-Net) опухолей» . ecanser.org . 3 октября 2017 года. Архивировано с оригинала 3 апреля 2018 года . Получено 2 апреля 2018 года .
- ^ Jump up to: а беременный в дюймовый и фон глин час я Дж «Снимок на наркотики: Lutathera» . США Управление по контролю за продуктами и лекарствами (FDA) . 20 февраля 2018 года. Архивировано с оригинала 11 декабря 2019 года . Получено 11 декабря 2019 года .
 Эта статья включает текст из этого источника, который находится в общественном доступе .
Эта статья включает текст из этого источника, который находится в общественном доступе .
- ^ Jump up to: а беременный в дюймовый и фон глин час я «FDA одобряет Lutetium Lu 177 Dotatate для педиатрических пациентов 12 лет» . Управление по контролю за продуктами и лекарствами США . 23 апреля 2024 года. Архивировано с оригинала 25 апреля 2024 года . Получено 25 апреля 2024 года .
 Эта статья включает текст из этого источника, который находится в общественном доступе .
Эта статья включает текст из этого источника, который находится в общественном доступе .
- ^ «Novartis получает одобрение FDA для Lutathera в педиатрическом лечении» . Marketscreener . 23 апреля 2024 года. Архивировано с оригинала 23 апреля 2024 года . Получено 23 апреля 2024 года .