Метаболизм фенилпропаноидов
Биосинтез фенилпропаноидов себя включает в ряд ферментов.
От аминокислот до корицы
[ редактировать ]У растений все фенилпропаноиды получены из аминокислот фенилаланина и тирозина .
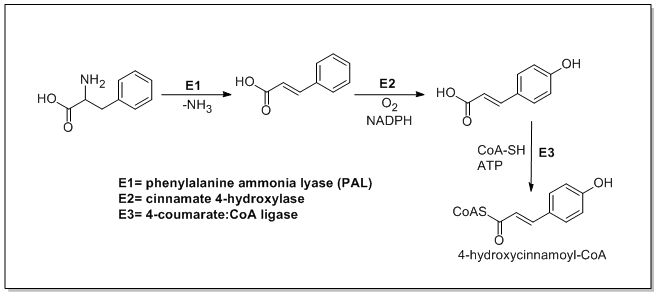
Фенилаланин аммиак-линиаза (PAL, ака фенилаланин/тирозин-аммиак-лиаза) представляет собой фермент, который трансформирует L- фенилаланин и тирозин в транстонной кислоту и P -кумарную кислоту , соответственно.
Транс-циннамат 4-монооксигеназа (4-гидроксилаза Cinnamate) представляет собой фермент, который транс-циннамат транс-циннамат в 4-гидроксициннамат ( P -кумарная кислота). 4-комарат-коа-лигаза -это фермент, который трансформирует 4-комарат ( P -кумарную кислоту) в 4-кумароил-CoA . [ 1 ]
Enzymes associated with biosynthesis of hydroxycinnamic acids
[edit]- Cinnamyl-alcohol dehydrogenase (CAD), an enzyme that transforms cinnamyl alcohol into cinnamaldehyde
- Sinapine esterase, an enzyme that transforms sinapoylcholine into sinapate (sinapic acid) and choline
- Trans-cinnamate 2-monooxygenase, an enzyme that transforms trans-cinnamate (cinnamic acid) into 2-hydroxycinnamate
- Caffeate O-methyltransferase, an enzyme that transforms caffeic acid into ferulic acid
- Caffeoyl-CoA O-methyltransferase, an enzyme that transforms caffeoyl-CoA into feruloyl-CoA
- 5-O-(4-coumaroyl)-D-quinate 3'-monooxygenase, an enzyme that transforms trans-5-O-(4-coumaroyl)-D-quinate into trans-5-O-caffeoyl-D-quinate
- Sinapoylglucose—choline O-sinapoyltransferase, an enzyme that transforms 1-O-sinapoyl-beta-D-glucose into sinapoylcholine (sinapine)
- Sinapoylglucose—malate O-sinapoyltransferase, an enzyme that transforms 1-O-sinapoyl-beta-D-glucose into sinapoyl-(S)-malate
- Cinnamoyl-CoA reductase, an enzyme that transforms cinnamoyl-CoA from cinnamaldehyde
Conjugation enzymes
[edit]These enzymes conjugate phenylpropanoids to other molecules.
- 2-coumarate O-beta-glucosyltransferase, the enzyme that transforms trans-2-hydroxycinnamate into trans-beta-D-glucosyl-2-hydroxycinnamate
- Hydroxycinnamate 4-beta-glucosyltransferase, the enzyme that transforms p-coumaric acid into 4-O-beta-D-glucosyl-4-hydroxycinnamate
- Shikimate O-hydroxycinnamoyltransferase, the enzyme that transforms 4-coumaroyl-CoA into 4-coumaroylshikimate
- Quinate O-hydroxycinnamoyltransferase, the enzyme that transforms feruloyl-CoA into O-feruloylquinate
- Sinapate 1-glucosyltransferase, the enzyme that transforms sinapate (sinapic acid) into 1-sinapoyl-D-glucose
- Coniferyl-alcohol glucosyltransferase, the enzyme that transforms coniferyl alcohol into coniferin
Deconjugation enzymes
[edit]- Coniferin beta-glucosidase, in the glucosidase that transforms coniferin into coniferol
Стильбеноиды биосинтез
[ редактировать ]- Пинозилвин-синтаза , фермент, который трансформирует пинозилвин из Cinnamoyl-CoA
- Тригидроксистильбена синтаза , фермент, который трансформирует 4-кумароил-Коа в ресвератрол .
Альтернативный путь бактериальной кетосинтазы, направленный на биосинтез , существует в Photorhabdus бактериальных симбионтах нематод гетерорхабдита , вызывая 3,5-дигидрокси-4-изопропил-транс-стильбена для антибиотических целей. [ 2 ]
Бимарины Биосинтез
[ редактировать ]- Скополетин глюкозилтрансфераза , фермент, который трансформирует скополину в скополин
Биосинтез халконов
[ редактировать ]4-Coumaroyl-CoA можно объединить с малонило-CoA , чтобы получить истинную основу флавоноидов, группы соединений, называемых халконаидами , которые содержат два фенильных кольца. Нарингенин-хальконе синтаза -это фермент, который катализирует следующее преобразование:
- 3-малонил-коа + 4-кумароил-коа → 4 CoA + naringenin chalcone + 3 co 2
Флавоноиды биосинтез
[ редактировать ]Конъюгатное кольцо халконов приводит к знакомой форме флавоноидов , трехкратной структуры флавона .
Биодеградация
[ редактировать ]Деградация гидроксициннамических кислот
[ редактировать ]- 3,4-диоксигеназа Caffeate -это фермент, в котором используются 3,4-дигидрокси-транс-циннамат ( кофеиновая кислота ) и кислород для получения 3- (2-карбоксиэтенил) -цис, цис-муконат .
Ссылки
[ редактировать ]- ^ Ververidis Filippos, F.; Trantas Emmanouil; Дуглас Карл; Воллмер Гуэнтер; Крецшмар Георг; Panopoulos Nickolas (октябрь 2007 г.). «Биотехнология флавоноидов и других фенилпропаноидных натуральных продуктов. Часть I: химическое разнообразие, влияние на биологию растений и здоровье человека». Биотехнологический журнал . 2 (10): 1214–34. doi : 10.1002/biot.200700084 . PMID 17935117 .
- ^ Joyce SA, Brachmann AO, Glazer I, Lango L, Schwär G, Clarke DJ, Bode HB (2008). «Бактериальный биосинтез мультипотентного стилбена». Angew Chem Int Ed Engl . 47 (10): 1942–5. Citeseerx 10.1.1.603.247 . doi : 10.1002/anie.200705148 . PMID 18236486 .