Фенестран
Фенестран , в органической химии — тип химического соединения с центральным четвертичным атомом углерода который служит общей вершиной для четырех конденсированных карбоциклов . [1] Их можно рассматривать как спиросоединения вдвойне. Из-за присущей им деформации и нестабильности фенестраны представляют теоретический интерес для химиков. Название предложено в 1972 году Власиосом Джорджином и Мартином Зальцманом. [2] — происходит от латинского слова «окно» , fenestra . Джорджиан имел в виду, что «фенестран» относится исключительно к [4.4.4.4] фенестрану, скелетная структура которого похожа на окна, а Кеннет Б. Виберг назвал эту конкретную структуру «оконным стеклом». [3] С тех пор термин фенестран стал обобщенным и стал относиться ко всему классу молекул, которые имеют кольца других размеров. Грузинская компания рекомендовала для этого сорта розеттан , основываясь на структурном виде розетки цветов . [3]
Номенклатура и структура
[ редактировать ]

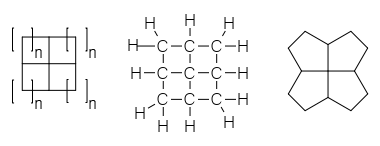
Структуры этого класса химических веществ могут быть названы в соответствии с числом атомов в каждом кольце в дополнение к систематической номенклатуре ИЮПАК правил наименования . Наименьшим членом семейства, состоящим из четырех конденсированных циклопропановых колец, является [3.3.3.3]фенестран, который имеет систематическое название тетрацикло[2.1.0.0]. 1,3 .0 2,5 ]пентан, его еще называют пирамиданом. Следующий симметричный член, [4.4.4.4]фенестран, имеет четыре конденсированных циклобутановых кольца и имеет систематическое название тетрацикло[3.3.1.0]. 3,9 .0 7,9 ]нонан. Кольца не обязательно должны быть одинакового размера, поэтому [4.4.4.5]фенестран имеет три циклобутановых кольца и одно циклопентановое кольцо. Другие структурные модификации меняют название, как обычно в систематической номенклатуре, поэтому [4.6.4.6] фенестрадиен имеет два циклобутановых кольца и два циклогексановых кольца в чередующемся порядке и два алкеновых звена в кольцевой структуре.

Помимо размеров колец, фенестраны могут иметь различные комбинации цис- и транс-геометрии при каждом слиянии колец. Эти детали обозначаются префиксами « c » и « t » к названию структуры, перечисленными в том же порядке, что и размеры колец. [4] Например, c , t , c , c- [4.5.5.5]фенестран имеет транс-конфигурацию в одном из слияний циклопентан/циклопентан, но цис-конфигурацию в другом слиянии циклопентан/циклопентан и в обоих слияниях бутанпентан/циклопентан.
В крайнем случае [ нужны разъяснения ] центральный атом углерода, который обычно имеет тетраэдрическую молекулярную геометрию для своих четырех связей, полностью сплющивается. В картине молекулярных орбиталей полученной квадратно-плоской геометрии метана два из трех sp 2 -гибридизированные орбитали атомов углерода образуют регулярные связи с двумя атомами водорода, как в плоском алкене . Третий сп 2 орбиталь взаимодействует в трехцентровой двухэлектронной связи с двумя оставшимися атомами водорода, используя только электроны водорода. Два дополнительных валентных электрона углерода расположены на ап-орбитали, перпендикулярной плоскости молекулы. Четыре связи C–H равны из-за резонанса . Расчеты in silico показывают, что для этого процесса требуется от 95 до 250 ккал/моль (от 400 до 1050 кДж/моль). [ нужна ссылка ]
Одним из наиболее напряженных фенестранов, которые были выделены, является [4.4.4.5] фенестран с валентными углами при центральном атоме углерода около 130 ° (по данным рентгеновской кристаллографии ) по сравнению со стандартом 109,45 ° для тетраэдрических атомов. . Длины связей углерод-углерод также отличаются от таковых у обычных алканов. В то время как связь C–C в этане составляет 155 пм, в этом фенестране связи, идущие от центрального атома углерода, укорачиваются до 149 пм , а по периметру удлиняются до 159 пм. [5]
Дитерпен содержащий под названием лауренен, кольцевую систему [5.5.5.7]фенестрана, был первым открытым природным фенестраном. [6] [7] Первым когда-либо синтезированным фенестраном был [4.5.5.6] фенестран: [2] [8]
Пирамиды
[ редактировать ]Пирамидан ([3.3.3.3]фенестран) представляет собой наименьший возможный фенестран и никогда не синтезировался. Если бы центральный углерод был тетраэдрическим, он имел бы форму спипентадиена , но с дополнительными связями между двумя циклопропильными кольцами, а не с двойными связями внутри них. Аналогичные герма- и станнапирамиданы с триметилсилильными группами, связанными с углами, , Ge[C 4 (SiMe 3 ) 4 ] и Sn[C 4 (SiMe 3 ) 4 ] были синтезированы. с другой стороны [9] Они принимают квадратную пирамидальную геометрию, аналогичную тригональной пирамиде тетраэдрана , с атомом германия или олова в вершине. Этот атом имеет геометрию перевернутого тетраэдра . Согласно анализу ядерного магнитного резонанса , четыре атома углерода основания пирамиды ведут себя как ароматическое кольцо .
Синтетические подходы
[ редактировать ]В одном исследовании был синтезирован [4.5.5.5]фенестран с одним атомом углерода, замененным на азот, поскольку аза -соединения и их соли с большей вероятностью образуют кристаллические соединения, пригодные для рентгеноструктурного анализа, чем низкомолекулярные алканы. [4] На этапе 1 алкилгалогенид 1-йод-3-бутен 1 превращается в цианоцинковый иодида цианидом меди ) , купрат 2 (путем трансметаллирования цинкорганического который на следующем этапе реагирует с 1-нитроциклопентеном 3 в результате нуклеофильного присоединения, в результате чего образуется нитронат. 4 захватывается фенилселененилбромидом до промежуточного селена 5 . перекисью водорода окислении При 5 образуется нитроалкен 6 в виде смеси син- и анти- изомеров . [4+2] -циклоприсоединение с н- бутиленола эфиром в присутствии триметилалюминия дает нитронат 7 присутствии карбоната калия дает нитрозоацеталь , а второе [3+2]-циклоприсоединение при нагревании в 8 . Гидрирование никелем Ренея дает диол 9 , который в результате двойной реакции Мицунобу (с донором аминных протонов) дает азафенестран 10 в виде борановой соли.

В борановой N–C–C соли валентный угол составляет 126°.
В одном исследовании описана необычная 8π дисротаторно -6π каскадная электроциклическая реакция , направленная на минимизацию количества стадий, необходимых для синтеза фенестрана. [10] [11]

См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Венепалли, Бхаскар Рао; Агоста, Уильям К. (1987). «Фенестраны и уплощение тетраэдрического углерода». хим. Откр. 87 (2): 399–410. дои : 10.1021/cr00078a007 .
- ^ Jump up to: а б Грузинский, Власиос; Зальцман, Мартин (1972). «Синтез, направленный на насыщенный «плоский» углерод». Буквы тетраэдра . 13 (42): 4315–4317. дои : 10.1016/S0040-4039(01)94304-7 .
- ^ Jump up to: а б Никон, Алекс; Сильверсмит, Эрнест Ф. (2013). Органическая химия: игра в имена: современные термины и их происхождение . Эльзевир. стр. 55–56. ISBN 9781483145235 .
- ^ Jump up to: а б Дания, Скотт Э .; Монтгомери, Джастин И.; Крампс, Лауренц А. (2006). «Синтез, рентгеновская кристаллография и компьютерный анализ 1-азафенестранов». Дж. Ам. хим. Соц. 128 (35): 11620–11630. дои : 10.1021/ja0632759 .
- ^ Рао, В. Бхаскар; Джордж, Клиффорд Ф.; Вольф, Стивен; Агоста, Уильям К. (1 октября 1985 г.). «Синтетические и структурные исследования ряда [4.4.4.5] фенестрана». Журнал Американского химического общества . 107 (20): 5732–5739. дои : 10.1021/ja00306a022 .
- ^ Будур, Айша; Шарпене, Мелани; Блондинка, Гаэль; Сюферт, Жан (2 декабря 2013 г.). «Фенестраны в синтезе: уникальные и очень вдохновляющие основы». Angewandte Chemie, международное издание . 52 (49): 12786–12798. дои : 10.1002/anie.201304555 .
- ^ Корбетт, Р. Эдвард; Лорен, Денис Р.; Ткачи, Рекс Т. (1979). «Структура лауренена, нового дитерпена из эфирного масла Dacrydium cupressinum. Часть 1». Журнал Химического общества, Perkin Transactions 1 : 1774. doi : 10.1039/P19790001774 .
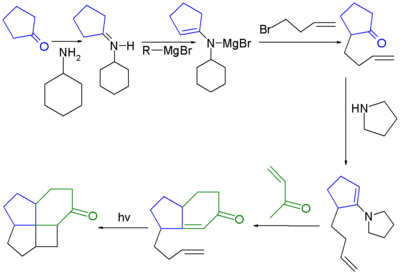
- ^ Первым шагом в этой последовательности реакций является адаптация енаминного алкилирования Сторка, взаимодействует в ходе которого циклопентанон с 3-бром-1-бутеном через производное имина с пирролидином и образуется магниевая соль с этилмагнийбромидом . Следующим шагом является обычная енаминовая реакция Сторка с последующей альдольной конденсацией с образованием циклогексенонового кольца. Заключительный этап — фотолитическое [2+2] циклоприсоединение .
- ^ Lee, Vladimir Ya.; Ito, Yuki; Sekiguchi, Akira; Gornitzka, Heinz; Gapurenko, Olga A.; Minkin, Vladimir I.; Minyaev, Ruslan M. (2013). "Pyramidanes". J. Am. Chem. Soc . 135 (24): 8794–8797. doi : 10.1021/ja403173e .
- ^ Юло, К.; Блондин, Г.; Сафферт, Дж. (2008). «Синтез [4.6.4.6] фенестрадиенов и [4.6.4.6] фенестренов на основе каскада 8π-6π-циклизации-окисления». Дж. Ам. хим. Соц. 130 (15): 5046–5047. дои : 10.1021/ja800691c .
- ^ Реагенты: P-2 Ni (Ni(OAc) 2 ·4H 2 O) / газообразный водород. Реакция, инициируемая органическим восстановлением алкина . в алкен