Винилацетат
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Этенилацетат | |
| Систематическое название ИЮПАК Этенил этаноат | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol ) | |
| 1209327 | |
| КЭБ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.003.224 |
| Номер ЕС |
|
| КЕГГ | |
| МеШ | C011566 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
| Число | 1301 |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 4 Н 6 О 2 | |
| Молярная масса | 86.090 g·mol −1 |
| Появление | Бесцветная жидкость |
| Запах | Сладкий, приятный, фруктовый; может быть резким и раздражающим [1] |
| Плотность | 0,934 г/см 3 |
| Температура плавления | -93,5 ° C (-136,3 ° F; 179,7 К) |
| Точка кипения | 72,7 ° C (162,9 ° F; 345,8 К) |
| −46.4 × 10 −6 см 3 /моль | |
| Опасности | |
| СГС Маркировка : | |
   | |
| Опасность | |
| Х225 , Х332 , Х335 , Х351 | |
| P201 , P202 , P210 , P233 , P240 , P241 , P242 , P243 , P261 , P271 , P280 , P281 , P303+P361+P353 , P304+P312 , P304+P340 , P308+P313 , , 12 П370 +П378 , П403+ П233 , П403+П235 , П405 , П501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | −8 ° C (18 ° F; 265 К) |
| 427 ° С (801 ° F; 700 К) | |
| Взрывоопасные пределы | 2.6–13.40% |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо) | никто [2] |
| Паспорт безопасности (SDS) | КМГС 0347 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
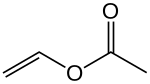
Винилацетат представляет собой соединение формулы органическое CH 3 CO 2 CH=CH 2 . Эта бесцветная жидкость является предшественником поливинилацетата , сополимеров этилена и винилацетата , поливинилового спирта и других важных промышленных полимеров. [3]
Производство
[ редактировать ]В 2007 году мировые мощности по производству винилацетата оценивались в 6 969 000 тонн в год, при этом большая часть мощностей сосредоточена в США (1 585 000, все в Техасе), Китае (1 261 000), Японии (725 000) и Тайване (650 000). [4] Средняя прейскурантная цена на 2008 год составила 1600 долларов США за тонну. Celanese является крупнейшим производителем (около 25% мировых мощностей), в то время как другие важные производители включают China Petrochemical Corporation (7%), Chang Chun Group (6%) и LyondellBasell (5%). [4]
Это ключевой ингредиент мебельного клея. [5]
Подготовка
[ редактировать ]Винилацетат – это ацетатный эфир винилового спирта . Поскольку виниловый спирт весьма нестабилен (по отношению к ацетальдегиду ), получение винилацетата более сложно, чем синтез других ацетатных эфиров.
Основной промышленный путь включает реакцию этилена и уксусной кислоты с кислородом в присутствии палладиевого катализатора. [6]
Этот метод заменил добавление уксусной кислоты к ацетилену. Основная побочная реакция — горение органических предшественников.
Механизм
[ редактировать ]Эксперименты по мечению изотопов и кинетике позволяют предположить, что в этом механизме участвуют промежуточные соединения, содержащие PdCH 2 CH 2 OAc. При удалении бета-гидрида образуются винилацетат и гидрид палладия, которые окисляются с образованием гидроксида. [7]
Альтернативные маршруты
[ редактировать ]Винилацетат когда-то получали главным образом гидроэтерификацией , т. е. добавлением уксусной кислоты к ацетилену в присутствии металлических катализаторов. Используя катализаторы ртути(II), винилацетат был впервые получен Фрицем Клатте в 1912 году. [3] В настоящее время ацетат цинка в качестве катализатора используется :
- CH 3 CO 2 H + C 2 H 2 → CH 3 CO 2 CHCH 2
Примерно 1/3 мирового производства зависит от этого маршрута, который, поскольку он экологически грязный, в основном практикуется в странах с смягченными экологическими нормами, таких как Китай.
Другой путь получения винилацетата включает разложение этилидендиацетата термическое :
- (CH 3 CO 2 ) 2 CHCH 3 → CH 3 CO 2 CHCH 2 + CH 3 CO 2 H
Полимеризация
[ редактировать ]Его можно полимеризовать с получением поливинилацетата (ПВА). С другими мономерами его можно использовать для получения различных сополимеров , таких как этилен-винилацетат (ЭВА), винилацетат- акриловая кислота (ВА/АА), поливинилхлорид ацетат (ПВХК) и поливинилпирролидон (сополимер Vp/Va, используемый в волосах ). гели ). [8] Из-за нестабильности радикала попытки контролировать полимеризацию с помощью большинства «живых/контролируемых» радикальных процессов оказались проблематичными. Однако RAFT -полимеризация (или, точнее, MADIX) предлагает удобный метод контроля синтеза ПВС путем добавления ксантогената или дитиокарбаматного агента переноса цепи.
Другие реакции
[ редактировать ]Винилацетат полезен в органическом синтезе . [9] Трансацетилирование используется для получения энантиообогащенных спиртов и сложных эфиров. Также было продемонстрировано трансацетилирование, катализируемое иридием: [10] [11]
- ROH + CH 2 =CHOAc → ROCH=CH 2 + HOAc
Трансвинилирование также возможно с использованием винилацетата. Вступает в реакцию Дильса-Альдера с диенами .
Винилацетат подвергается многим реакциям, ожидаемым для алкена и сложного эфира . Добавляют бром , получая дибромид. Галогенводороды добавляются с образованием 1-галогенэтилацетатов, которые невозможно получить другими методами из-за отсутствия соответствующих галогенспиртов. Уксусная кислота добавляется в присутствии палладиевых катализаторов с получением этилидендиацетата CH 3 CH(OAc) 2 . Он подвергается переэтерификации с различными карбоновыми кислотами . [12] Алкен также подвергается циклоприсоединениям Дильса-Альдера и 2+2.
Оценка токсичности
[ редактировать ]Испытания показывают, что винилацетат имеет низкую токсичность. Пероральная LD 50 для крыс составляет 2920 мг/кг. [3]
31 января 2009 г. окончательная оценка правительства Канады пришла к выводу, что воздействие винилацетата не вредно для здоровья человека. [13] Это решение в соответствии с Законом Канады об охране окружающей среды (CEPA) было основано на новой информации, полученной в период общественного обсуждения, а также на более поздней информации из оценки риска, проведенной Европейским Союзом.
В контексте крупномасштабного выброса в окружающую среду он классифицируется как чрезвычайно опасное вещество в Соединенных Штатах, как это определено в разделе 302 Закона США о чрезвычайном планировании и праве общества на информацию ( 42 USC 11002 ), в соответствии с которым он «не соответствует критериям токсичности [,], но из-за его острой летальности большой объем производства [или] известный риск считается вызывающим озабоченность химическим веществом». Согласно этому закону, к нему предъявляются строгие требования по отчетности со стороны предприятий, которые производят, хранят или используют его в количествах, превышающих 1000 фунтов. [14]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Заявление общественного здравоохранения о винилацетате» . Агентство по регистрации токсичных веществ и заболеваний, Центры по контролю заболеваний.
У него сладкий, приятный фруктовый запах, но у некоторых людей запах может быть резким и раздражающим.
- ^ Карманный справочник NIOSH по химическим опасностям. «#0656» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б с Биневальд, Франк; Лейболд, Эдгар; Тужина, Павел; Рошер, Гюнтер (2019). «Виниловые эфиры». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. стр. 1–16. дои : 10.1002/14356007.a27_419.pub2 . ISBN 978-3-527-30385-4 .
- ^ Jump up to: а б Х. Чинн (сентябрь 2008 г.). «Отчет о маркетинговом исследовании CEH: винилацетат» . Справочник по химической экономике . НИИ консалтинг . Проверено 1 июля 2011 г. [ мертвая ссылка ]
- ^ Карл Шмавонян (24 октября 2012 г.). «Pidilite Industries Мадукара Пареха зарабатывает его семье 1,36 миллиарда долларов» . Форбс.com . Проверено 27 января 2013 г.
хотя Pidilite пришлось бороться с ростом цен на мономер винилацетата, его ключевое сырье.
- ^ Ю.-Ф. Хан; Д. Кумар; К. Шивадинараяна и Д.В. Гудман (2004). «Кинетика горения этилена при синтезе винилацетата на катализаторе Pd/SiO 2 » (PDF) . Журнал катализа . 224 : 60–68. дои : 10.1016/j.jcat.2004.02.028 . Архивировано из оригинала (PDF) 7 марта 2008 г. Проверено 5 ноября 2006 г.
- ^ Стакчиола, Д.; Каласа, Ф.; Беркхолдер, Л.; Швабахер Алан, В.; Нейрок, М.; Тайсо Уилфред, Т. (2005). «Выяснение механизма реакции катализируемого палладием синтеза винилацетата». Angewandte Chemie, международное издание . 44 (29): 4572–4574. дои : 10.1002/anie.200500782 . ПМИД 15988776 .
- ^ «Сополимер ВП/ВА» . Совет по средствам личной гигиены. Архивировано из оригинала 16 октября 2012 года . Проверено 13 декабря 2012 г.
- ^ Манчанд, Перси С. (2001). «Винилацетат». Энциклопедия реагентов для органического синтеза . дои : 10.1002/047084289X.rv008 . ISBN 0-471-93623-5 .
- ^ Томотака Хирабаяси; Сатоши Сакагути; Ясутака Хер (2005). «Иридий-катализируемый синтез виниловых эфиров из спиртов и винилацетата» . Орг. Синтез . 82:55 orgsyn.082.0055 дои : 10.15227/ .
- ^ Ясуси Обора; Ясутака Хер (2012). «Приложение к обсуждению: катализируемый иридием синтез виниловых эфиров из спиртов и винилацетата». Орг. Синтез . 89 :307 дои : 10.15227/orgsyn.089.0307 .
- ^ Д. Сверн и Э. Ф. Джордан-младший (1963). «Виниллаурат и другие виниловые эфиры» (PDF) . Органические синтезы, Сборник . 4 : 977. Архивировано из оригинала (PDF) 5 июня 2011 г. Проверено 11 ноября 2007 г.
- ^ «Сводка комментариев общественности, полученных по проекту отчета правительства Канады об оценке винилацетата (CAS № 108-05-4)» (PDF) . Здоровье Канады. 2009.
- ^ «40 CFR: Приложение A к Части 355 — Список чрезвычайно опасных веществ и их пороговые плановые количества» (PDF) . Свод федеральных правил . заголовок 40, том. 30, часть 355, приложение. A (EPA) (изд. за декабрь 2017 г.). Государственная типография : 474. Декабрь 2017 г. Проверено 7 марта 2018 г. - через Генеральную прокуратуру США.

