Ячейка P19
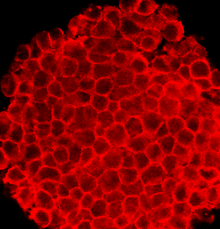
Клетки P19 эмбриональной карциномы представляют собой клеточную линию эмбрионального происхождения , полученную из тератокарциномы у мышей. Клеточная линия является плюрипотентной и может дифференцироваться в типы клеток всех трех зародышевых листков. Кроме того, это наиболее охарактеризованная клеточная линия эмбриональной карциномы (ЭК), которую можно индуцировать в клетках сердечной мышцы и нейрональных клетках с помощью различных специфических методов лечения. (ДМСО) на агрегированные клетки P19 Действительно, воздействие диметилсульфоксида вызывает дифференцировку в сердечные и скелетные мышцы . Кроме того, воздействие на клетки P19 ретиноевой кислоты (РА) может дифференцировать их в нейрональные клетки. [1]
Происхождение клеточной линии P19
[ редактировать ]Раковые клетки у людей могут привести к смерти пациента, если агрессивная раковая клетка растет и дает метастазы. Однако исследователи используют эти клетки для изучения развития раковых клеток, чтобы найти более конкретные методы лечения. Для биологов развития эмбриональная карцинома , происходящая из тератокарциномы, является хорошим объектом для изучения развития. В 1982 году Макберни и Роджерс трансплантировали 7,5-дневный эмбрион мыши в яичко, чтобы вызвать рост опухоли. клеточные культуры, содержащие недифференцированные стволовые клетки выделены Из первичной опухоли , имеющие эуплоидный кариотип . Эти стволовые клетки были названы клетками эмбриональной карциномы P19. [2] Эти производные клетки P19 быстро росли без фидерных клеток, и их было легко поддерживать. Более того, мультипотентность клеток P19 была затем подтверждена путем инъекции клеток в бластоцисты другой линии мышей. ткани всех трех зародышевых листков . Исследователи обнаружили, что у мыши-реципиента росли [3] На основе своих непрерывных исследований они дополнительно получили клеточные линии подтипов из исходных клеток P19: P19S18, P19D3, P19RAC65 и P19C16. Разница между этими клеточными линиями подтипов заключается в способности дифференцироваться в нейрональные клетки или мышечные клетки в ответ на лечение ретиноевой кислотой или ДМСО соответственно. [3] [4] [5] Совсем недавно в ходе различных исследований были созданы клеточные линии, которые первоначально были получены из дифференцированных клеток P19. Благодаря плюрипотентности клеток P19 эти новые производные клеточные линии могут быть клетками, подобными эктодерме , мезодерме и энтодерме . [6]
Дифференциация клеток P19
[ редактировать ]Клетки P19 могут поддерживать экспоненциальный рост благодаря стабильному хромосомному составу. Поскольку эмбриональная карцинома может дифференцироваться в клетки всех трех зародышевых листков, клетки P19 также могут дифференцироваться в эти клетки эктодермы, мезодермы и энтодермы. Когда клетки эмбриональной карциномы культивируются при высокой плотности, они начинают дифференцироваться . [7] Агрегируя клетки в эмбриональное тело, клетки ЭК также могут осуществлять дифференцировку. [8] В клетках P19 добавление нетоксичных концентраций лекарств к агрегированным эмбриоидным клеткам тела может индуцировать дифференцировку клеток P19 в определенные клеточные линии в зависимости от добавленного лекарства. [1] Двумя наиболее распространенными и эффективными препаратами являются ретиноевая кислота (РА) и диметилсульфоксид (ДМСО). Исследования показали, что определенная концентрация RA может индуцировать дифференцировку клеток P19 в нейрональные клетки, включая нейроны и глиальные клетки . [9] тогда как 0,5–1% ДМСО приводили к дифференцировке клеток P19 в клетки сердечной или скелетной мускулатуры. В методе лечения РА нейроны, астроглия и фибробласты могут быть идентифицированы после агрегации. Дифференцированные клетки также обладают активностью холин-ацетилтрансферазы и ацетилхолинэстеразы. [10] При лечении ДМСО клетки сердечной мышцы развивались через 5 дней воздействия, а клетки скелетных мышц появлялись через 8 дней воздействия. Эти исследования показали, что воздействие препарата заставляет мультипотентные клетки P19 дифференцироваться в разные слои клеток. Поскольку концентрации ретиноевой кислоты или ДМСО нетоксичны для клеток, специфическая дифференцировка препарата происходит за счет индукции клеток, а не отбора. Мутанты клеток P19 были созданы для изучения механизма специфической дифференцировки лекарств. [10] Более того, сигнальные пути, связанные с нейрогенезом и миогенезом, также были исследованы путем изучения экспрессии генов или создания мутантов клеток P19.
Нейрогенез в клетках P19.
[ редактировать ]Обработка недифференцированных клеток P19 ретиноевой кислотой может специфически индуцировать их в нейрональные клетки. Использование доз от 1 мкМ до 3 мкМ RA может привести к образованию нейронов как наиболее распространенного типа клеток. [4] Нейроны, подвергшиеся такому лечению, достигли наибольшей численности в период от шести до девяти дней. Некоторые нейрональные маркеры, такие как белки нейрофиламентов , антиген HNK-1 и места связывания столбнячного токсина, в эти дни экспрессируются на самых высоких уровнях. [11] После шести-девяти дней лечения относительная популяция нейронов снижается, вероятно, из-за более быстрой пролиферации ненейрональных клеток. Через 10 дней воздействия астроглиальные клетки можно обнаружить с помощью глиального фибриллярного кислого белка (GFAP), который является специфическим маркером глиальных клеток. Помимо нейронов и астроцитов , клетки P19 также могут дифференцироваться в олигодендроциты , что можно обнаружить с помощью специфических маркеров, миелин-ассоциированного гликопротеина и 2',3'-циклонуклеотидной 3'-фосфодиэстеразы . Более того, олигодендроциты также развивались и мигрировали в пучки волокон у мышей, когда индуцированные РА клетки были трансплантированы в мозг . [12]
Ретиноевая кислота может индуцировать не только клеток P19, но и других клеток-предшественников или эмбриональных стволовых клеток дифференцировку . Поскольку клетки после лечения ретиноевой кислотой не сразу экспрессировали гены-маркеры нейронов, РА должен инициировать некоторый путь процесса клеточной дифференцировки. Во многих исследованиях использовались клетки P19 для изучения механизмов, индуцированных РА, включая создание мутантного аллеля генов рецепторов ретиноевой кислоты и изучение экспрессии генов рецепторов, Hox-генов и ретинол-связывающих белков при воздействии РА. [13] [14]
Все эти исследования показывают, что клетка P19 является хорошей модельной системой in vitro для изучения механизма действия лекарств, которые влияют на определенные клеточные пути. Кроме того, используя способность RA-индуцированного нейрогенеза в клетках P19, многие исследователи начали выявлять механизмы дифференцировки нейро- или глиогенеза in vitro. Несколько родственных путей, в том числе путь Wnt/β-катенин, путь Notch и путь hedgehog, исследуются либо с использованием экспрессии генов, либо с созданием аллелей для родственных генов. [15] [16] [17]
Миогенез в клеточной линии P19
[ редактировать ]Как и в случае с ретиноевой кислотой, дифференцировка, индуцированная ДМСО, неспецифична для клеток P19. Он также может индуцировать нейробластомы клетки , клетки рака легких и ES-клетки мыши. [18] [19] [20] В концентрации 0,5–1% ДМСО индуцировал клетки P19 агрегировать и процессировать мезодермальные и энтодермальные типы клеток. [1] [10] [21]
Клеточные механизмы, происходящие при агрегации и дифференцировке, до сих пор полностью не изучены. Однако некоторые исследования показали, что клеточная коммуникация играет важную роль в мышечной дифференцировке клеток P19, что может объяснить, почему клеткам необходимо сначала агрегировать, чтобы осуществить мышечную дифференцировку. [6]
Чтобы выяснить механизм миогенеза в клетках P19, было обнаружено, что несколько сердечных специфичных транскрипционных факторов, включая GATA-4, MEF2c, Msx-1, Nkx2.5, MHox, Msx-2 и MLP, изменяются во время дифференцировки. [6] Отчеты показали, что GATA-4, NKx2.5 и MEF2c активировались после индукции ДМСО. [22] [23] В последние годы клетки Р19 стали также использовать при изучении механизма кардиальной дифференцировки и миогенеза. Основной затронутый сигнальный путь — путь костных морфогенетических белков (BMP) — наиболее изученный путь передачи сигналов в клетках P19. Создав клеточную линию P19CL6noggin, которая сверхэкспрессирует noggin -антагонист BMP , они обнаружили, что мутантные клетки не дифференцируются в кардиомиоциты при обработке 1% ДМСО, что позволяет предположить, что BMP необходимы для дифференцировки кардиомиоцитов в этой системе. Они также предоставили доказательства того, что TAK1, Nkx-2.5 и GATA-4 важны в кардиогенном сигнальном пути BMP. [24]
Будущие направления
[ редактировать ]Клетки P19 обеспечивают ценное образование как нейрональных, так и мышечных клеток in vitro. Поскольку клетки P19 легче поддерживать и культивировать по сравнению с другими эмбриональными стволовыми клетками, они являются удобной моделью для проведения исследований развития in vitro. Методы манипулирования этой клеточной линией для экспрессии или нокаута определенных генов позволяют детально исследовать сигнальные пути, функциональные аспекты и регуляцию экспрессии белков миогенеза и нейрогенеза. Расширенные исследования также могут пролить свет на более поздние стадии развития и созревания сердца или мозга .
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Макберни, штат Вашингтон; Роджерс, Би Джей (февраль 1982 г.). «Выделение клеток мужской эмбриональной карциномы и закономерности репликации их хромосом». Биология развития . 89 (2): 503–8. дои : 10.1016/0012-1606(82)90338-4 . ПМИД 7056443 .
- ^ Макберни, М.В. (1993). «Клетки эмбриональной карциномы P19». Int J Dev Biol . 37 (1): 135–140. ПМИД 8507558 .
- ^ Перейти обратно: а б Россант, Дж; Макберни, штат Вашингтон (август 1982 г.). «Потенциал развития эуплоидной мужской клеточной линии тератокарциномы после инъекции бластоцисты». Журнал эмбриологии и экспериментальной морфологии . 70 : 99–112. ПМИД 7142904 .
- ^ Перейти обратно: а б Фанесток, М; Кошланд Д.Э.-младший (февраль 1979 г.). «Контроль рецептора таксиса галактозы у Salmonella typhimurium» . Журнал бактериологии . 137 (2): 758–63. дои : 10.1128/jb.137.2.758-763.1979 . ПМК 218354 . ПМИД 370099 .
- ^ Крейн, БЛ; Руперт, CS (февраль 1979 г.). «Взаимодействия дезоксирибонуклеиновой кислоты с мембраной вблизи места начала репликации и инициации синтеза дезоксирибонуклеиновой кислоты в Escherichia coli» . Журнал бактериологии . 137 (2): 740–5. дои : 10.1128/jb.137.2.740-745.1979 . ПМК 218351 . ПМИД 370098 .
- ^ Перейти обратно: а б с ван дер Хейден, Массачусетс; Дефайз, ЛГ (1 мая 2003 г.). «Двадцать один год клеток P19: чему научила нас линия клеток эмбриональной карциномы о дифференцировке кардиомиоцитов» . Сердечно-сосудистые исследования . 58 (2): 292–302. дои : 10.1016/S0008-6363(02)00771-X . ПМИД 12757864 .
- ^ Макберни, MW (ноябрь 1976 г.). «Клональные линии клеток тератокарциномы in vitro: дифференцировка и цитогенетические характеристики». Журнал клеточной физиологии . 89 (3): 441–55. дои : 10.1002/jcp.1040890310 . ПМИД 988033 .
- ^ Мартин, Греция; Эванс М.Дж. (1975). «Множественная дифференциация клональных стволовых клеток тератокарциномы после формирования эмбриоидных тел in vitro». Клетка . 6 (4): 467–74. дои : 10.1016/0092-8674(75)90035-5 .
- ^ Эдвардс, МК; Харрис, Дж. Ф.; Макберни, штат Вашингтон (декабрь 1983 г.). «Индуцированная дифференцировка мышц в клеточной линии эмбриональной карциномы» . Молекулярная и клеточная биология . 3 (12): 2280–6. дои : 10.1128/mcb.3.12.2280 . ПМК 370099 . ПМИД 6656767 .
- ^ Перейти обратно: а б с Джонс-Вильнёв, ЕМ; Рудницкий, Массачусетс; Харрис, Дж. Ф.; Макберни, штат Вашингтон (декабрь 1983 г.). «Нейральная дифференцировка клеток эмбриональной карциномы, индуцированная ретиноевой кислотой» . Молекулярная и клеточная биология . 3 (12): 2271–9. дои : 10.1128/mcb.3.12.2271 . ПМК 370098 . ПМИД 6656766 .
- ^ Макберни, штат Вашингтон; Ройль, КР; Союзник, ИИ; Насипури, С; Белл, Дж. К.; Крейг, Дж (март 1988 г.). «Дифференцировка и созревание нейронов, происходящих из эмбриональной карциномы, в клеточной культуре» . Журнал неврологии . 8 (3): 1063–73. doi : 10.1523/JNEUROSCI.08-03-01063.1988 . ПМК 6569242 . ПМИД 2894413 .
- ^ Стейнс, Вашингтон; Крейг, Дж; Ройль, К; Макберни, штат Вашингтон (апрель 1996 г.). «Клетки эмбриональной карциномы P19, обработанные ретиноевой кислотой, дифференцируются в олигодендроциты, способные к миелинизации». Нейронаука . 71 (3): 845–53. дои : 10.1016/0306-4522(95)00494-7 . ПМИД 8867053 .
- ^ Пратт, Массачусетс; Кралова Дж.; Макберни, штат Вашингтон (декабрь 1990 г.). «Доминантно-негативная мутация гена рецептора альфа-ретиноевой кислоты в клетках эмбриональной карциномы, не реагирующих на ретиноевую кислоту» . Молекулярная и клеточная биология . 10 (12): 6445–53. дои : 10.1128/mcb.10.12.6445 . ПМК 362921 . ПМИД 2174108 .
- ^ Чен, Ю; Риз, Д.Х. (октябрь 2011 г.). «Сигнальный путь ретинола в плюрипотентных клетках P19 мыши» . Журнал клеточной биохимии . 112 (10): 2865–72. дои : 10.1002/jcb.23200 . ПМИД 21618588 .
- ^ Най, Дж. С.; Копан, Р; Аксель, Р. (сентябрь 1994 г.). «Активированный Notch подавляет нейрогенез и миогенез, но не глиогенез в клетках млекопитающих». Разработка . 120 (9): 2421–30. дои : 10.1242/dev.120.9.2421 . ПМИД 7956822 .
- ^ Хамада-Канадзава, М; Исикава, К; Номото, К; Уодзуми, Т; Каваи, Ю; Нарахара, М; Мияке, М (27 февраля 2004 г.). «Сверхэкспрессия Sox6 вызывает клеточную агрегацию и нейрональную дифференцировку клеток эмбриональной карциномы P19 в отсутствие ретиноевой кислоты» . Письма ФЭБС . 560 (1–3): 192–8. Бибкод : 2004FEBSL.560..192H . дои : 10.1016/S0014-5793(04)00086-9 . ПМИД 14988021 .
- ^ Тан, Ю; Се, Z; Дин, М; Ван, З; Ю, Кью; Мэн, Л; Чжу, Х; Хуанг, X; Ю, Л; Мэн, X; Чен, Ю (сентябрь 2010 г.). «Повышенные уровни транскрипционного фактора FoxA1 в плюрипотентных клетках эмбриональной карциномы P19 стимулируют нервную дифференцировку». Стволовые клетки и развитие . 19 (9): 1365–74. дои : 10.1089/scd.2009.0386 . ПМИД 19916800 .
- ^ Лако, М; Линдси, С; Линкольн, Дж; Кэрнс, премьер-министр; Армстронг, Л; Холе, Н. (2001). «Характеристика экспрессии гена Wnt во время дифференцировки мышиных эмбриональных стволовых клеток in vitro: роль Wnt3 в усилении гемопоэтической дифференцировки» . Механизмы развития . 103 (1–2): 49–59. дои : 10.1016/S0925-4773(01)00331-8 . ПМИД 11335111 .
- ^ Тралка, ТС; Рабсон, А.С. (декабрь 1976 г.). «Формирование ресничек в культурах клеток рака легких человека, обработанных диметилсульфоксидом». Журнал Национального института рака . 57 (6): 1383–8. дои : 10.1093/jnci/57.6.1383 . ПМИД 1003564 .
- ^ Литтауэр, УЗ; Палфри, К; Кимхи, Ю; Спектор, я (май 1978 г.). «Индукция дифференцировки клеток нейробластомы мыши». Монография Национального института рака (48): 333–7. ПМИД 748753 .
- ^ Макберни, Миссури; Джонс-Вильнёв, ЕМ; Эдвардс, МК; Андерсон, Пи Джей (9 сентября 1982 г.). «Контроль мышечной и нейрональной дифференцировки в культивируемой линии клеток эмбриональной карциномы». Природа . 299 (5879): 165–7. Бибкод : 1982Natur.299..165M . дои : 10.1038/299165a0 . ПМИД 7110336 . Через 2 дня воздействия появились энтодермоподобные клетки, напоминающие примитивную внеэмбриональную энтодерму. Через 6 дней воздействия внутри агрегатов появилась сердечная мышца. Содержание клеток сердечной мышцы составляло 25% клеток. Через 10 дней воздействия вокруг тела эмбриона появились клетки скелетных мышц.
- ^ Скерьянц, И.С.; Петропулос, Х; Риджуэй, AG; Уилтон, С. (25 декабря 1998 г.). «Фактор 2C энхансера миоцитов и Nkx2-5 усиливают экспрессию друг друга и инициируют кардиомиогенез в клетках P19» . Журнал биологической химии . 273 (52): 34904–10. дои : 10.1074/jbc.273.52.34904 . ПМИД 9857019 .
- ^ Грепен, К; Немер, Г; Немер, М. (июнь 1997 г.). «Усиленный кардиогенез в эмбриональных стволовых клетках, сверхэкспрессирующих фактор транскрипции GATA-4». Разработка . 124 (12): 2387–95. дои : 10.1242/dev.124.12.2387 . ПМИД 9199365 .
- ^ Монцен, К; Сиодзима, я; Хирои, Ю; Кудо, С; Ока, Т; Такимото, Э; Хаяши, Д; Хосода, Т; Хабара-Окубо, А; Накаока, Т; Фудзита, Т; Язаки, Ю; Комуро, я (октябрь 1999 г.). «Костные морфогенетические белки индуцируют дифференцировку кардиомиоцитов посредством митоген-активируемой протеинкиназы киназы киназы TAK1 и сердечных факторов транскрипции Csx/Nkx-2.5 и GATA-4» . Молекулярная и клеточная биология . 19 (10): 7096–105. дои : 10.1128/mcb.19.10.7096 . ПМК 84704 . ПМИД 10490646 .
Внешние ссылки
[ редактировать ]- Вандерхейден, М; Дефайз, Л. (2003). «Двадцать один год клеток P19: чему научила нас линия клеток эмбриональной карциномы о дифференцировке кардиомиоцитов» . Сердечно-сосудистые исследования . 58 (2): 292–302. дои : 10.1016/S0008-6363(02)00771-X . ПМИД 12757864 .
- Запись о целлозавре для P19