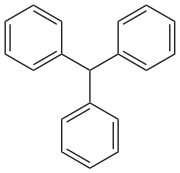
Трифенилметан
| |

| |
| Имена | |
|---|---|
| Предпочтительное имя IUPAC
1,1 ′ , 1 ″ -метанетриилтрибензол | |
| Другие имена
Трифенилметан
1,1 ′ , 1 ″ -метилидинетрисбензол | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Чеби | |
| Chemspider | |
| Echa Infocard | 100.007.524 |
| ЕС номер |
|
PubChem CID
|
|
| НЕКОТОРЫЙ | |
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 19 H 16 | |
| Молярная масса | 244.337 g·mol −1 |
| Появление | Бесцветный твердый |
| Плотность | 1,014 г/см 3 |
| Точка плавления | 92–94 ° C (с 198 до 201 ° F; 365 до 367 K) |
| Точка кипения | 359 ° C (678 ° F; 632 K) |
| Нерастворимый | |
| Растворимость | Растворим в диоксане [ 1 ] и гексан |
| Кислотность (p k a ) | 33.3 |
| −165.6×10 −6 см 3 /мол | |
| Опасности | |
| GHS Маркировка : | |

| |
| Предупреждение | |
| H315 , H319 , H335 | |
| Лист данных безопасности (SDS) | Внешние MSDS |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Трифенилметан или трифенил метан (иногда также известный как тритан ), является углеводородом с формулой (C 6 H 5 ) 3 Ch. Это бесцветное твердое вещество растворим в неполярных органических растворителях, а не в воде. Трифенилметан является основным скелетом многих синтетических красителей, называемых триарилметановыми красителями , многие из них являются индикаторами pH , а некоторые демонстрируют флуоресценцию . Группа Trityl в органической химии представляет собой трифенилметильную группу pH 3 C, например, трифенилметилхлорид (тритил хлорид) и трифенилметиловый радикал (радикал Trityl).
Подготовка
[ редактировать ]Трифенилметан был впервые синтезирован в 1872 году немецким химиком Августа Кекуле нагревающим дифенилльмерка (HG (C 6 H 5 ) 2 , Кексилбердифенил ) с бензалом хлор ( и его голландским учеником Антуан Пол Николас Франчамонт (1844–1919) , . 6 с ч , Бензилорид ). [ 2 ]
Трифенилметан может быть синтезирован реакцией Фриделя -Крафта от бензола и хлороформа с хлорида алюминия катализатором :
- 3 C 6 H 6 + CHCL 3 → PH 3 CH + 3 HCL
Альтернативно, бензол может реагировать с тетрахлоридом углерода, используя тот же катализатор, чтобы получить трифенилметилхлорид - алюминиевый хлоридный аддукт, который гидролизуется разбавленной кислотой: [ 3 ]
- 3 C 6 H 6 + CCL 4 + Alcl 3 → PH 3 CCL · Alcl 3
- PH 3 CCL · ALCL 3 + HCl → PH 3 CH
Он также может быть синтезирован из бензилиденххлорида , который готовится из бензальдегида и фосфора пентахлорида .
Реакции связи СН
[ редактировать ]Связь pH 3 C-H является относительно слабой, с энергией диссоциации связи (BDE) 81 ккал/моль, или около 24 ккал/моль меньше, чем метан. [ 4 ] Соответственно, трифенилметан мягко кислый, с P k a 33,3. [ 5 ]
Трифенилметан значительно более кислый, чем большинство других углеводородов, потому что заряд делокализуется на трех фенильных кольцах. Стерические эффекты, однако, предотвращают одновременно все три фенильных кольца одновременно. Следовательно, дифенилметан еще более кислый, хотя и слегка, потому что в его анионе заряд распространяется по двум фенильным кольцам одновременно.
Тритил анион изолирован в Crown Ethers :
Его натриевая соль может быть приготовлена из хлорида : [ 6 ]
- (C 6 H 5 ) 3 CCL + 2 Na → (C 6 H 5 ) 3 CNA + NaCl
Использование Tritylsodium в качестве сильной, ненуклеофильной основы было затмешено популяризацией бутиллита и связанных с ними сильных оснований.
Немодифицированный анион является красным и может использоваться в качестве индикатора в кислотно -базе . Полученные вещества оказались полезными в качестве химических красителей.
Триарилметановые красители
[ редактировать ]Примеры трюйлметановых красителей - зеленый бромокрозол :
Trityl Group
[ редактировать ]Защита группы
[ редактировать ]Трифенилметиловый заместитель, также называемый Trityl, широко используется в органической химии. Тритил служит защитной группой для спиртов. [ 7 ]
- Защита (требует акцептора Proton): pH 3 CCL + ROH → PH 3 COR + HCL
- Действие: pH 3 COR + HBR → ROH + PH 3 CBR
Платформа для необычных функциональных групп
[ редактировать ]Производные к тратированию реактивных функциональных групп часто являются кристаллическими, а в некоторых случаях стерически стабилизируются по сравнению с менее громоздкими производными. Три такие производные являются S -нитросотрифенилметанетиол (pH 3 CSNO), третилсульфенилхлорид (pH 3 CSCL) и Trityl Sulfenamide (pH 3 CSNH 2 ). [ 8 ]
Смотрите также
[ редактировать ]- Тетрафенилметан
- Трифенилметанол
- Трифенилметилхлорид
- Трифенилметил гексафторофосфат
- Трифенилметиловый радикал
Ссылки
[ редактировать ]- ^ "Трифенилметан | 519-73-3" .
- ^ Август Кекуле и А. Франчамонт (1872) «О трифенилметане» (на трифенилметане), сообщения о немецком химическом обществе , 5 : 906–908.
- ^ JF Норрис (1925). «Трифенилметан». Органические синтезы . 4 : 81. doi : 10.15227/orgsyn.004.0081 .
- ^ Сюэ, Сяо-Сонг; Джи, Пенджу; Чжоу, Биинг; Ченг, Джин-Пей (2017). «Основная роль энергетики связи в активации/функционализации C - H». Химические обзоры . 117 (13): 8622–8648. doi : 10.1021/acs.chemrev.6b00664 . PMID 28281752 .
- ^ Рональд Бреслоу и Уильям Чу (1969). «Электрохимические определения P k a 's. Triphenylmethanes и циклогептатриен». Журнал Американского химического общества . 92 (7): 2165. DOI : 10.1021/JA00710A077 .
- ^ WB Renfrow Jr и Cr Hauser (1943). «Трифенилметилсодий» . Органические синтезы ; Собранные объемы , вып. 2, с. 607
- ^ Дельберт Д. Рейнольдс, Уильям Ллойд Эванс (1942). «β -D -Glucose-1,2,3,4-тетраацетат». Органические синтезы . 22 : 56. doi : 10.15227/orgsyn.022.0056 .
- ^ Glidewell, C.; Фергюсон, Г. (1994). «Молекулы изоэлектронные с 2,2,2-трифенилэтанолом: множественные режимы водородных связей в структурах о-тритилгидроксиламина, pH 3 Conh 2 и трифенилметансульфенамид, pH 3 CSNH 2 ». Acta Crystallographica Раздел C Crystal Structure Communications . 50 (8): 1362–1366. BIBCODE : 1994CCRC..50.1362G . doi : 10.1107/s0108270194004439 .


