Авобензон
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК 3-(4- трет -Бутилфенил)-1-(4-метоксифенил)пропан-1,3-дион | |
| Другие имена бутилметоксидибензоилметан; 4-трет-бутил-4'-метоксидибензоилметан | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.067.779 |
| Номер ЕС |
|
| КЕГГ | |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 20 Н 22 О 3 | |
| Молярная масса | 310.39 g/mol |
| Появление | бесцветный кристалл |
| Страница дополнительных данных | |
| Авобензон (страница данных) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Авобензон ( торговые названия Parsol 1789 , Milestab 1789 , Eusolex 9020 , Escalol 517 , Neo Heliopan 357 и другие, INCI бутилметоксидибензоилметан) представляет собой органическую молекулу и маслорастворимый ингредиент, используемый в солнцезащитных продуктах для поглощения всего спектра UVA - лучей.
История
[ редактировать ]Авобензон был запатентован в 1973 году и одобрен в ЕС в 1978 году. Он был одобрен FDA в 1988 году. По состоянию на 2021 год FDA объявило, что не поддерживает авобензон как общепризнанный безопасный и эффективный препарат (GRASE). [1] сославшись на необходимость дополнительных данных по безопасности. Авобензон был запрещен в 2020 году правительством Палау из-за опасений по поводу токсичности для рифов. [2]
Характеристики
[ редактировать ]Чистый авобензон представляет собой кристаллический порошок от белесого до желтоватого цвета со слабым запахом. [3] растворяясь в изопропаноле , диметилсульфоксиде , децилолеате, каприновой кислоте/каприловой кислоте, триглицеридах и других маслах. Он не растворяется в воде.
Авобензон – производное дибензоилметана . Авобензон существует в основном состоянии в виде смеси енольной и кетоформ, отдавая предпочтение хелатному енолу. [4] Эта енольная форма стабилизируется за счет внутримолекулярных водородных связей внутри β-дикетона. [5] Его способность поглощать ультрафиолетовый свет в более широком диапазоне длин волн, чем у многих других солнцезащитных агентов, привела к его использованию во многих коммерческих препаратах, продаваемых как солнцезащитные кремы «широкого спектра». Авобензон имеет максимум поглощения 357 нм. [6]
Безопасность
[ редактировать ]Авобензон, солнцезащитный активный ингредиент на нефтяной основе. [7] безопасным и эффективным ( GRASE ) из-за отсутствия достаточных данных, подтверждающих это утверждение. обычно не признается FDA [1] Тем не менее, это по-прежнему единственный одобренный FDA фильтр UVA (концентрация до 3%). [8] Авобензон также одобрен во всех других юрисдикциях, таких как ЕС (до 5%), Австралия и Япония .
Исследование, проведенное в 2017 году в Московском государственном университете имени Ломоносова, показало, что хлорированная вода и ультрафиолетовый свет могут вызвать распад авобензона на различные другие органические соединения, в том числе; ароматические кислоты , альдегиды , фенолы и ацетофеноны , которые могут вызвать неблагоприятные последствия для здоровья. [9] [10] [11]
Стабильность
[ редактировать ]Авобензон чувствителен к свойствам растворителя, относительно стабилен в полярных протонных растворителях и нестабилен в неполярной среде. Кроме того, когда он облучается УФА-светом, он генерирует триплетное возбужденное состояние в кето-форме, которое может либо вызвать распад авобензона, либо передать энергию биологическим мишеням и вызвать вредные эффекты. [4]
Было показано, что авобензон значительно разлагается под действием света, что со временем приводит к снижению защиты. [12] [13] [14] УФ-А-излучения в солнечный день в умеренном климате достаточно, чтобы разрушить большую часть соединения. Данные, представленные Управлению по санитарному надзору за качеством пищевых продуктов и медикаментов Ассоциацией косметики, туалетных принадлежностей и парфюмерии, указывают на изменение УФ-поглощения авобензона на -36% после одного часа воздействия солнечного света. [15] По этой причине в солнцезащитных продуктах авобензон всегда содержится вместе с фотостабилизатором, например октокриленом . Другие фотостабилизаторы включают:
- 4-Метилбензилиденкамфора ( USAN Enzacamene)
- Тиносорб S ( Бемотризинол США , Бис-этилгексилоксифенол Метоксифенил Триазин INCI)
- США Тиносорб М ( бисоктризол , INCI метилен-бис-бензотриазолилтетраметилбутилфенол)
- Бутилоктилсалицилат (торговая марка HallBrite BHB - [1] )
- Гексадецилбензоат
- Бутилоктилбензоат
- HallBrite PSF (INCI ундецилкрилендиметиконE) [16]
- Mexoryl SX (USAN Ecamsule , терефталидендикамфорсульфоновая кислота INCI)
- Синоксил HSS (INCI триметоксибензилиденпентандион) [17]
- Corapan TQ (INCI диэтилгексил-2,6-нафталат) [18]
- Parsol SLX (INCI Полисиликон-15) [19]
- Oxynex ST (INCI диэтилгексил сирингилиден малонат) [20]
- Поликрилен (INCI Polyester-8) [21]
- SolaStay S1 (Этилгексилметоксикрилен INCI) [22]
- Октилсалицилат (INCI Ethylhexyl Salicylate) [23]
Комплексообразование авобензона с циклодекстринами также может повысить его фотостабильность. [24] Составы авобензона с гидроксипропил-бета-циклодекстрином показали значительное снижение фотоиндуцированной деградации, а также уменьшение трансдермального проникновения поглотителя УФ-излучения при использовании в высоких концентрациях. [25]
Фотостабильность авобензона еще больше увеличивается, когда в состав солнцезащитных кремов входят антиоксидантные соединения. Мангиферин , глутатион , убихинон , витамин С , витамин Е , бета-каротин и транс-ресвератрол продемонстрировали некоторую способность защищать авобензон от фотодеградации. [26] [27] [28] [29] Стабильность и эффективность авобензона, по-видимому, продолжает расти по мере добавления в солнцезащитный крем большего количества антиоксидантов.
Согласно некоторым исследованиям, «наиболее эффективные солнцезащитные кремы содержат авобензон и диоксид титана ». [30] [31] Авобензон может быстрее разлагаться на свету в сочетании с минеральными поглотителями УФ-излучения, такими как оксид цинка и диоксид титана, хотя при правильном покрытии минеральных частиц эту реакцию можно уменьшить. [32] Диоксид титана, легированный марганцем, может быть лучше, чем нелегированный диоксид титана, для улучшения стабильности авобензона. [33]
Различный
[ редактировать ]В виде енолята авобензон образуется с ионами тяжелых металлов (таких как Fe 3+ ) цветные комплексы, и хелатирующие агенты для их подавления можно добавлять . Стеараты , соли алюминия, магния и цинка могут привести к образованию плохо растворимых осадков. [3] Производители также рекомендуют избегать включения солей железа и трехвалентного железа, тяжелых металлов , доноров формальдегида, а также ПАБК и эфиров ПАБК. [ нужна ссылка ]
Авобензон в солнцезащитном креме может окрасить одежду в желто-оранжевый цвет и сделать ее липкой при стирке в воде, богатой железом, поскольку он вступает в реакцию с железом, вызывая ржавчину. Повреждение можно устранить с помощью средства для удаления ржавчины или пятновыводителя. [34] [35] Окрашивающие свойства солнцезащитного крема на основе авобензона особенно заметны на лодках из стекловолокна с белым гелькоутом. [ нужна ссылка ]
Авобензон также реагирует с трифторидом бора с образованием стабильного кристаллического комплекса, который сильно флуоресцирует под УФ-облучением. Эмиссионный цвет кристаллов зависит от молекулярной упаковки авобензонового комплекса бора. Фотолюминесценция также может быть изменена механической силой в твердом состоянии, что приводит к явлению, называемому « механохромной люминесценцией ». Измененный цвет излучения восстанавливается медленно при комнатной температуре или быстрее при более высоких температурах. [36]
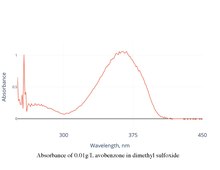
Спектр поглощения
[ редактировать ]Авобензон имеет пик поглощения около 360 нм в растворенном виде. Пик может слегка смещаться в зависимости от растворителя.
Подготовка
[ редактировать ]Соединение получают путем взаимодействия метилового эфира 4-трет-бутилбензойной кислоты (из 4-трет-бутилбензойной кислоты путем этерификации метанолом) с 4-метоксиацетофеноном в толуоле в присутствии амида натрия посредством конденсации Кляйзена . [37]

Согласно недавней заявке на патент, [38] Выходы до 95% получают с теми же исходными веществами в толуоле в присутствии метилата калия .
Он подвержен кето-енольной таутомерии и при растворении существует преимущественно енол . Под воздействием УФ-излучения он может превращаться в кето-форму, а после помещения в темноту снова превращаться в еноловую форму. [39]
См. также
Примечания
[ редактировать ]- ^ Jump up to: а б Исследования, Центр оценки лекарств и (16 ноября 2021 г.). «Вопросы и ответы: сообщения FDA считаются окончательным заказом и предлагаемым заказом на солнцезащитный крем, отпускаемый без рецепта» . FDA .
- ^ «ПРАВИЛА, ЗАПРЕЩАЮЩИЕ СОЛНЦЕЗАЩИТНЫЕ СРЕДСТВА, ТОКСИЧНЫЕ ДЛЯ РИФОВ» (PDF) . Правительство Палау. 2020.
- ^ Jump up to: а б «Делаем косметику®, авобензон» . Makingcosmetics.com . Архивировано из оригинала 1 августа 2015 г. Проверено 29 июля 2015 г.
- ^ Jump up to: а б Пэрис С., Льяобе-Валле В., Хименес О., Труллас С., Миранда М. (январь – февраль 2009 г.). «Блокированная дикето-форма авобензона: фотостабильность, фотосенсибилизирующие свойства и триплетное гашение с помощью UVB-фильтра, полученного из триазина» . Фотохимия и фотобиология . 85 (1): 178–184. дои : 10.1111/j.1751-1097.2008.00414.x . ПМИД 18673327 .
- ^ Завадьяк Дж., Мжичек М. (октябрь 2012 г.). «Влияние заместителя на УФ-поглощение и равновесие кето-енольной таутомерии производных дибензоилметана». Spectrochimica Acta Часть A: Молекулярная спектроскопия . 96 : 815–819. Бибкод : 2012AcSpA..96..815Z . дои : 10.1016/j.saa.2012.07.109 . ПМИД 22925908 .
- ^ Вильхабер Г., Гретер-Бек С., Кох О., Джонкок В., Крутманн Дж. (март 2006 г.). «Солнцезащитные кремы с максимумом поглощения > или = 360 нм обеспечивают оптимальную защиту от UVA1-индуцированной экспрессии матриксной металлопротеиназы-1, интерлейкина-1 и интерлейкина-6 в фибробластах кожи человека». Фотохимия Фотобиология . 5 (3): 275–282. дои : 10.1039/b516702g . ПМИД 16520862 . S2CID 37910033 .
- ^ «Зачем оценивать активный оксибензон солнцезащитного крема (бензофенон-3) на предмет канцерогенности и репродуктивной токсичности или считать его небезопасным для использования человеком?» (PDF) .
- ^ «Спустя более десяти лет FDA все еще не разрешает использование новых солнцезащитных кремов» .
- ^ «Солнцезащитные кремы под воздействием солнечного света распадаются на опасные химические соединения» . ЭврекАлерт! . Проверено 30 июня 2017 г.
- ^ Ван, Ченг; Бавкон Краль, Мойка; Кошмрль, Берта; Яо, Цзюнь; Кошенина, Сузана; Полякова Ольга Владимировна; Артаев Вячеслав Б.; Лебедев Альберт Т.; Требше, Полонца (сентябрь 2017 г.). «Стабильность и удаление некоторых продуктов хлорирования авобензона». Хемосфера . 182 : 238–244. Бибкод : 2017Chmsp.182..238W . doi : 10.1016/j.chemSphere.2017.04.125 . ПМИД 28500968 .
- ^ Требше, Полонка; Полякова Ольга Владимировна; Баранова Мария; Краль, Мойка Бавкон; Доленц, Дарко; Сараха, Мохамед; Кутин, Александр; Лебедев, Альберт Т. (15 сентября 2016 г.). «Превращение авобензона в условиях водного хлорирования и УФ-облучения». Исследования воды . 101 : 95–102. Бибкод : 2016WatRe.101...95T . дои : 10.1016/j.watres.2016.05.067 . ПМИД 27258620 .
- ^ Шатлен Э., Габар Б. (сентябрь 2001 г.). «Фотостабилизация бутилметоксидибензоилметана (авобензона) и этилгексилметоксициннамата с помощью бис-этилгексилоксифенолметоксифенилтриазина (Тиносорб S), нового широкополосного УФ-фильтра». Фотохимия и фотобиология . 74 (3): 401–406. doi : 10.1562/0031-8655(2001)0740401POBMAA2.0.CO2 . ISSN 0031-8655 . ПМИД 11594052 . S2CID 29879472 .
- ^
 Таррас-Вальберг Н., Стенхаген Г., Ларко О., Розен А., Веннберг А.М., Веннерстрем О. (октябрь 1999 г.). «Изменение поглощения ультрафиолета солнцезащитными кремами после ультрафиолетового облучения» . Журнал исследовательской дерматологии . 113 (4): 547–553. дои : 10.1046/j.1523-1747.1999.00721.x . ПМИД 10504439 .
Таррас-Вальберг Н., Стенхаген Г., Ларко О., Розен А., Веннберг А.М., Веннерстрем О. (октябрь 1999 г.). «Изменение поглощения ультрафиолета солнцезащитными кремами после ультрафиолетового облучения» . Журнал исследовательской дерматологии . 113 (4): 547–553. дои : 10.1046/j.1523-1747.1999.00721.x . ПМИД 10504439 . - ^ Ветц Ф., Рутабул К., Денис А., Рико-Латте I (март – апрель 2005 г.). «Новый длинноцепочечный УФ-поглотитель, полученный из 4-трет-бутил-4'-метоксидибензоилметана: стабильность поглощения при солнечном облучении» . Журнал косметической науки . 56 (2): 135–148. doi : 10.1562/2004-03-09-ra-106 (неактивен 18 февраля 2024 г.). ПМИД 15870853 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на февраль 2024 г. ( ссылка ) - ^ «Письмо CTFA о предварительной окончательной монографии по безрецептурному солнцезащитному крему» (PDF) . Управление по контролю за продуктами и лекарствами.
- ^ «Холлбрайт® ПСФ» . Архивировано из оригинала 2 октября 2011 г. Проверено 25 мая 2011 г.
- ^ Р.К. Чаудхури, М.А. Олленго, П. Сингх и Б.С. Мартинсиг, 3-(3,4,5-триметоксибензилиден)-2,4-пентандион: разработка нового фотостабилизатора со свойствами повышения SPF in vivo и его использование в разработке широкого спектра действия. Составы солнцезащитных средств спектра, Международный журнал косметической науки, 39(1):25-35, 2017; Впервые опубликовано 29 июня 2016 г. | дои: 10.1111/ics.12344
- ^ Бонда С.; Стейнберг, округ Колумбия (2000). «Новый фотостабилизатор для солнцезащитных кремов полного спектра». Косметика и туалетные принадлежности . 115 (6): 37–45.
- ^ «Архивная копия» (PDF) . Архивировано из оригинала (PDF) 24 февраля 2008 г. Проверено 3 декабря 2007 г.
{{cite web}}: CS1 maint: архивная копия в заголовке ( ссылка ) - ^ Чаудхури Р.К., Ласку З., Пуччетти Г., Дешпанде А.А., Пакникар С.К. (май – июнь 2006 г.). «Разработка фотостабилизатора со встроенными антиоксидантными свойствами и его применение при получении солнцезащитных составов широкого спектра действия». Фотохимия и фотобиология . 82 (3): 823–828. дои : 10.1562/2005-07-15-RA-612 . ПМИД 16492073 . S2CID 23707972 .
- ^ http://www.hallstar.com/techdocs/Polycrylene&CorapanTQAvoBenzoneStabilization.pdf [ мертвая ссылка ]
- ^ «Информационный листок о продукте: SolaStay S1» . Компания ХоллСтар. Архивировано из оригинала 2 октября 2011 года . Проверено 16 февраля 2010 г.
- ^ Ма, Хаохуа; Ван, Цзяньцян; Чжан, Вэньпей; Го, Ченг (2021). «Синтез функционализированного дипептидом фенилаланина и лейцина нанопористого материала на основе диоксида кремния в качестве безопасного УФ-фильтра для солнцезащитного крема» . Журнал золь-гель науки и технологий . 97 (2): 466–478. дои : 10.1007/s10971-020-05417-6 . S2CID 221937086 .
- ^ Скалия С., Симеони С., Барбьери А., Состеро С. (ноябрь 2002 г.). «Влияние гидроксипропил-бета-циклодекстрина на фотоиндуцированное образование свободных радикалов солнцезащитным агентом бутилметоксидибензоилметаном» . Журнал фармации и фармакологии . 54 (11): 1553–1558. дои : 10.1211/002235702207 . ПМИД 12495559 . S2CID 40228301 .
- ^ Ян Дж., Уайли С., Годвин Д., Фелтон Л. (июнь 2008 г.). «Влияние гидроксипропил-β-циклодекстрина на трансдермальное проникновение и фотостабильность авобензона». Европейский журнал фармацевтики и биофармацевтики . 69 (2): 605–612. дои : 10.1016/j.ejpb.2007.12.015 . ПМИД 18226883 .
- ^ Каваками, Камила Мартинс; Гаспар, Лорена Риго (октябрь 2015 г.). «Мангиферин и нарингенин влияют на фотостабильность и фототоксичность солнцезащитных кремов, содержащих авобензон» . Журнал фотохимии и фотобиологии B: Биология . 151 : 239–247. doi : 10.1016/j.jphotobiol.2015.08.014 . ISSN 1873-2682 . ПМИД 26318281 .
- ^ Говинду, Панчада Ч. В.; Хосамани, Басавапрабху; Мои, Смрити; Венкатачалам, Дхананджейан; Аша, Сабредди; Джон, Варун Н.; Сандип, В.; Гауд, Конкаллу Ханумаэ (01 января 2019 г.). «Глутатион как фотостабилизатор авобензона: оценка под солнечным светом, отфильтрованным стеклом, с использованием УФ-спектроскопии». Фотохимические и фотобиологические науки . 18 (1): 198–207. дои : 10.1039/c8pp00343b . ISSN 1474-9092 . ПМИД 30421772 . S2CID 53291937 .
- ^ Афонсу, С.; Хорита, К.; Соуза-э-Сильва, Япония; Алмейда, ИФ; Амарал, Миннесота; Лобао, Пенсильвания; Коста, ПК; Миранда, Маргарида С.; Эстевес да Силва, Жоаким КГ; Соуза Лобо, JM (ноябрь 2014 г.). «Фотодеградация авобензона: стабилизирующее действие антиоксидантов» . Журнал фотохимии и фотобиологии B: Биология . 140 : 36–40. doi : 10.1016/j.jphotobiol.2014.07.004 . ISSN 1873-2682 . ПМИД 25086322 .
- ^ Фрейтас, Юлиана Вескови; Лопес, Норберто Пепорин; Гаспар, Лорена Риго (12 октября 2015 г.). «Оценка фотостабильности пяти УФ-фильтров, транс-ресвератрола и бета-каротина в солнцезащитных кремах» . Европейский журнал фармацевтических наук . 78 : 79–89. дои : 10.1016/j.ejps.2015.07.004 . ISSN 1879-0720 . ПМИД 26159738 .
- ^ Уорвик Л. Морисон, доктор медицины (11 марта 2004 г.). "Светочувствительность". Медицинский журнал Новой Англии . 350 (11): 1111–1117. дои : 10.1056/NEJMcp022558 . ПМИД 15014184 .
- ^ «Солнцезащитные лекарственные препараты, отпускаемые без рецепта; маркетинговый статус продуктов, содержащих авобензон; правоприменительная политика» (PDF) . США Управление по контролю за продуктами и лекарствами . 30 апреля 1997 г. п. 23354. Архивировано (PDF) из оригинала 26 февраля 2007 г. Проверено 3 июня 2007 г.
- ^ Исследование стабильности авобензона с неорганическими солнцезащитными кремами, Плакат Kobo Products , 2001 г., онлайн-версия. Архивировано 7 мая 2007 г., на Wayback Machine.
- ^ Уэйкфилд Г., Липскомб С., Холланд Э., Ноулэнд Дж. (июль 2004 г.). «Влияние легирования марганцем на поглощение UVA и образование свободных радикалов микронизированного диоксида титана и его последствия для фотостабильности органических компонентов солнцезащитного крема, поглощающих UVA» . Фотохимия Фотобиология . 3 (7): 648–652. дои : 10.1039/b403697b . ПМИД 15238999 .
- ^ «Как удалить летние пятна с одежды» . Отчеты потребителей. 17 августа 2022 г.
- ^ «Секрет удаления пятен от солнцезащитного крема заключается в этом неожиданном чистящем средстве» . Си-Эн-Эн. 18 июля 2022 г.
- ^ Чжан Г; Лу Дж; Сабат М; Фрейзер, CL (февраль 2010 г.). «Полиморфизм и обратимая механохромная люминесценция авобензона дифторбора в твердом состоянии». Журнал Американского химического общества . 132 (7): 2160–2162. дои : 10.1021/ja9097719 . ПМИД 20108897 . S2CID 30823815 .
- ^ США 0
- ^ США 0
- ^ GJ Mturi, BS Martincigh (2008), «Фотостабильность солнцезащитного агента 4-трет-бутил-4-метоксидибензоилметана (авобензона) в растворителях различной полярности и протонности», J. Photochem. Фотобиол.: Химия , вып. 200, нет. 2–3, стр. 410–420, doi : 10.1016/j.jphotochem.2008.09.007.
