Ренилла-люциферин-2-монооксигеназа
В этой статье отсутствует информация о других белках, катализирующих эту реакцию (EC, вздох). ( ноябрь 2020 г. ) |
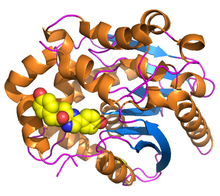
| Ренилла-люциферин-2-монооксигеназа | |||
|---|---|---|---|
 | |||
| Идентификаторы | |||
| Номер ЕС. | 1.13.12.5 | ||
| Номер CAS. | 61869-41-8 | ||
| Базы данных | |||
| ИнтЭнк | вид IntEnz | ||
| БРЕНДА | БРЕНДА запись | ||
| Экспаси | Просмотр NiceZyme | ||
| КЕГГ | КЕГГ запись | ||
| МетаЦик | метаболический путь | ||
| ПРЯМОЙ | профиль | ||
| PDB Структуры | RCSB PDB PDBe PDBsum | ||
| Генная онтология | АмиГО / QuickGO | ||
| |||
Ренилла-люциферин-2-монооксигеназа , Ренилла -люцифераза , или RLuc , представляет собой биолюминесцентный фермент, в Renilla reniformis , принадлежащем к группе целентеразинлюцифераз . обнаруженный Из этой группы ферментов люцифераза Renilla reniformis была наиболее тщательно изучена, и благодаря ее биолюминесценции, требующей только молекулярного кислорода, она имеет широкий спектр применений, включая использование в качестве зонда репортерного гена в культуре клеток, визуализации in vivo, и различные другие области биологических исследований. [ 2 ] Недавно были разработаны химеры RLuc, которые оказались самыми яркими люминесцентными белками на сегодняшний день и доказали свою эффективность как при неинвазивной визуализации отдельных клеток, так и при визуализации всего тела. [ 3 ]
Обратите внимание, что запись EC также включает другие несвязанные ферменты, которые катализируют ту же реакцию. Примером является кальций-зависимый фотопротеин экворин : хотя Rluc относится к суперсемейству гидролаз AB , экворин представляет собой белок руки EF . [ 4 ] Название не относится конкретно к Renilla , а относится к Renilla-люциферину, химическому веществу, также известному как целентеразин.
Химическая реакция
[ редактировать ]RLuc представляет собой оксидоредуктазу , специфически действующую на одиночные доноры с O 2 в качестве окислителя. Однако этот фермент, по-видимому, не связан с большинством других люцифераз, действующих на целентеразин, например, люцифераз веслоногих ракообразных . RLuc катализирует химическую реакцию
Коэлентеразин + О 2 целентерамид + CO 2 + hν
При этом целентеразин окисляется с одновременной потерей CO 2 и фотон синего света. испускается [ 5 ]
Биологическая функция
[ редактировать ]У Renilla reniformis RLuc обнаруживается в мембраносвязанных внутриклеточных структурах внутри специализированных светоизлучающих клеток. [ 6 ] [ 7 ] и связан с тесно взаимодействующим зеленым флуоресцентным белком (RrGFP), [ 8 ] и Ca ++ активированный люциферин-связывающий белок (RrLBP). [ 9 ] Хотя катализируемое люциферазой окисление целентеразина высвобождает фотон синего света (480 нм), in vivo этого не наблюдается . Вместо этого энергия, выделяемая в результате реакции с участием RLuc, передается посредством резонансной передачи энергии флуорофору RrGFP и излучается в виде зеленого фотона (505 нм). [ 10 ] что приводит к зеленой биолюминесценции, наблюдаемой у животного. Этот процесс основан на механизме резонансной передачи энергии Фёрстера (FRET), увеличивающем количество испускаемых фотонов примерно в шесть раз. [ 11 ]
Структура
[ редактировать ]Ренилла-люцифераза содержит 311 аминокислот . [ 1 ] и активен как почти сферический мономер с одной полипептидной цепью массой 36 кДа , который имеет тенденцию к самоассоциации, образуя неактивные димеры и тримеры. [ 12 ] [ 13 ] Как и другие ферменты суперсемейства дегалогеназ , он имеет в своей основе характерную последовательность α/β-гидролазы. [ 14 ] и разделяет консервативную каталитическую триаду остатков, используемых дегалогеназами . [ 15 ] В RLuc петля, содержащая остатки 153–163, является структурно гибкой, что способствует большей диффузии растворителей в активный центр, который содержит высококонсервативную каталитическую триаду , состоящую из аспарагиновой кислоты в остатке 120, глутаминовой кислоты в остатке 144 и гистидина в остатке. 285. [ 1 ]
Ферментный путь
[ редактировать ]В отличие от фотопротеинов , которые стабильно связывают целентеразин и излучают свет при добавлении кальция, целентеразин обычно связывается с RrLBP, белком, связывающим люциферин. При стимуляции Ca 2+ Ион сначала взаимодействует с RrLBP, вызывая высвобождение целентеразина. [ 9 ] Коэлентеразин затем окисляется RLuc до целентерамида один фотон , высвобождая при этом синего света (480 нм). Этот фотон захватывается соседним GFP, испуская фотон зеленого света . Этот путь кратко описан ниже.
Механизм
[ редактировать ], опосредованная RLuc Химическая реакция , включает каталитическую деградацию целентеразина и протекает через промежуточный продукт 1,2- диоксетан (также называемый диоксетаноном или циклическим пероксидом). [ 16 ] На основании исследований с использованием радиоактивно меченых форм кислорода в комплексе RLuc было установлено, что карбонильный кислород люциферина быстро заменяется кислородом из воды до включения атома кислорода из O 2 через диоксетановый промежуточный продукт. Образующийся CO 2 также быстро обменивает кислород с кислородом из окружающей воды. [ 17 ] Общий механизм изображен ниже.

Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Лёнинг А.М., Фенн Т.Д., Гамбхир СС (декабрь 2007 г.). «Кристаллические структуры люциферазы и зеленого флуоресцентного белка Renilla reniformis» . Журнал молекулярной биологии . 374 (4): 1017–28. дои : 10.1016/j.jmb.2007.09.078 . ПМК 2700051 . ПМИД 17980388 .
- ^ Даунерт, Сильвия (2006). Фотопротеины в биоанализе . Джон Уайли и сыновья.
- ^ Сайто К., Чанг Ю.Ф., Хорикава К., Хацугай Н., Хигучи Ю., Хашида М., Ёсида Ю., Мацуда Т., Араи Ю., Нагай Т. (11 декабря 2012 г.). «Люминесцентные белки для высокоскоростной визуализации отдельных клеток и всего тела» . Природные коммуникации . 3 : 1262. Бибкод : 2012NatCo...3.1262S . дои : 10.1038/ncomms2248 . ПМЦ 3535334 . ПМИД 23232392 .
- ^ MetaCyc апоэкворин-1
- ^ Шомбург, Дитмар (1994). Справочник по ферментам . Спрингер.
- ^ Андерсон Дж. М., Кормье М. Дж. (апрель 1973 г.). «Люмисомы, клеточный участок биолюминесценции кишечнополостных». Журнал биологической химии . 248 (8): 2937–43. ПМИД 4144548 .
- ^ Сперлок Б.О., Кормье М.Дж. (январь 1975 г.). «Исследование тонкой структуры антокодия Renilla mülleri. Доказательства существования биолюминесцентной органеллы, люминеллы» . Журнал клеточной биологии . 64 (1): 15–28. дои : 10.1083/jcb.64.1.15 . ПМК 2109472 . ПМИД 233975 .
- ^ Уорд WW, Кормье MJ (февраль 1979 г.). «Белок-переносчик энергии в биолюминесценции кишечнополостных. Характеристика зеленого флуоресцентного белка Renilla». Журнал биологической химии . 254 (3): 781–8. ПМИД 33175 .
- ^ Перейти обратно: а б Иноуе С. (март 2007 г.). «Экспрессия, очистка и характеристика запускаемого кальцием люциферин-связывающего белка Renilla reniformis». Экспрессия и очистка белков . 52 (1): 66–73. дои : 10.1016/j.pep.2006.07.028 . ПМИД 16997571 .
- ^ Мартель С, Дюгре-Бриссон С, Буле К, Бретон Б, Лапуант Г, Армандо С, Трепанье В, Дюшен Т, Бувье М, Дегросейлер Л (март 2010 г.). «Мультимеризация Staufen1 в живых клетках» . РНК . 16 (3): 585–97. дои : 10.1111/j.1751-1097.1978.tb07621.x . ПМЦ 2822923 . ПМИД 20075165 .
- ^ Уорд WW, Кормье MJ (сентябрь 1976 г.). «Перенос энергии in vitro в биолюминесценции Renilla». Журнал физической химии . 80 (20): 2289–91. дои : 10.1021/j100561a030 .
- ^ Мэтьюз Дж.С., Хори К., Кормье М.Дж. (январь 1977 г.). «Очистка и свойства люциферазы Renilla reniformis». Биохимия . 16 (1): 85–91. дои : 10.1021/bi00620a014 . ПМИД 12797 .
- ^ Карханис Ю.Д., Кормье М.Ю. (январь 1971 г.). «Выделение и свойства люциферазы Renilla reniformis, низкомолекулярного фермента преобразования энергии». Биохимия . 10 (2): 317–26. дои : 10.1021/bi00778a019 . ПМИД 4395343 .
- ^ Оллис Д.Л., Чеа Э., Сайглер М., Дейкстра Б., Фролов Ф., Франкен С.М., Харел М., Ремингтон С.Дж., Силман И., Шраг Дж. (апрель 1992 г.). «Складка альфа/бета-гидролазы» (PDF) . Белковая инженерия . 5 (3): 197–211. дои : 10.1093/белок/5.3.197 . hdl : 11370/2d4c057d-1a67-437d-ad10-701f7a60f1e6 . ПМИД 1409539 .
- ^ Лёнинг А.М., Фенн Т.Д., Ву А.М., Гамбхир С.С. (сентябрь 2006 г.). «Мутагенез люциферазы Renilla, управляемый консенсусом, обеспечивает повышенную стабильность и светоотдачу» . Белковая инженерия, проектирование и отбор . 19 (9): 391–400. дои : 10.1093/протеин/gzl023 . ПМИД 16857694 .
- ^ Андерсон Дж. М., Шарбонно Х., Кормье М. Дж. (март 1974 г.). «Механизм индукции кальцием биолюминесценции Renilla. Участие кальций-триггерного белка, связывающего люциферин». Биохимия . 13 (6): 1195–200. дои : 10.1021/bi00703a602 . ПМИД 4149963 .
- ^ Харт Р.К., Стемпель К.Е., Бойер П.Д., Кормье М.Дж. (апрель 1978 г.). «Механизм ферментативно-катализируемого биолюминесцентного окисления люциферина кишечнополостного типа». Связь с биохимическими и биофизическими исследованиями . 81 (3): 980–6. дои : 10.1016/0006-291X(78)91447-X . ПМИД 27179 .

![{\displaystyle RrLBP{\ce {->[{\ce {+Ca^{2+}}}]}}apoRrLBP(+Ca^{2+})+коэлентеразин}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9e740022b3d02af4cce0c187b65558ad9d30acd3)
![{\displaystyle коэлэнтеразин+O2{\ce {->[{\ce {RLuc}}]}}коэлентерамид+CO2+hv(480 нм)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b074c627fa2a1299751d41bfa8658f8092fb81ac)
![{\displaystyle hv(480nm){\ce {->[{\ce {RrGFP}}]}}hv(505nm)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cdcd4f740cf085b4cc2a4f732ffe1c8f870f078d)