EF рука
| EF рука | |||
|---|---|---|---|
 | |||
| Идентификаторы | |||
| Символ | Эфханд | ||
| Пфам | PF00036 | ||
| ИнтерПро | ИПР002048 | ||
| PROSITE | PDOC00018 | ||
| ОБЛАСТЬ ПРИМЕНЕНИЯ 2 | 1оса / СКОПе / СУПФАМ | ||
| CDD | cd00051 | ||
| |||
Рука EF представляет собой спираль-петля-спираль, структурный домен или мотив обнаруженный в большом семействе кальций-связывающих белков .
Мотив EF-рука содержит топологию спираль-петля-спираль, очень похожую на растопыренный большой и указательный пальцы человеческой руки, в которой Ca 2+ ионы координируются лигандами внутри петли. Мотив получил свое название от традиционной номенклатуры , используемой при описании белка парвальбумина , который содержит три таких мотива и, вероятно, участвует в мышечной релаксации посредством своей кальцийсвязывающей активности.
EF-рука состоит из двух альфа-спиралей, соединенных короткой петлей (обычно около 12 аминокислот ), которая обычно связывает ионы кальция . EF-руки также появляются в каждом структурном домене сигнального белка кальмодулина и в мышечном белке тропонине-С .
Сайт связывания ионов кальция
[ редактировать ]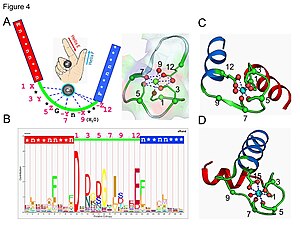
Ион кальция координирован в пятиугольной бипирамидальной конфигурации. Шесть остатков, участвующих в связывании, находятся в положениях 1, 3, 5, 7, 9 и 12; эти остатки обозначены X, Y, Z, -Y, -X и -Z. Инвариант Glu или Asp в положении 12 обеспечивает два атома кислорода для лигандирования кальция (бидентатный лиганд).
Ион кальция связан как с атомами основной цепи белка, аминокислот так и с боковыми цепями , особенно анионных аминокислотных остатков аспартата и глутамата . Эти остатки заряжены отрицательно и будут взаимодействовать с положительно заряженным ионом кальция. Мотив руки EF был одним из первых структурных мотивов, требования к последовательности которых были подробно проанализированы. Пять остатков петли связывают кальций и, таким образом, отдают предпочтение кислородсодержащим боковым цепям, особенно аспартату и глутамату. Шестой остаток в петле обязательно представляет собой глицин из-за конформационных требований основной цепи. Остальные остатки обычно гидрофобны и образуют гидрофобное ядро , которое связывает и стабилизирует две спирали.
При связывании с Ca 2+ , этот мотив может претерпевать конформационные изменения, которые позволяют Ca 2+ -регулируемые функции, как видно из Ca 2+ эффекторы, такие как кальмодулин (CaM) и тропонин C (TnC) и Ca 2+ буферы, такие как кальретикулин и кальбиндин D9k . В то время как большинство известных кальций-связывающих белков (CaBP) EF-hand содержат парные мотивы EF-hand, CaBP с одиночными EF-руками также были обнаружены как у бактерий, так и у эукариот. Кроме того, у ряда бактерий обнаружены «мотивы, подобные EF-руке». Хотя координационные свойства остаются сходными с каноническим мотивом EF-hand спираль-петля-спираль из 29 остатков, EF-hand-подобные мотивы отличаются от EF-hand тем, что они содержат отклонения во вторичной структуре фланкирующих последовательностей и/или изменение длины Ca 2+ - координационная петля.
Руки EF обладают очень высокой селективностью в отношении кальция. Например, константа диссоциации альфа- парвальбумина для Ca 2+ в ~1000 раз ниже, чем для аналогичного иона Mg 2+ . [ 2 ] Такая высокая селективность обусловлена относительно жесткой координационной геометрией, наличием множества заряженных боковых цепей аминокислот в месте связывания, а также свойствами сольватации ионов. [ 3 ] [ 4 ] [ 5 ]
Прогноз
[ редактировать ]
Поиск шаблона (подписи мотива) - один из наиболее простых способов прогнозирования непрерывного EF-рука Ca. 2+ -сайты связывания в белках. На основе результатов выравнивания последовательностей канонических мотивов EF-hand, особенно консервативных боковых цепей, непосредственно участвующих в Ca. 2+ шаблон PS50222 связывания, был создан для прогнозирования канонических сайтов EF-hand. Серверы прогнозов можно найти в разделе внешних ссылок.
Классификация
[ редактировать ]С момента определения мотива EF-hand в 1973 году семейство белков EF-hand расширилось и теперь включает по меньшей мере 66 подсемейств. Мотивы EF-рук делятся на две основные структурные группы:
- Канонические EF-руки , наблюдаемые в кальмодулине (CaM) и прокариотическом CaM-подобном белке калеритрине. Каноническая петля EF-hand из 12 остатков связывает Ca 2+ главным образом через карбоксилаты или карбонилы боковой цепи (положения петлевой последовательности 1, 3, 5, 12). Остаток на оси –X координирует Ca 2+ иона через мостиковую молекулу воды. Петля EF-hand имеет бидентатный лиганд (Glu или Asp) на оси –Z.
- Псевдо-EF-руки встречаются исключительно на N-концах S100 и S100-подобных белков. Петля псевдоEF-hand из 14 остатков хелатирует Ca 2+ преимущественно через карбонилы основной цепи (положения 1, 4, 6, 9).

Дополнительные моменты:
- EF-hand-подобные белки с разнообразными фланкирующими структурными элементами вокруг Ca 2+ -связывающая петля обнаружена у бактерий и вирусов. Эти прокариотические EF-hand-подобные белки широко вовлечены в Ca. 2+ передача сигналов и гомеостаз у бактерий. Они содержат гибкие отрезки Ca 2+ - петли для вязания, отличающиеся от мотивов EF-hand. Однако их координационные свойства напоминают классические мотивы EF-hand.
- Например, полунепрерывный Ca 2+ -Связывающий сайт в D -галактозосвязывающем белке (GBP) содержит петлю из девяти остатков. Калифорния 2+ Ион координируется семью атомами кислорода белка, пять из которых принадлежат петле, имитирующей каноническую EF-петлю, тогда как два других принадлежат карбоксилатной группе отдаленного Glu.
- Другой пример — новый домен под названием Экскалибур (внеклеточный Ca 2+ -связывающая область), выделенных из Bacillus subtilis . Этот домен имеет консервативный Ca из 10 остатков. 2+ -связывающая петля поразительно похожа на каноническую петлю EF-hand из 12 остатков.
- Разнообразие структуры фланкирующей области иллюстрируется обнаружением EF-hand-подобных доменов в бактериальных белках. Например, структура спираль-петля-цепь вместо структуры спираль-петля-спираль имеется в периплазматическом галактозосвязывающем белке ( Salmonella typhimurium , PDB : 1gcg ) или альгинатсвязывающем белке ( Sphingomonas sp ., 1kwh ); входящая спираль отсутствует у защитного антигена ( Bacillus anthracis , 1acc ) или докерина ( Clostridium thermocellum , 1daq ).
Среди всех структур, о которых сообщалось на сегодняшний день, большинство мотивов EF-руки спарены либо между двумя каноническими, либо между одним псевдо- и одним каноническим мотивом. Для белков с нечетным числом EF-рук, таких как пента-EF-рука кальпаин, мотивы EF-рук соединялись посредством гомо- или гетеродимеризации. Недавно обнаруженная EF-рука, содержащая ER Ca. 2+ Было показано, что сенсорный белок, молекулы стромального взаимодействия 1 и 2 (STIM1, STIM2), содержит Ca 2+ -связывающий канонический мотив EF-руки, который сочетается с непосредственным, последующим атипичным «скрытым» не-Ca 2+ -связывание EF-руки. Одиночные мотивы EF-hand могут служить модулями стыковки белков: например, одиночная EF-рука в белках NKD1 и NKD2 связывает белки Disheveled (DVL1, DVL2, DVL3).
Функционально EF-руки можно разделить на два класса:
- сигнальные белки
- буферные/транспортные белки.
Первая группа является самой крупной и включает в себя наиболее известные представители семейства, такие как кальмодулин, тропонин С и S100B. Эти белки обычно претерпевают кальций-зависимые конформационные изменения, которые открывают целевой сайт связывания. Последняя группа представлена кальбиндином D9k и эти белки не претерпевают кальцийзависимых конформационных изменений.
Подсемейства
[ редактировать ]Примеры
[ редактировать ]Экворин
[ редактировать ]Экворин представляет собой кальцийсвязывающий белок (CaBP), выделенный из книдарий Aequorea victoria . Экворин принадлежит к семейству CaBP EF-hand с петлями EF-hand, которые тесно связаны с CaBP у млекопитающих. Кроме того, экворин уже много лет используется в качестве индикатора Ca. 2+ и было показано, что он безопасен и хорошо переносится клетками. Экворин состоит из двух компонентов – кальцийсвязывающего компонента апоаекворина (AQ) и хемилюминесцентной молекулы целентеразина . Часть AQ этого белка содержит кальцийсвязывающие домены EF-hand. [ 6 ]
Белки человека
[ редактировать ]Белки человека, содержащие этот домен, включают:
- АКТН1 ; АКТН2 ; АКТН3 ; АКТН4 ; APBA2BP ; АЙТЛ1 ; АЙТЛ2
- C14orf143 ; САВР1 ; САВР2 ; САВР3 ; САВР4 ; САВР5 ; CABP7 ; КАЛБ1 ; КАЛБ2 ; СПОКОЙНО2 ; СПОКОЙНО3 ; КАЛМЛ3 ; КАЛМЛ4 ; КАЛМЛ5 ; КАЛМЛ6 ; КАЛН1 ; КАЛУ ; КАПН1 ; КАПН11 ; КАПН2 ; КАПН3 ; КАПН9 ; КАПНС1 ; КАПНС2 ; ЗАГЛАВНЫЕ ; КАПС2 ; КАПСЛ ; КБАРА1 ; ЦЕТН1 ; ЦЕТН2 ; ЦЕТН3 ; ТЭЦ ; ТЭЦ2 ; КИБ1 ; КИБ2 ; КИБ3 ; КИБ4 ; ЦРНН
- ДГКА ; ДГКБ ; ДГКГ ; летнее время ; ДУОКС1 ; ДУОКС2
- ЕФКАБ1 ; ЕФКАБ2 ; ЕФКАБ4А ; EFCAB4B ; ЕФКАБ6 ; ЕФКБП1 ; ЕФКБП2 ; ЕФХА1 ; ЕФХА2 ; ЭФХБ ; ЭФХК1 ; ЭФХД1 ; ЭФХД2 ; EPS15 ; ЭПС15Л1
- ФКБП10 ; ФКБП14 ; ФКБП7 ; ФКБП9 ; ФКБП9Л ; ЧАСТОТА ; ФСТЛ1 ; ФСТЛ5
- ГКА ; ГПД2 ; ГУЦА1А ; ГУКА1Б ; GUCA1C
- гиппокальцин ; HPCAL1 ; HPCAL4 ; ХЗГЖ
- ИФПС ; ИТСН1 ; ИТСН2 ; КЦНИП1 ; КЦНИП2 ; КЦНИП3 ; КЦНИП4 ; КИАА1799
- ЛКП1
- МАКФ1 ; МРЛЦ2 ; МРЛЦ3 ; МСТ133 ; МИЛ1 ; МИЛ2 ; МИЛ5 ; МИЛ6Б ; МИЛ7 ; МИЛ9 ; МИЛК2ПЛ ; МИЛПФ
- НКАЛД ; НИН ; НКД1 ; НКД2 ; НЛП ; НОКС5 ; НУСБ1 ; НУСБ2
- ОКМ
- ПДКД6 ; ПЭФ1 ; ПКД2 ; ПЛКД1 ; ПЛКД4 ; ПЛЧ1 ; ПЛЧ2 ; ПЛС1 ; ПЛС3 ; ПП1187 ; ППЭФ1 ; ППЭФ2 ; ППП3Р1 ; ППП3Р2 ; ПРККШ ; ПВАЛБ
- РАБ11ФИП3 ; РАСЕФ ; РАСГРП ; РАСГРП1 ; РАСГРП2 ; РАСГРП3 ; РЦН1 ; РЦН2 ; РЦН3 ; РКВ1 ; РКВРН ; РЕПС1 ; РХБДЛ3 ; РОТ1 ; РОТ2 ; РПТН ; РИР2 ; РИР3
- С100А1 ; С100А11 ; С100А12 ; С100А6 ; С100А8 ; С100А9 ; С100Б ; С100Г ; С100З ; СКАМЦ-2 ; СКГН ; СКН5А ; СДФ4 ; СЛК25А12 ; СЛК25А13 ; СЛК25А23 ; СЛК25А24 ; СЛК25А25 ; СПАТА21 ; ЗИП1 ; СПТАН1 ; НИИ
- ТБС1D9 ; ТБС1D9B ; ТЧХ ; ТЭСК ; ТННК1 ; ТННК2
- USP32
- ВСНЛ1
- ЗЗЕФ1
См. также
[ редактировать ]- Другим отличительным кальций-связывающим мотивом, состоящим из альфа-спиралей, является домен докерина .
Ссылки
[ редактировать ]- ^ Бан С., Рамакришнан Б., Линг К.Ю., Кунг С., Сундаралингам М. (январь 1994 г.). «Структура рекомбинантного кальмодулина Paramecium тетраурелия при разрешении 1,68 А». Акта Кристаллогр. Д. 50 (Часть 1): 50–63. дои : 10.1107/S0907444993007991 . ПМИД 15299476 .
- ^ Шваллер, Б. (13 октября 2010 г.). «Цитозольные Са2+-буферы» . Перспективы Колд-Спринг-Харбор в биологии . 2 (11): а004051. doi : 10.1101/cshperspect.a004051 . ПМК 2964180 . ПМИД 20943758 .
- ^ Гиффорд, Джессика Л.; Уолш, Майкл П.; Фогель, Ханс Дж. (15 июля 2007 г.). «Структура и свойства связывания ионов металлов Ca-связывающих мотивов спираль-петля-спираль EF-hand». Биохимический журнал . 405 (2): 199–221. дои : 10.1042/BJ20070255 . ПМИД 17590154 .
- ^ Дудев, Тодор; Лим, Кармей (16 сентября 2013 г.). «Конкуренция между ионами металлов за места связывания с белками: факторы, определяющие селективность ионов металлов в белках». Химические обзоры . 114 (1): 538–556. дои : 10.1021/cr4004665 . ПМИД 24040963 .
- ^ Цзин, Чжифэн; Лю, Чэнвэнь; Ци, Руи; Рен, Пэнъюй (23 июля 2018 г.). «Эффект многих тел определяет селективность в отношении кальция и магния в белках» . Труды Национальной академии наук . 115 (32): Е7495–Е7501. дои : 10.1073/pnas.1805049115 . ПМК 6094099 . ПМИД 30038003 .
- ^ Детерт Дж.А., Адамс Э.Л., Лешер Дж.Д., Лайонс Дж.А., Мойер Дж.Р. (2013). «Предварительная обработка апоаекворином защищает нейроны CA1 гиппокампа от кислородно-глюкозной депривации» . ПЛОС ОДИН . 8 (11): е79002. дои : 10.1371/journal.pone.0079002 . ПМЦ 3823939 . ПМИД 24244400 .
Дальнейшее чтение
[ редактировать ]- Брэнден С., Туз Дж. (1999). «Глава 2: Мотивы структуры белка». Введение в структуру белка . Нью-Йорк: Паб Garland. стр. 24–25. ISBN 0-8153-2305-0 .
- Накаяма С., Крецингер Р.Х. (1994). «Эволюция семейства белков EF-hand». Annu Rev Biophys Biomol Struct . 23 : 473–507. дои : 10.1146/annurev.bb.23.060194.002353 . ПМИД 7919790 .
- Чжоу Ю, Ян В., Кирбергер М., Ли Х.В., Аяласомаяджула Г., Ян Дж.Дж. (ноябрь 2006 г.). «Прогнозирование кальцийсвязывающих белков EF-руки и анализ бактериальных белков EF-руки». Белки . 65 (3): 643–55. дои : 10.1002/прот.21139 . ПМИД 16981205 . S2CID 8904181 .
- Чжоу Ю, Фрей Т.К., Ян Дж.Дж. (июль 2009 г.). «Вирусная кальциомика: взаимодействие между Ca2+ и вирусом» . Клеточный кальций . 46 (1): 1–17. дои : 10.1016/j.ceca.2009.05.005 . ПМК 3449087 . ПМИД 19535138 .
- Накаяма С., Монкриф Н.Д., Крецингер Р.Х. (май 1992 г.). «Эволюция белков, модулированных кальцием EF-hand. II. Домены нескольких подсемейств имеют разнообразную эволюционную историю». Дж. Мол. Эвол . 34 (5): 416–48. дои : 10.1007/BF00162998 . ПМИД 1602495 . S2CID 34614223 .
- Хог CW, Макманус Дж.П., Банвиль Д., Сабо А.Г. (июль 1992 г.). «Сравнение усиления люминесценции тербия (III) у мутантов EF-белков, связывающих кальций» . Ж. Биол. Хим . 267 (19): 13340–7. дои : 10.1016/S0021-9258(18)42216-8 . ПМИД 1618836 .
- Байрох А., Кокс Дж.А. (сентябрь 1990 г.). «Мотивы EF-hand в инозитолфосфолипид-специфической фосфолипазе C» . ФЭБС Летт . 269 (2): 454–6. дои : 10.1016/0014-5793(90)81214-9 . ПМИД 2401372 .
- Финн Б.Е., Форсен С. (январь 1995 г.). «Развивающаяся модель структуры, функции и активации кальмодулина» . Структура . 3 (1): 7–11. дои : 10.1016/S0969-2126(01)00130-7 . ПМИД 7743133 .
- Статопулос П.Б., Чжэн Л., Ли Г.Ю., Плевин М.Дж., Икура М. (октябрь 2008 г.). «Структурное и механистическое понимание STIM1-опосредованной инициации поступления кальция в депо» . Клетка . 135 (1): 110–22. дои : 10.1016/j.cell.2008.08.006 . ПМИД 18854159 .
- Нельсон М.Р., Тулин Э., Фаган П.А., Форсен С., Чазин В.Дж. (февраль 2002 г.). «Домен EF-hand: глобально кооперативная структурная единица» . Белковая наука . 11 (2): 198–205. дои : 10.1110/ps.33302 . ПМЦ 2373453 . ПМИД 11790829 .
Внешние ссылки
[ редактировать ]- ресурсов Eukaryotic Linear Motif Класс мотивов LIG_EH_1
- ресурсов Eukaryotic Linear Motif Класс мотивов LIG_IQ
- ресурса Eukaryotic Linear Motif Класс мотива DOC_PP2B_LxvP_1
- ресурсов Eukaryotic Linear Motif Класс мотивов LIG_IQ
- Нельсон М., Чазин В. «Библиотека данных EF-Hand по кальцийсвязывающим белкам» . Университет Вандербильта . Проверено 29 августа 2009 г.
- Хайек Дж. «База данных белков EF-hand (EF-handome)» . Европейское кальциевое общество и Свободный университет Брюсселя . Проверено 29 августа 2009 г.
по запросу на [email protected]
- Ян Дж. «Кальциомика» . Государственный университет Джорджии. Архивировано из оригинала 12 октября 2009 г. Проверено 29 августа 2009 г.
сервер прогнозирования для кальцийсвязывающих белков EF-hand