Лабораторная диагностика вирусных инфекций
| Лабораторная диагностика вирусных инфекций | |
|---|---|
| Цель | тест на вирусную инфекцию |
В диагностической лаборатории вирусные инфекции можно подтвердить множеством методов. Диагностическая вирусология быстро изменилась благодаря появлению молекулярных методов и повышению клинической чувствительности серологических анализов. [1]
Выборка
[ редактировать ]Для вирусологического тестирования можно использовать самые разнообразные образцы. Тип образца, отправляемого в лабораторию, часто зависит от типа диагностируемой вирусной инфекции и требуемого анализа. Правильная техника отбора проб необходима во избежание потенциальных преаналитических ошибок. Например, различные типы образцов необходимо собирать в соответствующие пробирки, чтобы сохранить целостность образца, и хранить при соответствующих температурах (обычно 4 °C), чтобы сохранить вирус и предотвратить рост бактерий или грибков. Иногда можно также выбрать несколько сайтов. [ нужна ссылка ]
Типы образцов включают следующее:
- Мазок из носоглотки
- Кровь
- Кожа
- Мокрота , полоскания и промывания бронхов
- Моча
- сперма
- Кал
- Цереброспинальная жидкость
- Ткани ( биопсия или вскрытие )
- Засохшие пятна крови
Например, для диагностики риновируса можно провести анализ носовой слизи. [2]
Выделение вируса
[ редактировать ]Вирусы часто выделяют из первоначального образца пациента. Это позволяет выращивать образцы вируса в больших количествах и проводить с ними большее количество тестов. Это особенно важно для образцов, содержащих новые или редкие вирусы, для которых еще не разработаны диагностические тесты. [ нужна ссылка ]
Многие вирусы можно выращивать в культуре клеток в лаборатории. Для этого образец вируса смешивается с клетками (процесс, называемый адсорбцией) , после чего клетки заражаются и производят больше копий вируса. [3] Хотя различные вирусы часто растут только в определенных типах клеток, существуют клетки, которые поддерживают рост большого количества вирусов и являются хорошей отправной точкой, например, линия клеток почек африканской обезьяны ( клетки Vero ), фибробласты легких человека (клетки Vero). MRC-5 ) и клетки эпидермоидной карциномы человека ( HEp-2 ). Одним из способов определения того, успешно ли клетки реплицируют вирус, является проверка изменения морфологии клеток или наличия гибели клеток с помощью микроскопа.
Другие вирусы могут потребовать альтернативных методов роста, таких как инокуляция куриных яиц с эмбрионами (например, вирусы птичьего гриппа [4] ) или внутричерепная инокуляция вируса новорожденным мышам (например, лиссавирусы [5] ).
Методы на основе нуклеиновых кислот
[ редактировать ]Молекулярные методы являются наиболее специфичными и чувствительными диагностическими тестами. [6] Они способны обнаруживать либо весь вирусный геном, либо его части. В прошлом тесты на нуклеиновые кислоты в основном использовались в качестве вторичного теста для подтверждения положительных серологических результатов. [3] Однако по мере того, как они становятся более дешевыми и автоматизированными, они все чаще становятся основным инструментом диагностики, а также могут использоваться для мониторинга лечения вирусноинфицированных лиц, т.е. [3]
Полимеразная цепная реакция
[ редактировать ]Обнаружение вирусных РНК и ДНК-геномов можно проводить с помощью полимеразной цепной реакции . Этот метод позволяет создавать множество копий генома вируса с использованием вирус-специфичных зондов. Варианты ПЦР, такие как ПЦР с вложенной обратной транскриптазой и ПЦР в реальном времени, также могут использоваться для определения вирусной нагрузки в сыворотке пациентов. Это часто используется для мониторинга успеха лечения в случаях ВИЧ . [ нужна ссылка ]
Секвенирование
[ редактировать ]Секвенирование — единственный диагностический метод, позволяющий получить полную последовательность генома вируса. Следовательно, он предоставляет больше информации об очень небольших различиях между двумя вирусами, которые при использовании других диагностических тестов выглядели бы одинаково. В настоящее время он используется только тогда, когда требуется такая глубина информации. Например, секвенирование полезно при проверке конкретных мутаций у пациента с целью определения противовирусной терапии и восприимчивости к инфекции. Однако, поскольку тесты становятся дешевле, быстрее и автоматизированнее, секвенирование, вероятно, станет основным диагностическим инструментом в будущем. [ нужна ссылка ]
Методы на основе микроскопии
[ редактировать ]Иммунофлуоресценция или иммунопероксидаза
[ редактировать ]иммунофлуоресцентный или иммунопероксидазный Для обнаружения присутствия вируса в образце ткани обычно используются анализы. Эти тесты основаны на том принципе, что если ткань заражена вирусом, антитело, специфичное к этому вирусу, сможет с ним связаться. Для этого с образцом ткани смешивают антитела, специфичные к разным типам вирусов. После того, как ткань подвергается воздействию света определенной длины волны или химического вещества, позволяющего визуализировать антитела. [ нужна ссылка ]
Для этих тестов требуются специализированные антитела, которые производятся и приобретаются у коммерческих компаний. Эти коммерческие антитела обычно хорошо охарактеризованы и, как известно, связываются только с одним конкретным типом вируса. Они также конъюгированы со специальной меткой, которая позволяет визуализировать антитело в лаборатории, то есть излучать флуоресценцию или цвет. Следовательно, иммунофлуоресценция относится кк обнаружению флуоресцентных антител (иммуно) и иммунопероксидазы относится к обнаружению окрашенных антител (пероксидаза дает темно-коричневый цвет). [ нужна ссылка ]
| Иммунофлуоресцентный анализ | Иммунопероксидазный анализ |
|---|---|
Электронная микроскопия
[ редактировать ]Электронная микроскопия — это метод, позволяющий получить изображение целого вируса и выявить его форму и структуру. Обычно его не используют в качестве рутинного диагностического теста, поскольку он требует узкоспециализированной подготовки проб, микроскопа и технических знаний. Однако электронная микроскопия очень универсальна благодаря своей способности анализировать любой тип образца и идентифицировать любой тип вируса. Таким образом, он остается золотым стандартом для выявления вирусов, которые не обнаруживаются при рутинных диагностических тестах или для которых рутинные тесты дают противоречивые результаты. [7]
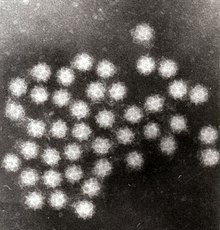 |
Обнаружение антител хозяина
[ редактировать ]У человека, недавно заразившегося вирусом, в кровотоке вырабатываются антитела, которые специфически распознают этот вирус. Это называется гуморальным иммунитетом . Важны два типа антител. Первый, называемый IgM, очень эффективен при нейтрализации вирусов, но вырабатывается клетками иммунной системы только в течение нескольких недель. Второй, называемый IgG , вырабатывается неопределенно долго. Таким образом, наличие IgM в крови хозяина используется для проверки острой инфекции, тогда как IgG указывает на инфекцию когда-то в прошлом. [8] Оба типа антител измеряются при тестов на иммунитет . проведении [9]
Тестирование на антитела стало широко доступным. Это можно сделать для отдельных вирусов (например, с помощью анализа ELISA), но все большее распространение получают автоматизированные панели, которые могут одновременно проверять множество вирусов. [ нужна ссылка ]
Анализ гемагглютинации
[ редактировать ]Некоторые вирусы прикрепляются к молекулам, присутствующим на поверхности эритроцитов, например, вирус гриппа. [10] Следствием этого является то, что – при определенных концентрациях – вирусная суспензия может связывать ( агглютинировать ) эритроциты, предотвращая тем самым их осаждение из суспензии. [ нужна ссылка ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Лиланд, Д.С.; Гиноккио, CC (2007). «Роль клеточной культуры для обнаружения вирусов в век технологий» . Обзоры клинической микробиологии . 20 (1): 49–78. дои : 10.1128/CMR.00002-06 . ПМК 1797634 . ПМИД 17223623 .
- ^ Гуолтни Дж. М., Хайден Ф. Г. (февраль 1992 г.). «Психологический стресс и простуда». N Engl J Med . 326 (9): 644–5, ответ автора 645–6. дои : 10.1056/NEJM199202273260915 . ПМИД 1310349 .
- ^ Jump up to: а б с «Методы диагностики в вирусологии, вирусологические методы, культура вирусов, выделение вирусов» . virology-online.com . Проверено 3 января 2018 г.
- ^ Брауэр, Рена; Чен, Питер (2015). «Размножение вируса гриппа в куриных яйцах с эмбрионами» . Журнал визуализированных экспериментов (97). дои : 10.3791/52421 . ПМК 4401370 . ПМИД 25867050 .
- ^ Кузьмин, Иван В. (2015). «Выделение вирусов у животных». Современные лабораторные методы диагностики, исследований и профилактики бешенства, Том 2 . стр. 13–23. дои : 10.1016/B978-0-12-801919-1.00002-6 . ISBN 9780128019191 .
- ^ Дхамад, А.Е.; Абдал Рида, Массачусетс (2020). «COVID-19: молекулярные и серологические методы обнаружения» . ПерДж . 8 : е10180. дои : 10.7717/peerj.10180 . ПМЦ 7547594 . ПМИД 33083156 .
- ^ Хейзелтон, Пол Р.; Гелдерблом, Ханс Р. (2003). «Электронная микроскопия для быстрой диагностики новых инфекционных агентов1» . Новые инфекционные заболевания . 9 (3): 294–303. дои : 10.3201/eid0903.020327 . ПМЦ 2958539 . ПМИД 12643823 .
- ^ Грир, Шон; Александр, Грэм Дж. М. (1995). «4 Вирусная серология и обнаружение». Клиническая гастроэнтерология Байера . 9 (4): 689–721. дои : 10.1016/0950-3528(95)90057-8 . ПМИД 8903801 .
- ^ Лоуренс, Джеффри С. (2005). «Иммунизация против гепатита А и В лиц, инфицированных вирусом иммунодефицита человека». Американский медицинский журнал . 118 (10): 75–83. doi : 10.1016/j.amjmed.2005.07.024 . ПМИД 16271546 .
- ^ «Анализ торможения гемагглютинации при гриппе» . www.virology.ws . Проверено 19 октября 2020 г.
