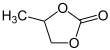
Пропиленкарбонат
| |||

| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
4-Метил-1,3-диоксолан-2-он | |||
| Другие имена
( RS )-4-Метил-1,3-диоксолан-2-он
Циклический пропиленкарбонат Эфир пропилена угольной кислоты Циклический 1,2-пропиленкарбонат Циклический карбонат пропиленгликоля 1,2-Пропандиол карбонат 4-Метил-2-оксо-1,3-диоксолан Арконат 5000 Техасар ПК | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.003.248 | ||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| C4H6OC4H6O3 | |||
| Молярная масса | 102.089 g·mol −1 | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 1,205 г/см 3 | ||
| Температура плавления | -48,8 ° C (-55,8 ° F; 224,3 К) | ||
| Точка кипения | 242 ° С (468 ° F; 515 К) | ||
| Очень растворим (240 г/л при 20°C) | |||
Показатель преломления ( n D )
|
1.4189 | ||
| Структура | |||
| 4,9 Д | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности
|
Раздражающий | ||
| СГС Маркировка : [ 3 ] | |||

| |||
| Предупреждение | |||
| H319 | |||
| П305+П351+П338 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 132 ° С (270 ° F; 405 К) | ||
| 455 ° С (851 ° F; 728 К) | |||
| Паспорт безопасности (SDS) | Паспорт безопасности от Mallinckrodt Baker | ||
| Родственные соединения | |||
Родственные соединения
|
Этиленкарбонат Диметилкарбонат | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Пропиленкарбонат (часто сокращенно PC ) представляет собой органическое соединение с формулой C 4 H 6 O 3 . Это циклический эфир карбоната, полученный из пропиленгликоля . [ 4 ] Эта бесцветная жидкость без запаха полезна в качестве полярного апротонного растворителя . [ 5 ] Пропиленкарбонат является хиральным , но в большинстве случаев используется как рацемическая смесь .
Подготовка
[ редактировать ]Хотя многие органические карбонаты производятся с использованием фосгена , пропилен и этиленкарбонаты являются исключениями. В основном их получают путем карбонизации эпоксидов . [ 5 ] (здесь эпоксипропан или оксид пропилена ):
- СН 3 СН 2 О + СО 2 → СН 3 С 2 Н 3 О 2 СО
Этот процесс особенно привлекателен, поскольку при производстве этих эпоксидов потребляется углекислый газ. Таким образом, эта реакция является хорошим примером зеленого процесса. Соответствующая реакция 1,2-пропандиола с фосгеном является сложной и приводит не только к пропиленкарбонату, но и к олигомерным продуктам.
Пропиленкарбонат также можно синтезировать из мочевины и пропиленгликоля над ацетатом цинка . [ 6 ]
Приложения
[ редактировать ]В качестве растворителя
[ редактировать ]Пропиленкарбонат используется в качестве полярного апротонного растворителя. [ 7 ] Он имеет высокий молекулярный дипольный момент (4,9 Д ), что значительно выше, чем у ацетона (2,91 Д ) и этилацетата (1,78 Д ). [ 1 ] Можно, например, получить их хлоридов и других солей , калий, натрий и другие щелочные металлы электролизом растворенных в пропиленкарбонате. [ 8 ]
Электролит
[ редактировать ]Из-за своей высокой относительной диэлектрической проницаемости (диэлектрической проницаемости), равной 64, он часто используется в качестве с высокой диэлектрической проницаемостью компонента электролитов в литиевых батареях , обычно вместе с растворителем низкой вязкости (например, диметоксиэтаном ). Его высокая полярность позволяет ему создавать эффективную сольватную оболочку вокруг ионов лития, тем самым создавая проводящий электролит . Однако он не используется в литий-ионных аккумуляторах из-за его разрушительного воздействия на графит . [ 9 ]
Другой
[ редактировать ]Пропиленкарбонат также можно найти в некоторых клеях , средствах для снятия краски и в косметике . [ 10 ] Он также используется в качестве пластификатора . Пропиленкарбонат также используется в качестве растворителя для удаления CO 2 из природного газа и синтез-газа, в которых H 2 также отсутствует S. Это использование было разработано компаниями El Paso Natural Gas Company и Fluor Corporation в 1950-х годах для использования на газовом заводе округа Террелл в Западном Техасе, который сейчас принадлежит Occidental Petroleum. [ 11 ]
Продукт пропиленкарбоната можно преобразовать в другие сложные эфиры карбоната путем переэтерификации также (см. Эфир карбоната # Переэтерификация карбоната ). [ 5 ]
В масс-спектрометрии с ионизацией электрораспылением пропиленкарбонат легируют в растворы с низким поверхностным натяжением для увеличения заряда аналита. [ 12 ]
В реакции Гриньяра пропиленкарбонат (или большинство других сложных эфиров карбонатов) можно использовать для создания третичных спиртов . [ 13 ]
Безопасность
[ редактировать ]Клинические исследования показывают, что пропиленкарбонат не вызывает раздражения или сенсибилизации кожи при использовании в косметических препаратах, тогда как при использовании в неразбавленном виде наблюдается умеренное раздражение кожи. Никаких существенных токсических эффектов не наблюдалось у крыс, которых кормили пропиленкарбонатом, подвергали воздействию паров или неразбавленной жидкости. [ 14 ] В США пропиленкарбонат не регулируется как летучее органическое соединение (ЛОС), поскольку он не вносит существенного вклада в образование смога и поскольку неизвестно или не предполагается, что его пары вызывают рак или другие токсические эффекты. [ 15 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б Хейнс, Уильям М., изд. (2011). Справочник CRC по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press . ISBN 1-4398-5511-0 .
- ^ Пропиленкарбонат в Sigma-Aldrich .
- ^ СГС: ГЕСТИС 070730.
- ^ Страница веб-книги по пропиленкарбонату .
- ^ Jump up to: а б с Ханс-Йозеф Буйш. «Эфиры угольной кислоты». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a05_197 . ISBN 978-3527306732 . .
- ^ Синтез пропиленкарбоната из мочевины http://pubs.acs.org/doi/abs/10.1021/ie049948i
- ^ Дитер Стой. «Растворители». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a24_437 . ISBN 978-3527306732 . .
- ^ Ж. Йорне; CW Тобиас (1975). «Электроосаждение щелочных металлов из пропиленкарбоната» . Дж. Прил. Электрохим . 5 (4): 279–290. дои : 10.1007/BF00608791 . S2CID 93629501 .
- ^ Дорон Аурбах (1999). Неводная электрохимия . ЦРК Пресс. ISBN 978-0824773342 .
- ^ Пропиленкарбонат в базе данных информации о потребительских товарах .
- ^ Шендель, Р. «Сравнение процессов с фторсодержащими растворителями и селексолом» (PDF) . Проверено 4 апреля 2016 г.
- ^ Тео Калифорния, Дональд Вашингтон (май 2014 г.). «Добавки в раствор для повышения заряда белков сверх теоретического максимального предела переноса протона в масс-спектрометрии с ионизацией электрораспылением». Анальный. Хим . 86 (9): 4455–62. дои : 10.1021/ac500304r . ПМИД 24712886 .
- ^ Пейн, Ричард; Теодору, Игнатий Э. (сентябрь 1972 г.). «Диэлектрические свойства и релаксация в этиленкарбонате и пропиленкарбонате» . Журнал физической химии . 76 (20): 2892–2900. дои : 10.1021/j100664a019 . ISSN 0022-3654 .
- ^ «Экологический профиль пропиленкарбоната» . Агентство по охране окружающей среды США. 1998.
- ^ Джонсон, Уильям Л. «ПЕРЕСМОТР ОПРЕДЕЛЕНИЯ ЛЕТУЧИХ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ – ИСКЛЮЧЕНИЕ ПРОПИЛЕНОВОГО КАРБОНАТА И ДИМЕТИЛКАРБОНАТА» . Агентство по охране окружающей среды США . Агентство по охране окружающей среды США . Проверено 11 июля 2015 г.