3-меркаптопируватсертрансфераза
| 3-меркаптопируватсертрансфераза | |||
|---|---|---|---|
 | |||
| Идентификаторы | |||
| Номер ЕС. | 2.8.1.2 | ||
| Номер CAS. | 9026-05-5 | ||
| Базы данных | |||
| ИнтЭнк | вид IntEnz | ||
| БРЕНДА | БРЕНДА запись | ||
| Экспаси | Просмотр NiceZyme | ||
| КЕГГ | КЕГГ запись | ||
| МетаЦик | метаболический путь | ||
| ПРЯМОЙ | профиль | ||
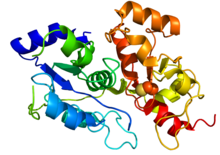
| PDB Структуры | RCSB PDB PDBe PDBsum | ||
| Генная онтология | АмиГО / QuickGO | ||
| |||
| 3-меркаптопируватсертрансфераза | |||
|---|---|---|---|
| Идентификаторы | |||
| Символ | МПСТ | ||
| Альт. символы | МСТ, ТСТ2, ТУМ1 | ||
| Альт. имена | Роданская печень человека | ||
| ген NCBI | 4357 | ||
| HGNC | 7223 | ||
| МОЙ БОГ | 602496 | ||
| ПДБ | 3ОЛХ | ||
| RefSeq | НП_066949 | ||
| ЮниПрот | P25325 | ||
| Другие данные | |||
| Номер ЕС | 2.8.1.2 | ||
| Локус | 22 q123 | ||
| |||
В энзимологии 3 -меркаптопируватсульфераза ( EC 2.8.1.2 ) — фермент химические , катализирующий реакции 3 меркаптопирувата - . Этот фермент принадлежит к семейству трансфераз , в частности серотрансфераз. [ 1 ] Этот фермент участвует в метаболизме цистеина . Он кодируется MPST геном . [ 2 ]
Фермент представляет интерес, поскольку обеспечивает путь детоксикации цианида , особенно потому, что он широко встречается в цитозоле и широко распределяется. [ 3 ]
Номенклатура
[ редактировать ]Систематическое название этого класса ферментов — 3-меркаптопируват:цианидсертрансфераза. Этот фермент также называют бета-меркаптопируватсульфотрансферазой, а в более старой литературе — роданезом печени человека. [ 4 ]
Структура
[ редактировать ]Ген
[ редактировать ]Ген MPST расположен в хромосоме 22q12.3 и состоит из 6 экзонов . Альтернативно сплайсированные варианты транскриптов, кодирующие один и тот же белок, были идентифицированы. [ 2 ] [ 5 ]
Белок
[ редактировать ]Кодируемый цитоплазматический белок является членом семейства роданезы, но сам по себе не является роданезой, которая обнаруживается только в митохондриях. Белок MPST состоит из 317 аминокислотных остатков и весит 35250 Да. MPST содержит два роданских домена со схожими вторичными структурами, что позволяет предположить общее эволюционное происхождение. Каталитический остаток цистеина существует только в С-концевом роданезном домене. Белок может функционировать как мономер или как гомодимер с дисульфидной связью.
Функция и механизм
[ редактировать ]Биологическая функция MPST остается неясной. Он может участвовать в детоксикации цианидов, биосинтезе тиосульфата, производстве сигнальной молекулы сероводорода или деградации цистеина.
MPST реагирует с 3-MP, превращая цистеинильный остаток в персульфидсодержащий промежуточный продукт: [ 3 ]
- РШ + ХЩ 2 C(O)CO 2 − → РСШ + CH 3 C(O)CO 2 −
Персульфидная группа лабильна и может передавать S другим группам, таким как цианид. Он также подвержен восстановлению с выделением сероводорода .
H 2 S производится из l-цистеина с помощью цистатионин-γ-лиазы (CSE) и MPST. Зависимое от l-цистеина производство H 2 S с помощью MPST представляет собой двухстадийную реакцию. На первом этапе цистеинтрансаминаза превращает L-цистеин вместе с α-кетоглутаратом в 3-меркаптопируват (3-МП). Впоследствии MPST преобразует 3-MP в H 2 S. [ 6 ] MPST катализирует перенос атома серы от меркаптопирувата к акцепторам серы, таким как цианиды или тиоловые соединения. [ 7 ] Таким образом, считается, что он также участвует в деградации цистеина. [ 5 ] MPST генерирует H 2 S в коронарной артерии , опосредуя свои эффекты посредством прямой модуляции NO , а именно вазодилатации. Это имеет важное значение для терапии на основе H 2 S в здоровых и больных коронарных артериях. [ 8 ]
Биологическое значение
[ редактировать ]MPST экспрессируется в ряде тканей, включая почки, печень, легкие, сердце, мышцы, селезенку и мозг. [ 9 ] [ 10 ] [ 11 ]
3- Меркаптопируват (3-МП) вместе с α-кетоглутаратом образуется из цистеина под действием аминотрансферазы . Таким образом, MPST может участвовать в деградации цистеина.
Биомедицинский
[ редактировать ]Производство сероводорода
[ редактировать ]H 2 S производится из MPST (а также с помощью цистатионин-γ-лиазы ). [ 6 ] [ 1 ] MPST генерирует H 2 S в коронарной артерии , опосредуя свои эффекты посредством прямой модуляции NO , а именно вазодилатации. Это имеет важное значение для терапии на основе H 2 S в здоровых и больных коронарных артериях. [ 8 ]
Меркаптолактат-цистеиновая дисульфидурия
[ редактировать ]Дефицит MPST был обнаружен в связи с дисульфидурией меркаптолактат-цистеина (или синдромом Амполы ), редким наследственным заболеванием, связанным с чрезмерной секрецией дисульфида меркаптолактат-цистеина в моче. [ 12 ] этим редким заболеванием страдают менее 1000 человек В Соединенных Штатах . [ 13 ] Симптомы и признаки включают: высокий лоб, судороги, арахнодактилию , вальгумное колено , гиполазию ушного хряща и пупочная грыжа.
Рак мочевого пузыря
[ редактировать ]Иммунореактивность к MPST была обнаружена в образцах злокачественного уроэпителия и мышечного слоя рака мочевого пузыря . Уровни белка и каталитическая активность MPST повышались с увеличением степени злокачественности тканей мочевого пузыря человека и клеточных линий уротелиально-клеточной карциномы мочевого пузыря (UCB), и это может способствовать применению новых ферментов MPST для диагностики или лечения UCB. [ 14 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Ядав П.К., Ямада К., Чику Т., Кутмос М., Банерджи Р. (июль 2013 г.). «Структура и кинетический анализ продукции H2S меркаптопируватсульфотрансферазой человека» . Журнал биологической химии . 288 (27): 20002–13. дои : 10.1074/jbc.M113.466177 . ПМЦ 3707699 . ПМИД 23698001 .
- ^ Перейти обратно: а б «Ген Энтрез: меркаптопируватсертрансфераза MPST» .
- ^ Перейти обратно: а б Паттерсон С.Е., Мёллер Б., Нагасава Х.Т., Винс Р., Крэнкшоу Д.Л., Бриггс Дж., Стутельберг М.В., Виннакота К.В., Лог Б.А. (июнь 2016 г.). «Разработка сульфаногена для борьбы с массовыми жертвами цианидов» . Анналы Нью-Йоркской академии наук . 1374 (1): 202–9. Бибкод : 2016NYASA1374..202P . дои : 10.1111/nyas.13114 . ПМЦ 4940216 . ПМИД 27308865 .
- ^ Паллини Р., Гуацци Г.К., Каннелла С., Какаче М.Г. (октябрь 1991 г.). «Клонирование и анализ последовательности роданезы печени человека: сравнение с бычьими и куриными ферментами» . Связь с биохимическими и биофизическими исследованиями . 180 (2): 887–93. дои : 10.1016/S0006-291X(05)81148-9 . ПМИД 1953758 .
- ^ Перейти обратно: а б Нагахара Н., Окадзаки Т., Нишино Т. (июль 1995 г.). «Цитозольная меркаптопируватсульфераза эволюционно родственна митохондриальной роданезе. Поразительное сходство в аминокислотной последовательности активного центра и увеличение активности меркаптопируватсульфотрансферазы роданезы за счет сайт-направленного мутагенеза» . Журнал биологической химии . 270 (27): 16230–5. дои : 10.1074/jbc.270.27.16230 . ПМИД 7608189 .
- ^ Перейти обратно: а б Сибуя Н., Миками Ю., Кимура Ю., Нагахара Н., Кимура Х. (ноябрь 2009 г.). «Сосудистый эндотелий экспрессирует 3-меркаптопируватсертрансферазу и производит сероводород». Журнал биохимии . 146 (5): 623–6. дои : 10.1093/jb/mvp111 . ПМИД 19605461 .
- ^ Вачек Х., Вуд Дж.Л. (январь 1972 г.). «Очистка и свойства меркаптопируватсеротрансферазы из Escherichia coli». Acta биохимии и биофизики (BBA) - энзимология 258 (1): 133–46. дои : 10.1016/0005-2744(72)90973-4 . ПМИД 4550801 .
- ^ Перейти обратно: а б Куо ММ, Ким Д.Х., Джанду С., Бергман Ю., Тан С., Ван Х., Панди Д.Р., Абрахам Т.П., Шукас А.А., Берковиц Д.Е., Сантанам Л. (январь 2016 г.). «MPST, но не CSE, является основным регулятором продукции и функции сероводорода в коронарной артерии» . Американский журнал физиологии. Физиология сердца и кровообращения . 310 (1): H71–9. дои : 10.1152/ajpheart.00574.2014 . ПМЦ 4796461 . ПМИД 26519030 .
- ^ Бийо-Ладен I, Рат Е, Аллорж Д, Крунель-Тибо А, Кофье С, Шевалье Д, Ло-Гидис ЖМ, Броли Ф (август 2006 г.). «Доказательства функционального генетического полиморфизма меркаптопируватсульфотрансферазы человека (MPST), фермента детоксикации цианидов». Письма по токсикологии . 165 (2): 101–11. дои : 10.1016/j.toxlet.2006.02.002 . ПМИД 16545926 .
- ^ Убука Т., Хосаки Ю., Нишина Х., Икеда Т. (1985). «Активность 3-меркаптопируватсульфотрансферазы в тканях морских свинок и крыс». Физиологическая химия и физико-медицинский ЯМР . 17 (1): 41–3. ПМИД 3862140 .
- ^ Нагахара Н., Ито Т., Китамура Х., Нишино Т. (сентябрь 1998 г.). «Тканевое и субклеточное распределение меркаптопируватсеротрансферазы у крыс: конфокальная лазерная флуоресценция и иммуноэлектронно-микроскопические исследования в сочетании с биохимическим анализом». Гистохимия и клеточная биология . 110 (3): 243–50. дои : 10.1007/s004180050286 . ПМИД 9749958 . S2CID 25430792 .
- ^ Сёрбо Б (1987). «3-меркаптопируват, 3-меркаптолактат и меркаптоацетат». Сера и серные аминокислоты . Методы энзимологии. Том. 143. стр. 178–82. дои : 10.1016/0076-6879(87)43033-4 . ISBN 9780121820435 . ПМИД 3657534 .
- ^ «Бета-меркаптолактат-цистеин-дисульфидурия - О болезни - Информационный центр генетических и редких заболеваний» . Rarediseases.info.nih.gov . Проверено 9 марта 2024 г.
- ^ Гай Дж.В., Цинь В., Лю М., Ван Х.Ф., Чжан М., Ли М., Чжоу В.Х., Ма QT, Лю ГМ, Сун В.Х., Цзинь Дж., Ма Х.С. (апрель 2016 г.). «Профиль экспрессии сероводорода и его синтаз коррелирует со стадией и степенью опухоли уротелиально-клеточного рака мочевого пузыря». Урологическая онкология . 34 (4): 166.e15–20. дои : 10.1016/j.urolonc.2015.06.020 . ПМИД 26847849 .
Дальнейшее чтение (в основном старая литература)
[ редактировать ]- Фидлер Х., Вуд Дж.Л. (сентябрь 1956 г.). «Исследование специфичности системы транссульфурации бета-меркаптопируват-цианид» . Журнал биологической химии . 222 (1): 387–97. дои : 10.1016/S0021-9258(19)50803-1 . ПМИД 13367011 .
- Хилин Дж. В., Вуд Дж. Л. (август 1959 г.). «Ферментативное образование полисульфидов из меркаптопирувата» . Журнал биологической химии . 234 (8): 2141–4. дои : 10.1016/S0021-9258(18)69881-3 . ПМИД 13673028 .
- Сорбо Б (май 1957 г.). «Ферментативный переход серы из меркаптопирувата в сульфат или сульфинаты». Биохимика и биофизика Acta . 24 (2): 324–9. дои : 10.1016/0006-3002(57)90201-9 . ПМИД 13436433 .
- Вачек Х., Вуд Дж.Л. (январь 1972 г.). «Очистка и свойства меркаптопируватсеротрансферазы из Escherichia coli». Acta биохимии и биофизики (BBA) - энзимология 258 (1): 133–46. дои : 10.1016/0005-2744(72)90973-4 . ПМИД 4550801 .
- Ван ден Хамер CJ, Морелл А.Г., Шейнберг И.Х. (май 1967 г.). «Исследование содержания меди в бета-меркаптопируват-транссульфуразе» . Журнал биологической химии . 242 (10): 2514–6. дои : 10.1016/S0021-9258(18)95992-2 . ПМИД 6026243 .