XRCC1
| XRCC1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | XRCC1 , RCC, рентгеновская репарация, дополняющая дефектную репарацию в клетках китайского хомячка 1, перекрестная комплементарная рентгеновская репарация 1, SCAR26 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 194360 ; МГИ : 99137 ; Гомологен : 31368 ; Генные карты : XRCC1 ; OMA : XRCC1 — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Белок репарации ДНК XRCC1 , также известный как белок 1 перекрестной комплементации рентгеновской репарации , представляет собой белок , который у человека кодируется XRCC1 геном . XRCC1 участвует в репарации ДНК , образуя комплекс с ДНК-лигазой III.
Функция
[ редактировать ]| XRCC1_N | |||
|---|---|---|---|
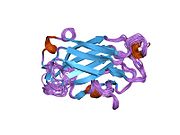
 Структура раствора ЯМР белка репарации одноцепочечного разрыва xrcc1-n-концевой домен | |||
| Идентификаторы | |||
| Символ | XRCC1_N | ||
| Пфам | PF01834 | ||
| Пфам Клан | CL0202 | ||
| ИнтерПро | ИПР002706 | ||
| ОБЛАСТЬ ПРИМЕНЕНИЯ 2 | 1xnt / SCOPe / СУПФАМ | ||
| |||
XRCC1 участвует в эффективном восстановлении одноцепочечных разрывов ДНК, образовавшихся под воздействием ионизирующего излучения и алкилирующих агентов. Этот белок взаимодействует с ДНК-лигазой III, бета-полимеразой и поли(АДФ-рибозо)-полимеразой, участвуя в пути эксцизионной репарации оснований . Он может играть роль в процессинге ДНК во время мейогенеза, т.е. во время индукции мейоза и рекомбинации в зародышевых клетках. Редкий микросателлитный полиморфизм этого гена связан с раком у пациентов с различной радиочувствительностью. [ 5 ]
Белок XRCC1 не обладает ферментативной активностью, но действует как каркасный белок, который взаимодействует с множеством ферментов репарации. Этот каркас позволяет этим ферментам репарации затем выполнять свои ферментативные этапы по восстановлению ДНК. XRCC1 участвует в репарации одноцепочечных разрывов, эксцизионной репарации оснований и эксцизионной репарации нуклеотидов . [ 6 ]
По мнению Лондона, [ 6 ] Белок XRCC1 имеет три глобулярных домена, соединенных двумя линкерными сегментами длиной ~150 и 120 остатков. N-концевой домен XRCC1 связывается с ДНК-полимеразой бета, C-концевой домен BRCT взаимодействует с ДНК- лигазой III альфа, а центральный домен содержит мотив связывания поли(ADP-рибозы) . Этот центральный домен позволяет рекрутировать XRCC1 в полимерную ADP-рибозу, которая образуется на PARP1 после того, как PARP1 связывается с одноцепочечными разрывами. Первый линкер содержит последовательность ядерной локализации, а также имеет область, которая взаимодействует с белком репарации ДНК REV1 , а REV1 рекрутирует трансповреждающие полимеразы. Второй линкер взаимодействует с полинуклеотидкиназной фосфатазой (PNKP) (которая обрабатывает разорванные концы ДНК во время репарации вырезаемых оснований), апратаксином (активен в репарации одноцепочечной ДНК и соединении негомологичных концов) и третьим белком, называемым апратаксин- и PNKP-подобным. фактор.
XRCC1 играет важную роль в микрогомологическом восстановлении двухцепочечных разрывов (MMEJ). MMEJ — это путь репарации ДНК с высокой вероятностью ошибок, который приводит к делеционным мутациям. XRCC1 — один из 6 белков, необходимых для этого пути. [ 7 ]
Чрезмерная экспрессия при раке
[ редактировать ]XRCC1 сверхэкспрессируется при немелкоклеточном раке легкого (НМРЛ). [ 8 ] и на еще более высоком уровне в метастатических лимфатических узлах НМРЛ. [ 9 ]
Недостаточная экспрессия при раке
[ редактировать ]Дефицит XRCC1 из-за гетерозиготности по мутированному гену XRCC1, кодирующему укороченный белок XRCC1, подавляет рост опухоли у мышей. [ 10 ] В трех экспериментальных условиях, вызывающих три типа рака (рак толстой кишки, меланома или рак молочной железы), мыши, гетерозиготные по этой мутации XRCC1, имели существенно меньший объем или количество опухолей, чем мыши дикого типа, подвергавшиеся такому же канцерогенному лечению.
Сравнение с другими генами репарации ДНК при раке
[ редактировать ]Рак очень часто страдает от недостаточной экспрессии одного или нескольких генов репарации ДНК, но сверхэкспрессия гена репарации ДНК при раке встречается реже. Например, по крайней мере 36 белков репарации ДНК, будучи мутационно дефектными в клетках зародышевой линии, вызывают повышенный риск развития рака (наследственные раковые синдромы ). [ нужна ссылка ] (Также см. «Нарушение репарации ДНК» .) Аналогичным образом, по крайней мере 12 генов репарации ДНК часто оказываются эпигенетически репрессированными при одном или нескольких видах рака. [ нужна ссылка ] (См. также Эпигенетическое снижение репарации ДНК и рак .) Обычно недостаточная экспрессия фермента репарации ДНК приводит к увеличению количества невосстановленных повреждений ДНК, которые из-за ошибок репликации ( синтез транслейкоза ) приводят к мутациям и раку. Однако репарация MMEJ , опосредованная XRCC1 , является непосредственно мутагенной, поэтому в этом случае сверхэкспрессия, а не недостаточная экспрессия, по-видимому, приводит к раку. Уменьшение мутагенной репарации MMEJ, опосредованной XRCC1, приводит к замедлению прогрессирования рака.
Старение
[ редактировать ]В старых человеческих стволовых клетках , полученных из жировой ткани , нарушена репарация эксцизионного основания (BER), но не репарация двухцепочечного разрыва ДНК. Белок XRCC1, но не другие факторы BER, продемонстрировал связанное с возрастом снижение. [ 11 ] Сверхэкспрессия XRCC1 обратила вспять возрастное снижение функции BER.
Восстановление после инсульта
[ редактировать ]Окислительный стресс усиливается в головном мозге во время ишемического инсульта, что приводит к увеличению нагрузки на механизмы устойчивости к стрессу, в том числе механизмы восстановления окислительно-поврежденной ДНК . Следовательно, любая потеря системы восстановления, которая обычно восстанавливала бы поврежденную ДНК, может препятствовать выживанию и нормальному функционированию нейронов головного мозга . Гош и др. [ 12 ] сообщили, что частичная потеря функции XRCC1 вызывает увеличение повреждения ДНК в головном мозге и замедление восстановления после ишемического инсульта. Это открытие указывает на то, что XRCC1-опосредованное восстановление основания при иссечении важно для быстрого восстановления после инсульта.
Структура
[ редактировать ]в растворе ЯМР Структура Xrcc1 N-концевого домена (Xrcc1 NTD) показывает, что структурное ядро представляет собой бета-сэндвич с бета-нитями, соединенными петлями, тремя спиралями и двумя короткими двухцепочечными бета-листами на каждой стороне соединения. Xrcc1 NTD специфически связывает ДНК с одноцепочечным разрывом (с разрывом и разрывом) и комплекс ДНК-бета-Pol с разрывом . [ 13 ]
Взаимодействия
[ редактировать ]Было показано, что XRCC1 взаимодействует с:
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с GRCh38: Версия Ensembl 89: ENSG00000073050 – Ensembl , май 2017 г.
- ^ Перейти обратно: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000051768 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ген Энтрез: рентгеновская репарация XRCC1, дополняющая дефектную репарацию в клетках китайского хомячка 1» .
- ^ Перейти обратно: а б Лондон RE (2015). «Структурные основы репарации ДНК, опосредованной XRCC1» . Восстановление ДНК (Амст.) . 30 : 90–103. дои : 10.1016/j.dnarep.2015.02.005 . ПМК 5580684 . ПМИД 25795425 .
- ^ Шарма С., Джавадекар С.М., Панди М., Шривастава М., Кумари Р., Рагхаван С.К. (2015). «Гомология и ферментативные требования к зависимому от микрогомологии альтернативному соединению концов» . Смерть клетки Дис . 6 (3): e1697. дои : 10.1038/cddis.2015.58 . ПМЦ 4385936 . ПМИД 25789972 .
- ^ Кан Ч., Чан Б.Г., Ким Д.В., Чунг Д.Х., Ким Ю.Т., Чжон С., Сунг С.В., Ким Дж.Х. (2010). «Прогностическое значение экспрессии ERCC1, BRCA1, XRCC1 и бетаIII-тубулина у пациентов с немелкоклеточным раком легкого, получавших неоадъювантную химиотерапию на основе платины и таксанов и хирургическую резекцию». Рак легких . 68 (3): 478–83. дои : 10.1016/j.lungcan.2009.07.004 . ПМИД 19683826 .
- ^ Кан Ч., Чан Б.Г., Ким Д.В., Чунг Д.Х., Ким Ю.Т., Чжон С., Сун С.В., Ким Дж.Х. (2009). «Различия в профилях экспрессии группы 1 перекрестной комплементации эксцизионной репарации, группы 1 перекрестной комплементации рентгеновской репарации и бетаIII-тубулина между первичным немелкоклеточным раком легкого и метастатическими лимфатическими узлами, а также значение в среднесрочной выживаемости» . Дж Торак Онкол . 4 (11): 1307–12. дои : 10.1097/JTO.0b013e3181b9f236 . ПМИД 19745766 . S2CID 30337977 .
- ^ Петтан-Брюэр С., Мортон Дж., Каллен С., Эннс Л., Керли К.Р., Сидорова Дж., Го Дж., Койл Р., Ладиж В.К. (2012). «Рост опухоли подавляется у мышей, экспрессирующих укороченный белок XRCC1» . Am J Cancer Res . 2 (2): 168–77. ПМЦ 3304571 . ПМИД 22432057 .
- ^ Чжан Х, Цай Б, Гэн А, Тан Х, Чжан В, Ли С, Цзян Ю, Тан Р, Ван Х, Мао Цзы (февраль 2020 г.). «В старых стволовых клетках человека, полученных из жировой ткани, нарушается эксцизионное восстановление оснований, но не восстановление двухцепочечного разрыва ДНК» . Стареющая клетка . 19 (2): e13062. дои : 10.1111/acel.13062 . ПМК 6996963 . ПМИД 31782607 .
- ^ Гош С., Канугови С., Юн Дж.С., Уилсон Д.М., Крото Д.Л., Мэттсон М.П., Бор В.А. (июль 2015 г.). «Частичная потеря белка, поддерживающего репарацию ДНК, Xrcc1, приводит к усилению повреждения головного мозга и замедлению восстановления после ишемического инсульта у мышей» . Нейробиол. Старение . 36 (7): 2319–2330. doi : 10.1016/j.neurobiolaging.2015.04.004 . ПМЦ 5576895 . ПМИД 25971543 .
- ^ Маринчев А., Маллен М.А., Мациевский М.В., Пан Б., Грик М.Р., Маллен Г.П. (сентябрь 1999 г.). «Структура раствора N-концевого домена белка репарации одноцепочечного разрыва XRCC1». Структурная биология природы . 6 (9): 884–93. дои : 10.1038/12347 . ПМИД 10467102 . S2CID 20325918 .
- ^ Видал А.Е., Бойте С., Хиксон И.Д., Радицелла Дж.П. (ноябрь 2001 г.). «XRCC1 координирует начальную и позднюю стадии восстановления абазического участка ДНК посредством белок-белковых взаимодействий» . Журнал ЭМБО . 20 (22): 6530–9. дои : 10.1093/emboj/20.22.6530 . ПМЦ 125722 . ПМИД 11707423 .
- ^ Дате Х, Игараси С., Сано Ю., Такахаси Т., Такахаши Т., Такано Х., Цудзи С., Нисидзава М., Онодера О (декабрь 2004 г.). «Домен FHA апратаксина взаимодействует с C-концевой областью XRCC1». Связь с биохимическими и биофизическими исследованиями . 325 (4): 1279–85. дои : 10.1016/j.bbrc.2004.10.162 . ПМИД 15555565 .
- ^ Перейти обратно: а б Гювен Н., Бешерель О.Дж., Киджас А.В., Чен П., Хоу О., Рудольф Дж.Х., Гатти Р., Дате Х., Онодера О., Таучер-Шольц Г., Лавин М.Ф. (май 2004 г.). «Апратаксин, новый белок, защищающий от генотоксического стресса» . Молекулярная генетика человека . 13 (10): 1081–9 дои : 10.1093/hmg/ddh122 . ПМИД 15044383 .
- ^ Марсин С., Видаль А.Е., Соссу М., Менисье-де Мурсия Ж., Ле Пейдж Ф., Боите С., де Мурсия Г., Радичелла Ж.П. (ноябрь 2003 г.). «Роль XRCC1 в координации и стимуляции восстановления окислительных повреждений ДНК, инициируемого ДНК-гликозилазой hOGG1» . Журнал биологической химии . 278 (45): 44068–74. дои : 10.1074/jbc.M306160200 . ПМИД 12933815 .
- ^ Шрайбер В., Аме Х.К., Долле П., Шульц И., Ринальди Б., Фраулоб В., Менисье-де Мурсия Ж., де Мурсия Г. (июнь 2002 г.). «Поли(АДФ-рибоза)-полимераза-2 (PARP-2) необходима для эффективной репарации ДНК с вырезанием оснований в сочетании с PARP-1 и XRCC1» (PDF) . Журнал биологической химии . 277 (25): 23028–36. дои : 10.1074/jbc.M202390200 . ПМИД 11948190 .
- ^ Перейти обратно: а б Фан Дж., Оттерлей М., Вонг Х.К., Томкинсон А.Е., Уилсон Д.М. (2004). «XRCC1 локализуется и физически взаимодействует с PCNA» . Исследования нуклеиновых кислот . 32 (7): 2193–201. дои : 10.1093/nar/gkh556 . ПМК 407833 . ПМИД 15107487 .
- ^ Уайтхаус СиДжей, Тейлор Р.М., Тистлетуэйт А., Чжан Х., Карими-Бушери Ф., Ласко Д.Д., Вайнфельд М., Калдекотт К.В. (январь 2001 г.). «XRCC1 стимулирует активность полинуклеотидкиназы человека на поврежденных концах ДНК и ускоряет восстановление одноцепочечных разрывов ДНК» . Клетка . 104 (1): 107–17. дои : 10.1016/S0092-8674(01)00195-7 . ПМИД 11163244 . S2CID 1487128 .
- ^ Юинг Р.М., Чу П., Элизма Ф., Ли Х., Тейлор П., Клими С., МакБрум-Серажевски Л., Робинсон М.Д., О'Коннор Л., Ли М., Тейлор Р., Дарси М., Хо Ю, Хейлбут А., Мур Л., Чжан С., Орнацкий О., Бухман Ю.В., Этьер М., Шэн Ю., Василеску Дж., Абу-Фарха М., Ламберт Дж.П., Дювел. Х.С., Стюарт II, Кюль Б., Хог К., Колвилл К., Гладвиш К., Маскат Б., Кинач Р., Адамс С.Л., Моран М.Ф., Морин ГБ, Топалоглу Т., Фигейс Д. (2007). «Крупномасштабное картирование белково-белковых взаимодействий человека методом масс-спектрометрии» . Молекулярная системная биология . 3 (1): 89. дои : 10.1038/msb4100134 . ПМЦ 1847948 . ПМИД 17353931 .
- ^ Ван Л., Бхаттачарья Н., Челси ДМ, Эскобар П.Ф., Банерджи С. (ноябрь 2004 г.). «Новый ядерный белок MGC5306 взаимодействует с ДНК-полимеразой бета и играет потенциальную роль в клеточном фенотипе». Исследования рака . 64 (21): 7673–7. doi : 10.1158/0008-5472.CAN-04-2801 . ПМИД 15520167 . S2CID 35569215 .
- ^ Кубота Ю., Нэш Р.А., Клунгланд А., Шер П., Барнс Д.Э., Линдал Т. (декабрь 1996 г.). «Восстановление эксцизионной репарации оснований ДНК очищенными белками человека: взаимодействие между ДНК-полимеразой бета и белком XRCC1» . Журнал ЭМБО . 15 (23): 6662–70. дои : 10.1002/j.1460-2075.1996.tb01056.x . ПМК 452490 . ПМИД 8978692 .
- ^ Бхаттачария Н., Банерджи С. (июль 2001 г.). «Новая роль XRCC1 в функциях бета-варианта ДНК-полимеразы». Биохимия . 40 (30): 9005–13. дои : 10.1021/bi0028789 . ПМИД 11467963 .
- ^ Массон М., Нидерганг С., Шрайбер В., Мюллер С., Менисье-де Мурсия Дж., де Мурсия Дж. (июнь 1998 г.). «XRCC1 специфически связан с поли(АДФ-рибозо)-полимеразой и отрицательно регулирует ее активность после повреждения ДНК» . Молекулярная и клеточная биология . 18 (6): 3563–71. дои : 10.1128/MCB.18.6.3563 . ПМК 108937 . ПМИД 9584196 .
Дальнейшее чтение
[ редактировать ]- Хунг Р.Дж., Холл Дж., Бреннан П., Боффетта П. (ноябрь 2005 г.). «Генетические полиморфизмы в базовом пути эксцизионной репарации и риск рака: обзор HuGE» . Американский журнал эпидемиологии . 162 (10): 925–42. дои : 10.1093/aje/kwi318 . ПМИД 16221808 .
- Томпсон Л.Х., Брукман К.В., Джонс Н.Дж., Аллен С.А., Каррано А.В. (декабрь 1990 г.). «Молекулярное клонирование человеческого гена XRCC1, которое исправляет дефектную репарацию разрыва цепи ДНК и обмен сестринских хроматид» . Молекулярная и клеточная биология . 10 (12): 6160–71. дои : 10.1128/mcb.10.12.6160 . ПМЦ 362891 . ПМИД 2247054 .
- Томпсон Л.Х., Бачински Л.Л., Столлингс Р.Л., Дольф Г., Вебер К.А., Вестервельд А., Сицилиано М.Дж. (ноябрь 1989 г.). «Комплементация мутаций гена репарации на гемизиготной хромосоме 9 в CHO: третий ген репарации на хромосоме 19 человека» . Геномика . 5 (4): 670–9. дои : 10.1016/0888-7543(89)90107-9 . ПМИД 2591959 .
- Гьяпай Дж., Мориссетт Дж., Виньяль А., Диб С., Физамес С., Миллассо П., Марк С., Бернарди Дж., Латроп М., Вайссенбах Дж. (июнь 1994 г.). «Карта генетических связей человека Généthon 1993–94 годов». Природная генетика . 7 (2 спецификации): 246–339. дои : 10.1038/ng0694supp-246 . ПМИД 7545953 . S2CID 24662426 .
- Вэй Ц, Сюй Икс, Ченг Л., Легерски Р.Дж., Али-Осман Ф. (ноябрь 1995 г.). «Одновременная амплификация четырех генов репарации ДНК и бета-актина в лимфоцитах человека с помощью мультиплексной ПЦР с обратной транскриптазой». Исследования рака . 55 (21): 5025–9. ПМИД 7585546 .
- Ламердин Дж.Э., Монтгомери М.А., Стилваген С.А., Шайдекер Л.К., Теббс Р.С., Брукман К.В., Томпсон Л.Х., Каррано А.В. (январь 1995 г.). «Сравнение геномных последовательностей областей гена репарации ДНК XRCC1 человека и мыши». Геномика . 25 (2): 547–54. дои : 10.1016/0888-7543(95)80056-R . ПМИД 7789989 .
- Калдекотт К.В., МакКаун С.К., Такер Дж.Д., Юнгквист С., Томпсон Л.Х. (январь 1994 г.). «Взаимодействие между белком репарации ДНК млекопитающих XRCC1 и ДНК-лигазой III» . Молекулярная и клеточная биология . 14 (1): 68–76. дои : 10.1128/MCB.14.1.68 . ПМЦ 358357 . ПМИД 8264637 .
- Траск Б., Фертитта А., Кристенсен М., Янгблом Дж., Бергманн А., Коупленд А., де Йонг П., Моренвейзер Х., Олсен А., Каррано А. (январь 1993 г.). «Картирование флуоресцентной гибридизации in situ хромосомы 19 человека: расположение цитогенетических полос 540 космид и 70 генов или маркеров ДНК» . Геномика . 15 (1): 133–45. дои : 10.1006/geno.1993.1021 . ПМИД 8432525 .
- Кубота Ю., Нэш Р.А., Клунгланд А., Шер П., Барнс Д.Э., Линдал Т. (декабрь 1996 г.). «Восстановление эксцизионной репарации оснований ДНК очищенными белками человека: взаимодействие между ДНК-полимеразой бета и белком XRCC1» . Журнал ЭМБО . 15 (23): 6662–70. дои : 10.1002/j.1460-2075.1996.tb01056.x . ПМК 452490 . ПМИД 8978692 .
- Нэш Р.А., Калдекотт К.В., Барнс Д.Е., Линдал Т. (апрель 1997 г.). «Белок XRCC1 взаимодействует с одной из двух различных форм ДНК-лигазы III». Биохимия . 36 (17): 5207–11. дои : 10.1021/bi962281m . ПМИД 9136882 .
- Шен М.Р., Джонс И.М., Моренвейзер Х. (февраль 1998 г.). «Варианты неконсервативных аминокислотных замен существуют с полиморфной частотой в генах репарации ДНК у здоровых людей». Исследования рака . 58 (4): 604–8. ПМИД 9485007 .
- Прайс Э.А., Борн С.Л., Рэдборн Р., Лоутон П.А., Ламердин Дж., Томпсон Л.Х., Арранд Дж.Э. (июль 1997 г.). «Редкие микросателлитные полиморфизмы генов репарации ДНК XRCC1, XRCC3 и XRCC5, связанные с раком у пациентов с различной радиочувствительностью». Соматическая клетка и молекулярная генетика . 23 (4): 237–47. дои : 10.1007/BF02674415 . ПМИД 9542526 . S2CID 32956047 .
- Массон М., Нидерганг С., Шрайбер В., Мюллер С., Менисье-де Мурсия Дж., де Мурсия Дж. (июнь 1998 г.). «XRCC1 специфически связан с поли(АДФ-рибозо)-полимеразой и отрицательно регулирует ее активность после повреждения ДНК» . Молекулярная и клеточная биология . 18 (6): 3563–71. дои : 10.1128/MCB.18.6.3563 . ПМК 108937 . ПМИД 9584196 .
- Тейлор Р.М., Уикстед Б., Кронин С., Калдекотт К.В. (июль 1998 г.). «Роль домена BRCT во взаимодействии ДНК-лигазы III-альфа с белком репарации ДНК XRCC1» . Современная биология . 8 (15): 877–80. дои : 10.1016/S0960-9822(07)00350-8 . ПМИД 9705932 . S2CID 17117423 .
- Чжоу ZQ, Уолтер Калифорния (январь 1998 г.). «Клонирование и характеристика промотора павиана XRCC1, гена, участвующего в восстановлении разрыва цепи ДНК». Соматическая клетка и молекулярная генетика . 24 (1): 23–39. дои : 10.1007/BF02677493 . ПМИД 9776979 . S2CID 21863472 .
- Тейлор Р.М., Мур DJ, Уайтхаус Дж., Джонсон П., Калдекотт К.В. (январь 2000 г.). «Специфическая для клеточного цикла потребность в домене XRCC1 BRCT II во время восстановления разрыва цепи ДНК млекопитающих» . Молекулярная и клеточная биология . 20 (2): 735–40. дои : 10.1128/MCB.20.2.735-740.2000 . ПМЦ 85188 . ПМИД 10611252 .
- Маринчев А., Робертсон А., Димитриадис Е.К., Прасад Р., Уилсон Ш., Маллен Г.П. (май 2000 г.). «Доменоспецифическое взаимодействие в бета-комплексе XRCC1-ДНК-полимеразы» . Исследования нуклеиновых кислот . 28 (10): 2049–59. дои : 10.1093/нар/28.10.2049 . ПМЦ 105377 . ПМИД 10773072 .
- Дуэлл Э.Дж., Винке Дж.К., Ченг Т.Дж., Варкони А., Цзо З.Ф., Ашок Т.Д., Марк Э.Дж., Уэйн Дж.К., Кристиани Д.С., Келси К.Т. (май 2000 г.). «Полиморфизмы генов репарации ДНК XRCC1 и ERCC2 и биомаркеры повреждения ДНК в мононуклеарных клетках крови человека» (PDF) . Канцерогенез . 21 (5): 965–71. дои : 10.1093/carcin/21.5.965 . ПМИД 10783319 .
- Уайтхаус СиДжей, Тейлор Р.М., Тистлетуэйт А., Чжан Х., Карими-Бушери Ф., Ласко Д.Д., Вайнфельд М., Калдекотт К.В. (январь 2001 г.). «XRCC1 стимулирует активность полинуклеотидкиназы человека на поврежденных концах ДНК и ускоряет восстановление одноцепочечных разрывов ДНК» . Клетка . 104 (1): 107–17. дои : 10.1016/S0092-8674(01)00195-7 . ПМИД 11163244 . S2CID 1487128 .
- Дулик А., Бейтс П.А., Чжан Х, Мартин С.Р., Фримонт П.С., Линдал Т., Барнс Д.Е. (май 2001 г.). «Взаимодействие домена BRCT в гетеродимерном белке репарации ДНК XRCC1-ДНК-лигазе III». Биохимия . 40 (20): 5906–13. дои : 10.1021/bi002701e . ПМИД 11352725 .
Внешние ссылки
[ редактировать ]- Рентген + восстановление + перекрест + дополнение + белок + 1 в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Обзор всей структурной информации, доступной в PDB для UniProt : P18887 (белок репарации ДНК XRCC1) в PDBe-KB .