Релятивистская квантовая химия
Релятивистская квантовая химия сочетает в себе релятивистскую механику с квантовой химией для расчета свойств и структуры элементов , особенно для более тяжелых элементов таблицы Менделеева . Ярким примером является объяснение цвета золота : из-за релятивистских эффектов оно не серебристое, как большинство других металлов. [1]
Термин «релятивистские эффекты» был разработан в свете истории квантовой механики. Первоначально квантовая механика разрабатывалась без учета теории относительности . [2] Релятивистские эффекты — это расхождения между значениями, рассчитанными моделями, учитывающими относительность, и теми, которые не учитывают ее. [3] Релятивистские эффекты важны для более тяжелых элементов с высокими атомными номерами , таких как лантаноиды и актиниды . [4]
Релятивистские эффекты в химии можно рассматривать как возмущения или небольшие поправки к нерелятивистской теории химии, которая развивается на основе решений уравнения Шрёдингера . Эти поправки по-разному влияют на электроны в зависимости от скорости электрона по сравнению со скоростью света . Релятивистские эффекты более заметны в тяжелых элементах, потому что только в этих элементах электроны достигают достаточных скоростей, чтобы элементы имели свойства, отличные от того, что предсказывает нерелятивистская химия. [5]
История
[ редактировать ]Начиная с 1935 года Берта Свирлз описала релятивистскую трактовку многоэлектронной системы. [6] несмотря на утверждение Поля Дирака 1929 года о том, что единственные несовершенства, оставшиеся в квантовой механике, «возникают трудности только тогда, когда речь идет о высокоскоростных частицах, и поэтому не имеют значения при рассмотрении атомной и молекулярной структуры и обычных химических реакций, в которых она действительно, обычно достаточно точен, если пренебречь изменением относительности массы и скорости и предположить только кулоновские силы между различными электронами и атомными ядрами». [7]
Химики-теоретики в целом соглашались с мнением Дирака до 1970-х годов, когда в тяжелых элементах наблюдались релятивистские эффекты. [8] Уравнение Шредингера было разработано без учета теории относительности в статье Шредингера 1926 года. [9] Релятивистские поправки были внесены в уравнение Шредингера (см. уравнение Клейна-Гордона ) для описания тонкой структуры атомных спектров, но это и другие разработки не сразу проникли в химическое сообщество. Поскольку атомные спектральные линии в основном относились к области физики, а не химии, большинство химиков были незнакомы с релятивистской квантовой механикой, и их внимание было сосредоточено на более легких элементах, типичных для органической химии того времени. [10]
Мнение Дирака о роли релятивистской квантовой механики в химических системах неверно по двум причинам. Во-первых, электроны на s- и p- атомных орбиталях движутся со скоростью, существенно превышающей скорость света. Во-вторых, релятивистские эффекты приводят к косвенным следствиям, особенно очевидным для d- и f -орбиталей атомов. [8]
Качественное лечение
[ редактировать ]Этот раздел нуждается в дополнительных цитатах для проверки . ( август 2018 г. ) |
Эту статью необходимо обновить . ( декабрь 2020 г. ) |

наиболее важных и известных результатов теории относительности состоит в том, что релятивистская масса электрона Один из увеличивается по мере того, как
где — масса покоя электрона , скорость электрона и скорость света соответственно. Рисунок справа иллюстрирует этот релятивистский эффект как функцию скорости.
Это имеет непосредственное влияние на радиус Бора ( ), что определяется выражением
где — приведенная постоянная Планка , а α — постоянная тонкой структуры (релятивистская поправка к модели Бора ).
Бор подсчитал, что 1s-орбитальный электрон атома водорода, вращающийся по орбите с радиусом Бора 0,0529 нм, движется со скоростью почти 1/137 скорости света. [11] Это можно распространить на более крупный элемент с атомным номером Z, используя выражение для 1s-электрона, где v — его радиальная скорость , т. е. его мгновенная скорость, касательная к радиусу атома. Для золота с Z = 79 v ≈ 0,58 c , поэтому 1s-электрон будет двигаться со скоростью 58% скорости света. Подставив это значение вместо v / c в уравнение для релятивистской массы, можно найти, что m rel = 1,22 m e , и, в свою очередь, подставив это значение для приведенного выше радиуса Бора, можно обнаружить, что радиус уменьшается на 22%.
Если подставить «релятивистскую массу» в уравнение радиуса Бора, можно записать

Отсюда следует, что
Справа приведенное выше соотношение релятивистского и нерелятивистского радиусов Бора изображено в зависимости от скорости электрона. Обратите внимание, как релятивистская модель показывает, что радиус уменьшается с увеличением скорости.
Когда трактовка Бора распространяется на водородные атомы , радиус Бора становится где — главное квантовое число , а Z — целое число атомного номера . В модели Бора угловой момент задается как . Подставляя в приведенное выше уравнение и решая дает
С этого момента атомарные единицы можно использовать для упрощения выражения до
Подстановка этого значения в упомянутое выше выражение для отношения Бора дает
На этом этапе видно, что низкое значение и высокая ценность приводит к . Это соответствует интуиции: электроны с меньшими главными квантовыми числами будут иметь более высокую плотность вероятности оказаться ближе к ядру. Ядро с большим зарядом приведет к тому, что электрон будет иметь большую скорость. Более высокая скорость электронов означает увеличение релятивистской массы электронов, и в результате электроны будут большую часть времени находиться вблизи ядра и тем самым сжимать радиус для малых главных квантовых чисел. [12]
Отклонения таблицы Менделеева
[ редактировать ]Меркурий
[ редактировать ]Ртуть (Hg) представляет собой жидкость при температуре примерно до −39 °C (точка плавления ) . Силы связи для связей Hg–Hg слабее, чем для их непосредственных соседей, таких как кадмий (т.пл. 321 °С) и золото (т.пл. 1064 °С). Сокращение лантаноидов лишь частично объясняет эту аномалию. [11] Потому что 6s 2 орбиталь сжимается из-за релятивистских эффектов и поэтому может лишь незначительно способствовать какой-либо химической связи, связь Hg-Hg должна быть в основном результатом сил Ван-дер-Ваальса . [11] [13] [14]
Газ ртути в основном одноатомный, Hg(g). Hg 2 (g) образуется редко и имеет низкую энергию диссоциации, как и ожидалось, из-за отсутствия прочных связей. [15]
Au 2 (g) и Hg(g) аналогичны H 2 (g) и He(g) в отношении того же характера различий. Релятивистское сжатие шестерок 2 орбиталь приводит к образованию газообразной ртути, которую иногда называют псевдоблагородным газом . [11]
Цвет золота и цезия
[ редактировать ]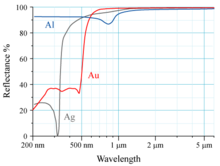

Отражательная способность алюминия ( Al ), серебра (Ag) и золота (Au) показана на графике справа. Человеческий глаз воспринимает электромагнитное излучение с длиной волны около 600 нм как желтое. Золото поглощает синий свет больше, чем другие видимые длины волн света; Таким образом, отраженный свет, достигающий глаза, не имеет синего цвета по сравнению с падающим светом. Поскольку желтый дополняет синий, кусок золота в белом свете кажется человеческому глазу желтым.
За это поглощение отвечает электронный переход с 5d-орбитали на 6s-орбиталь. Аналогичный переход происходит в серебре, но релятивистские эффекты меньше, чем в золоте. В то время как 4d-орбиталь серебра испытывает некоторое релятивистское расширение и сжатие 5s-орбитали, расстояние 4d–5s в серебре намного больше, чем расстояние 5d–6s в золоте. Релятивистские эффекты увеличивают расстояние 5d-орбитали от ядра атома и уменьшают расстояние 6s-орбитали. Из-за уменьшения орбитального расстояния 6s электронный переход в основном поглощает в фиолетово-синей области видимого спектра, а не в УФ-области. [16]
Цезий , самый тяжелый из щелочных металлов , который можно собрать в количествах, достаточных для наблюдения, имеет золотистый оттенок, тогда как остальные щелочные металлы серебристо-белые. Однако релятивистские эффекты не очень существенны при Z = 55 для цезия (недалеко от Z = 47 для серебра). Золотой цвет цезия обусловлен уменьшением частоты света, необходимого для возбуждения электронов щелочных металлов по мере нисхождения группы. Для лития через рубидий эта частота находится в ультрафиолете, а для цезия она достигает сине-фиолетового конца видимого спектра; другими словами, плазмонная частота щелочных металлов становится ниже от лития к цезию. Таким образом, цезий преимущественно пропускает и частично поглощает фиолетовый свет, в то время как другие цвета (имеющие более низкую частоту) отражаются; поэтому он кажется желтоватым. [17]
Свинцово-кислотный аккумулятор
[ редактировать ]Без теории относительности можно было бы ожидать, что свинец ( Z = 82) будет вести себя так же, как олово ( Z = 50), поэтому оловянно-кислотные батареи должны работать так же хорошо, как и свинцово-кислотные батареи, обычно используемые в автомобилях. Однако расчеты показывают, что около 10 В из 12 В, вырабатываемых 6-элементной свинцово-кислотной батареей, возникает исключительно из-за релятивистских эффектов, что объясняет, почему оловянно-кислотные батареи не работают. [18]
Эффект инертной пары
[ редактировать ]Tl(I) ( таллий ), Pb(II) ( свинец ) и Bi(III) ( висмут ) В комплексах 6s 2 электронная пара существует. Эффект инертной пары — это тенденция этой пары электронов сопротивляться окислению из-за релятивистского сжатия 6s-орбитали. [8]
Другие эффекты
[ редактировать ]Дополнительные явления, обычно вызываемые релятивистскими эффектами, следующие:
- Влияние релятивистских эффектов на металлофильные взаимодействия неясно. Хотя Рунеберг и др. (1999) рассчитали эффект притяжения, [19] Ван и др. (2021) вместо этого рассчитали отталкивающий эффект. [20]
- Стабильность анионов золота и платины в таких соединениях, как аурид цезия . [21]
- Несколько сниженная реакционная способность франция по сравнению с цезием. [22] [23]
- Около 10% сокращения лантаноидов объясняется релятивистской массой высокоскоростных электронов и, как следствие, меньшим радиусом Бора . [24]
См. также
[ редактировать ]- Энергия ионизации
- Электроотрицательность
- Сродство к электрону
- Квантовая механика
- Релятивистская квантовая механика
Ссылки
[ редактировать ]- ^ Пекка Пюиккё (январь 2012 г.). «Релятивистские эффекты в химии: более распространены, чем вы думали». Ежегодный обзор физической химии . 63 (1): 45–64. Бибкод : 2012ARPC...63...45P . doi : 10.1146/annurev-physchem-032511-143755 . ПМИД 22404585 .
- ^ Клеппнер, Дэниел (1999). «Краткая история атомной физики ХХ века» (PDF) . Обзоры современной физики . 71 (2): С78–С84. Бибкод : 1999RvMPS..71...78K . дои : 10.1103/RevModPhys.71.S78 . Архивировано из оригинала (PDF) 3 марта 2016 г. Проверено 17 июля 2012 г.
- ^ Калдор, У.; Уилсон, Стивен (2003). Теоретическая химия и физика тяжелых и сверхтяжелых элементов . Дордрехт, Нидерланды: Kluwer Academic Publishers. п. 4. ISBN 978-1-4020-1371-3 .
- ^ Калдор, У.; Уилсон, Стивен (2003). Теоретическая химия и физика тяжелых и сверхтяжелых элементов . Дордрехт, Нидерланды: Kluwer Academic Publishers. п. 2. ISBN 978-1-4020-1371-3 .
- ^ Гупта, вице-президент (22 октября 2015 г.). Принципы и приложения квантовой химии . Эльзевир Наука. ISBN 978-0-12-803478-1 . Проверено 7 января 2024 г.
- ^ Свирлз, Б. (1935). «Релятивистское самосогласованное поле» . Труды Королевского общества A: Математические, физические и технические науки . 152 (877): 625–649. Бибкод : 1935RSPSA.152..625S . дои : 10.1098/rspa.1935.0211 .
- ^ Дирак, ПАМ (1929). «Квантовая механика многоэлектронных систем» . Труды Королевского общества A: Математические, физические и технические науки . 123 (792): 714–733. Бибкод : 1929RSPSA.123..714D . дои : 10.1098/rspa.1929.0094 . JSTOR 95222 .
- ^ Jump up to: а б с Пюиккё, Пекка (1988). «Релятивистские эффекты в структурной химии». Химические обзоры . 88 (3): 563–594. дои : 10.1021/cr00085a006 .
- ^ Эрвин Шрёдингер (1926). «О связи квантовой механики Гейзенберга-Борна-Джордана с моей» (PDF) . Анналы физики (на немецком языке). 384 (8). Лейпциг: 734–756. Нагрудный код : 1926АнП...384..734С . дои : 10.1002/andp.19263840804 . Архивировано из оригинала (PDF) 17 декабря 2008 г.
- ^ Калдор, У.; Уилсон, Стивен, ред. (2003). Теоретическая химия и физика тяжелых и сверхтяжелых элементов . Дордрехт, Нидерланды: Kluwer Academic Publishers. п. 17. ISBN 978-1-4020-1371-3 .
- ^ Jump up to: а б с д Норрби, Ларс Дж. (1991). «Почему ртуть жидкая? Или почему релятивистские эффекты не попадают в учебники химии?». Журнал химического образования . 68 (2): 110. Бибкод : 1991ЖЧЭд..68..110Н . дои : 10.1021/ed068p110 .
- ^ Питцер, Кеннет С. (1979). «Релятивистское влияние на химические свойства» (PDF) . Отчеты о химических исследованиях . 12 (8): 271–276. дои : 10.1021/ar50140a001 . S2CID 95601322 .
- ^ Кальво, Флоран; Паль, Эльке; Червь, Майкл; Швердтфегер, Питер (2013). «Доказательства низкотемпературного плавления ртути благодаря теории относительности» . Angewandte Chemie, международное издание . 52 (29): 7583–7585. дои : 10.1002/anie.201302742 . ISSN 1521-3773 . ПМИД 23780699 .
- ^ Хоус2013-06-21T00:00:00+01:00, Лора. «Относительность ликвидности ртути» . Химический мир . Проверено 21 января 2022 г.
{{cite web}}: CS1 maint: числовые имена: список авторов ( ссылка ) - ^ Зенакер, А. (1 июня 1987 г.). «Экспериментальное исследование холодного димера ртути» . Журнал химической физики . 86 : 6565–6566.
- ^ Пюиккё, Пекка; Декло, Жан Поль (1979). «Относительность и периодическая система элементов». Отчеты о химических исследованиях . 12 (8): 276. дои : 10.1021/ar50140a002 .
- ^ Аддисон, CC (1984). Химия жидких щелочных металлов . Уайли. п. 7. ISBN 9780471905080 .
- ^ Ахуджа, Раджив; Бломквист, Андерс; Ларссон, Питер; Пюиккё, Пекка; Залески-Эйгерд, Патрик (2011). «Относительность и свинцово-кислотная батарея». Письма о физических отзывах . 106 (1): 018301. arXiv : 1008.4872 . Бибкод : 2011PhRvL.106a8301A . doi : 10.1103/PhysRevLett.106.018301 . ПМИД 21231773 . S2CID 39265906 .
- ^ Рунеберг, Нино; Шютц, Мартин; Вернер, Ханс-Иоахим (1999). «Аурофильное влечение в интерпретации методов локальной корреляции». Дж. Хим. Физ. 110 (15): 7210–7215. Бибкод : 1999JChPh.110.7210R . дои : 10.1063/1.478665 .
- ^ Ван, Цинъюнь; Ян, Цзюнь; То, Вай-Понг; Че, Чи-Мин (5 января 2021 г.). «Сильное отталкивание Паули между металлами приводит к отталкивающей металлофильности в металлоорганических комплексах d 8 и d 10 с закрытой оболочкой» . Труды Национальной академии наук . 118 (1): e2019265118. Бибкод : 2021PNAS..11819265W . дои : 10.1073/pnas.2019265118 . ISSN 0027-8424 . ПМЦ 7817198 . ПМИД 33372160 .
- ^ Янсен, Мартин (декабрь 2005 г.). «Влияние релятивистского движения электронов на химию золота и платины» . Науки о твердом теле . 7 (12): 1464–1474. Бибкод : 2005SSSci...7.1464J . doi : 10.1016/j.solidstatesciences.2005.06.015 .
- ^ «Элементы IYPT 2019 087: Франций: не самый реактивный элемент группы 1» . Исследования бытовых химических соединений . 6 ноября 2019 г.
- ^ Андреев С.В.; Летохов В.С.; Мишин В.И. (21 сентября 1987 г.). «Лазерная резонансная фотоионизационная спектроскопия ридберговских уровней во Fr». Письма о физических отзывах . 59 (12): 1274–1276. Бибкод : 1987PhRvL..59.1274A . дои : 10.1103/PhysRevLett.59.1274 . ПМИД 10035190 .
- ^ Пюикко, Пекка (1 мая 1988 г.). «Релятивистские эффекты в структурной химии». Химические обзоры . 88 (3): 563–594. дои : 10.1021/cr00085a006 .
Дальнейшее чтение
[ редактировать ]- П.А. Кристиансен; В. К. Эрмлер; КС Питцер. Релятивистские эффекты в химических системах. Ежегодный обзор физической химии 1985 , 36 , 407–432. дои : 10.1146/annurev.pc.36.100185.002203



















