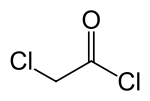
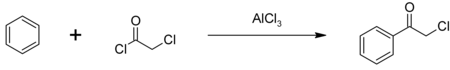Хлороацетилхлорид
| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Хлороацетилхлорид | |
| Другие имена
2-хлорацетилхлорид
Хлорид хлоруксусной кислоты Хлороуксусный хлорид Монохлорацетилхлорид | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.001.065 |
| Номер ЕС |
|
| КЕГГ | |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1752 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 2 Н 2 Cl 2 О | |
| Молярная масса | 112.94 g·mol −1 |
| Появление | Бесцветная или желтая жидкость |
| Плотность | 1,42 г/мл |
| Температура плавления | -22 ° C (-8 ° F; 251 К) |
| Точка кипения | 106 ° С (223 ° F; 379 К) |
| Реагирует | |
| Давление пара | 19 мм рт.ст. (20°С) [ 1 ] |
| Опасности | |
| СГС Маркировка : | |
   
| |
| Опасность | |
| Х301 , Х311 , Х314 , Х331 , Х372 , Х400 | |
| P260 , P261 , P264 , P270 , P271 , P273 , P280 , P301+P310 , P301+P330+P331 , P302+P352 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P311 , P312 , P314 , P321 , P322 , P330 , P361 , P363 , P391 , P403+P233 , P405 , P501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | негорючий [ 1 ] |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо)
|
никто [ 1 ] |
РЕЛ (рекомендуется)
|
TWA 0,05 частей на миллион (0,2 мг/м 3 ) [ 1 ] |
IDLH (Непосредственная опасность)
|
без даты [ 1 ] |
| Паспорт безопасности (SDS) | Оксфордский паспорт безопасности материалов |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Хлороацетилхлорид представляет собой хлорированный ацилхлорид . Это бифункциональное соединение , что делает его полезным химическим строительным материалом.
Производство
[ редактировать ]его получают карбонилированием метиленхлорида , В окислением винилиденхлорида или . добавлением хлора к кетену промышленности [ 3 ] Его можно получить из хлоруксусной кислоты и тионилхлорида , пентахлорида фосфора или фосгена .
Реакции
[ редактировать ]Хлороацетилхлорид бифункционален: ацилхлорид легко образует сложные эфиры. [ 4 ] и амиды , тогда как другой конец молекулы способен образовывать другие связи, например, с аминами. использование хлорацетилхлорида в синтезе лидокаина : Показательно [ 5 ]
Приложения
[ редактировать ]В основном хлорацетилхлорид используется в качестве промежуточного продукта при производстве гербицидов семейства хлорацетанилидов, включая метолахлор , ацетохлор , алахлор и бутахлор ; ежегодно используется около 100 миллионов фунтов. Некоторое количество хлорацетилхлорида также используется для производства фенацилхлорида , другого химического промежуточного продукта, также используемого в качестве слезоточивого газа. [ 3 ] Фенацилхлорид синтезируется методом Фриделю-Крафтсу ацилирования бензола по с использованием катализатора из хлорида алюминия : [ 6 ]
Вместе с анизолом используется для синтеза венлафаксина .
Безопасность
[ редактировать ]Как и другие ацилхлориды, реакция с другими протонными соединениями, такими как амины, спирты и вода, приводит к образованию соляной кислоты , что делает ее слезоточивым средством .
не существует Нормированных допустимых пределов воздействия, установленных Управлением по охране труда, . Однако Национальный институт охраны труда установил рекомендуемый предел воздействия на уровне 0,05 частей на миллион в течение восьмичасового рабочего дня. [ 7 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и Карманный справочник NIOSH по химическим опасностям. «#0120» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ «База данных по профессиональным химикатам OSHA» . Управление по охране труда (OSHA).
- ^ Jump up to: а б Пол Р. Уоршам (1993). «15. Галогенированные производные» ( отрывок из Google Books ) . В Зеллере, Джозеф Р.; Агреда, В.Х. (ред.). Уксусная кислота и ее производные . Нью-Йорк: М. Деккер. стр. 288–298. ISBN 0-8247-8792-7 .
- ^ Роберт Х. Бейкер и Фредерик Г. Бордвелл (1955). «трет-Бутилацетат» . Органические синтезы ; Сборник томов , т. 3 .
- ^ Ти Джей Рейли (1999). «Приготовление лидокаина» . Дж. Хим. Образование. 76 (11): 1557. Бибкод : 1999JChEd..76.1557R . дои : 10.1021/ed076p1557 .
- ^ Натан Левин и Уолтер Х. Хартунг (1955). «ω-хлоризонитрозоацетофенон» . Органические синтезы ; Сборник томов , т. 3, с. 191 .
- ^ «Карманный справочник NIOSH по химическим опасностям» . Центры по контролю и профилактике заболеваний. 2011.