Железосвязывающие белки
Железосвязывающие белки — это белки-переносчики и металлопротеины , которые играют важную роль в метаболизме железа. [1] и иммунный ответ. [2] [3] Железо необходимо для жизни.
Железозависимые ферменты катализируют множество биохимических реакций и могут быть разделены на три широких класса в зависимости от структуры их активного центра: негемовое моножелезо, негемовое дижелезо или гем-центры. [4] Хорошо известное семейство железозависимых ферментов включает оксигеназы, которые облегчают присоединение гидроксильной группы к одному или обоим атомам о 2 . Известные ферменты включают триптофандиоксигеназу, ферредоксин и 2-оксоглутаратдиоксигеназу. [5]
Гемовые белки
[ редактировать ]
Гем-белки — это белки, содержащие простетическую группу гема. Гемовая группа состоит из порфиринового кольца, координированного ионом железа. Четыре атома азота в порфириновом кольце действуют как лиганд для железа в центре. Во многих случаях экваториальный порфирин дополняется одним или двумя аксиальными лигандами. Примером этого является гемоглобин, где порфирин работает вместе с боковой цепью гистидина и связанной молекулой О 2 , образуя октаэдрический комплекс.
Гемоглобин
[ редактировать ]
Гемоглобин – белок-переносчик кислорода, обнаруженный практически у всех позвоночных. Гемоглобин А — основной тип, встречающийся у взрослых людей. Это тетрамер, состоящий из двух альфа- и двух бета-субъединиц. Каждая из четырех мономерных единиц содержит простетическую группу гема, в которой катион трехвалентного железа связан между четырьмя атомами азота порфиринового кольца. Наряду с гистидином апо-форма имеет пять лигандов, окружающих атом железа. Кислород связывается с пустой шестой позицией, образуя октаэдрический комплекс в голо-форме. [6] Связывание кислорода полностью кооперативно для каждой из субъединиц, поскольку, когда первый кислород связывается с одной из четырех групп гема, белок претерпевает резкое конформационное изменение, которое резко увеличивает сродство к кислороду трех других субъединиц. [7]
Гемоглобин имеет различное сродство в зависимости от pH, структуры и CO 2 парциального давления . Фетальный гемоглобин представляет собой вариант, содержащий две гамма-субъединицы вместо двух бета-субъединиц. Фетальный гемоглобин является преобладающей формой до тех пор, пока ребенку не исполнится несколько месяцев, и он имеет большее сродство к кислороду, чтобы компенсировать низкое напряжение кислорода в подаваемой материнской крови во время беременности. [8] Гемоглобин имеет более низкое сродство к кислороду при низком pH. Это обеспечивает быструю диссоциацию, поскольку насыщенный кислородом гемоглобин транспортируется к клеткам по всему организму. В результате продукции CO 2 и образования водной угольной кислоты в дышащих клетках насыщенный кислородом гемоглобин диссоциирует, чтобы доставить к клеткам необходимый кислород. [9] Гемоглобин имеет сродство к связыванию монооксида углерода в 250 раз больше, чем к кислороду. Это основа отравления угарным газом , поскольку гемоглобин больше не может переносить кислород к клеткам.
Цитохромы
[ редактировать ]Цитохромы представляют собой гемсодержащие ферменты, которые действуют как переносчики одноэлектронов, в первую очередь как переносчики электронов при окислительном фосфорилировании и фотосинтезе. Типы хорошо изученных цитохромов включают цитохромы ac, цитохромоксидазу и цитохром P450. [10] Эти белки действуют как переносчики электронов, переключая степень окисления атома железа гема между двухвалентным (Fe 2+ ) и железо (Fe 3+ ). Различные цитохромы в сочетании с другими редокс-активными молекулами образуют градиент стандартных восстановительных потенциалов, который повышает эффективность энергетического взаимодействия во время событий переноса электрона.
Железо-серные белки
[ редактировать ]Железо-серные белки — это белки, структура железа которых включает серу. Существует множество форм, в которых железо и сера могут приниматься в белках, но наиболее распространенными являются [2Fe 2S] и [4Fe 4S]. Кластеры часто связаны с остатками цистеина в белковой цепи. [11]
Негемовые белки
[ редактировать ]Трансферрин
[ редактировать ]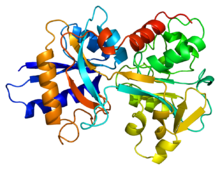
Трансферрин содержится в плазме человека и используется для транспортировки и импорта негемового железа. [12] Он свободно перемещается во внеклеточном пространстве. [13] Когда железо необходимо клетке, оно переносится в цитозоль с помощью рецептора трансферрина . Трансферрин может связывать два иона Fe(III) вместе с анионом (обычно карбонатом). Для высвобождения железа карбонат-анион протонируется. Это изменяет взаимодействие карбоната с белком, изменяя конформацию и позволяя переносить Fe (III).
Трансферрин имеет молекулярную массу около 80 кДа. Это гликопротеин, что означает, что к его аминокислотной цепи прикреплены сахара.
Лактоферрин
[ редактировать ]Лактоферрин является членом семейства трансферринов и является преобладающим белком, обнаруженным в экзокринных секретах млекопитающих, таких как слезы, молоко и слюна. Он состоит примерно из 700 остатков и существует в основном в виде тетрамера с соотношением мономер:тетрамер 1:4 при концентрации белка 10 мкМ. [14] Третичная структура состоит из двух долей, называемых долями N и C, каждая из которых содержит один карман для связывания железа. Каждый карман содержит четыре аминокислоты (два тирозина, один гистидин и один аспартат) и вместе с двумя карбонатными или бикарбонатными анионами образует шестичленную координату вокруг катиона железа. Именно эта специфическая комбинация делает сродство лактоферрина к железу в 300 раз выше, чем у трансферрина. [15]

Лактоферрин обладает значительными антимикробными свойствами. Самая высокая концентрация — 150 нг/мл — содержится в молозиве человека (тип молока, вырабатываемого на последних стадиях беременности), обеспечивая столь необходимую иммунную поддержку новорожденным. [16] Широко распространено мнение, что лактоферрин является лишь бактериостатическим средством из-за его высокого сродства к железу и способности связывать свободные атомы железа из патогенных микробов. Однако теперь известно, что основная антимикробная движущая сила заключается в бактерицидных свойствах его железосвязанного кармана и специфического пептида лактоферрицина, расположенного в N-доле. Лактоферрин способен связываться со слоем ЛПС ( липополисахарида ) бактерий, а в его голо-форме атом железа окисляет липополисахариды, лизируя внешнюю мембрану и одновременно производя токсичную перекись водорода. [17] Кроме того, при расщеплении лактоферрина трипсином образуется пептид лактоферрицин, который связывается с H. + -АТФаза, нарушающая транслокацию протонов и в конечном итоге убивающая клетку. [18]
Ферритин
[ редактировать ]
Ферритин является резервуаром железа для отдельной клетки. Он обнаружен во всех типах клеток и локализуется в цитозоле. Ферритин — это большой белок, состоящий из 24 субъединиц, окружающих ядро, полное атомов железа. Он способен удерживать 0-4500 атомов железа, [19] который можно использовать в качестве резервуара для клеточных нужд. Железо сохраняется, когда его избыток, и извлекается, когда железо снова необходимо. [12] Субъединицы представляют собой смесь H (тяжелая или сердечная) и L (легкая или печеночная). Субъединицы образуют кластер шириной 70-80 Ангстрем, который затем заполняется ферригидритом железа. [20]
Ферритин является высококонсервативным белком во всех сферах жизни. Он настолько консервативен, что субъединицы лошадей и людей могут собираться вместе в функциональный белок. [12] Каждая субъединица состоит из пяти альфа-спиралей.
Ферритин используется для диагностики низкого уровня железа у людей. [19] Его можно использовать для определения уровня биодоступного железа, что полезно для диагностики анемии. Обычный диапазон для мужчин составляет 18–270 нг/мл, а для женщин — 18–160 нг/мл. [21]
См. также
[ редактировать ]Внешние ссылки
[ редактировать ]- Железосвязывающие + белки Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)
Ссылки
[ редактировать ]- ^ Брок Дж. Х. (1989). «Железосвязывающие белки». Acta Paediatrica Scandinavica. Добавка . 361 : 31–43. дои : 10.1111/apa.1989.78.s361.31 . ПМИД 2485582 . S2CID 44752615 .
- ^ Де Соуза М., Бридвелт Ф., Дайнезиус-Трентэм Р., Трентам Д., Лам Дж. (1988). «Железо, железосвязывающие белки и клетки иммунной системы». Анналы Нью-Йоркской академии наук . 526 (1): 310–22. Бибкод : 1988NYASA.526..310S . дои : 10.1111/j.1749-6632.1988.tb55515.x . ПМИД 3291685 . S2CID 12756539 .
- ^ Каплан Дж., Уорд DM (август 2013 г.). «Основная природа использования и регулирования железа» . Современная биология . 23 (15): Р642-6. дои : 10.1016/j.cub.2013.05.033 . ПМЦ 3928970 . ПМИД 23928078 .
- ^ Соломон Э.И., Брунольд Т.К., Дэвис М.И., Кемсли Дж.Н., Ли С.К., Ленерт Н., Низ Ф., Скулан А.Дж., Ян Ю.С., Чжоу Дж. (январь 2000 г.). «Геометрические и электронные корреляции структуры и функции в ферментах негемового железа». Химические обзоры . 100 (1): 235–350. дои : 10.1021/cr9900275 . ПМИД 11749238 .
- ^ Ченг AX, Хан XJ, Ву YF, Лу HX (январь 2014 г.). «Функция и катализ 2-оксоглутарат-зависимых оксигеназ, участвующих в биосинтезе флавоноидов растений» . Международный журнал молекулярных наук . 15 (1): 1080–95. дои : 10.3390/ijms15011080 . ПМЦ 3907857 . ПМИД 24434621 .
- ^ Менис, Оскар (1968). «Техническая нота 454» . Секция аналитической координации химии: сводная информация о деятельности с июля 1967 г. по июнь 1968 г. Гейтерсбург, доктор медицинских наук: Секция аналитической координации химии, Отделение аналитической химии, Институт исследования материалов. дои : 10.6028/nbs.tn.454 .
- ^ Михайлеску М.Р., Руссу И.М. (март 2001 г.). «Признак перехода T → R в гемоглобине человека» . Труды Национальной академии наук Соединенных Штатов Америки . 98 (7): 3773–7. Бибкод : 2001PNAS...98.3773M . дои : 10.1073/pnas.071493598 . ПМК 31128 . ПМИД 11259676 .
- ^ Берг Дж. М., Тимочко Дж. Л., Страйер Л. (2002). Биохимия (5-е изд.). Нью-Йорк: WH Freeman. ISBN 0716730510 . OCLC 48055706 .
- ^ Хассельбальх К.А. (декабрь 1964 г.). «Расчет концентрации ионов водорода в крови по связыванию свободного и связанного углекислого газа с кислородом в зависимости от Ph». Обзор анестезиологии . 8 (6): 607–32. дои : 10.1097/00132586-196412000-00059 .
- ^ Л., Ленинджер, Альберт (2000). Ленингерские принципы биохимии . Нельсон, Дэвид Л. (Дэвид Ли), 1942-, Кокс, Майкл М. (3-е изд.). Нью-Йорк: Издательство Worth. ISBN 1572591536 . OCLC 42619569 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Джонсон, Дебора К.; Дин, Деннис Р.; Смит, Арчер Д.; Джонсон, Майкл К. (18 февраля 2005 г.). «Структура, функции и формирование биологических железо-серных кластеров». Ежегодный обзор биохимии . 74 (1): 247–281. doi : 10.1146/annurev.biochem.74.082803.133518 . ISSN 0066-4154 . ПМИД 15952888 .
- ^ Jump up to: а б с Айсен П., Эннс К., Весслинг-Ресник М. (октябрь 2001 г.). «Химия и биология метаболизма железа у эукариот». Международный журнал биохимии и клеточной биологии . 33 (10): 940–59. дои : 10.1016/s1357-2725(01)00063-2 . ПМИД 11470229 .
- ^ «TF - предшественник серотрансферрина - Homo sapiens (человек) - ген и белок TF» . www.uniprot.org . Проверено 11 ноября 2018 г.
- ^ Бейкер Э.Н., Бейкер Х.М. (ноябрь 2005 г.). «Молекулярная структура, связывающие свойства и динамика лактоферрина» . Клеточные и молекулярные науки о жизни . 62 (22): 2531–9. дои : 10.1007/s00018-005-5368-9 . ПМЦ 11139133 . ПМИД 16261257 . S2CID 218464085 .
- ^ Мазурье Дж., Спик Дж. (май 1980 г.). «Сравнительное изучение железосвязывающих свойств трансферринов человека. I. Полное и последовательное насыщение железом и десатурация лактотрансферрина». Биохимика и биофизика Acta . 629 (2): 399–408. дои : 10.1016/0304-4165(80)90112-9 . ПМИД 6770907 .
- ^ Санчес Л., Кальво М., Брок Дж. Х. (май 1992 г.). «Биологическая роль лактоферрина» . Архив болезней в детстве . 67 (5): 657–61. дои : 10.1136/adc.67.5.657 . ПМЦ 1793702 . ПМИД 1599309 .
- ^ Фарно С., Эванс Р.В. (ноябрь 2003 г.). «Лактоферрин - многофункциональный белок с антимикробными свойствами». Молекулярная иммунология . 40 (7): 395–405. дои : 10.1016/S0161-5890(03)00152-4 . PMID 14568385 .
- ^ Кувата Х, Йип Т.Т., Йип КЛ, Томита М., Хатченс Т.В. (апрель 1998 г.). «Бактерицидный домен лактоферрина: обнаружение, количественное определение и характеристика лактоферрицина в сыворотке с помощью аффинной масс-спектрометрии SELDI». Связь с биохимическими и биофизическими исследованиями . 245 (3): 764–73. дои : 10.1006/bbrc.1998.8466 . ПМИД 9588189 .
- ^ Jump up to: а б Эндрюс, Северная Каролина (июль 2008 г.). «Ковка поля: золотой век биологии железа» . Кровь . 112 (2): 219–30. дои : 10.1182/кровь-2007-12-077388 . ПМЦ 2442739 . ПМИД 18606887 .
- ^ Крайтон Р.Р., Шарлото-Вотерс М. (май 1987 г.). «Транспортировка и хранение железа» . Европейский журнал биохимии . 164 (3): 485–506. дои : 10.1111/j.1432-1033.1987.tb11155.x . ПМИД 3032619 .
- ^ «Что такое анализ крови на ферритин? Что означают результаты?» . ВебМД . Проверено 11 ноября 2018 г.