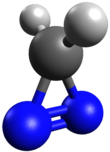Диазирин
| |||
| Идентификаторы | |||
|---|---|---|---|
| |||
3D model ( JSmol )
|
|||
| 605387 | |||
| КЭБ |
| ||
| ХимическийПаук |
| ||
ПабХим CID
|
| ||
Панель управления CompTox ( EPA )
|
| ||
| Характеристики | |||
| Ч 2 Н 2 | |||
| Молярная масса | 42.041 g·mol −1 | ||
| Родственные соединения | |||
Родственные соединения
|
1H-диазирин | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||

В органической химии диазирины представляют собой класс органических молекул, состоящих из углерода , связанного с двумя атомами азота , которые соединены двойной связью друг с другом, образуя циклопропен -подобное кольцо, 3 H -диазирин ( >CN 2 ). Они изомерны диазоуглеродным ( группам >C=N=N ) и подобно им могут служить предшественниками карбенов за счет потери молекулы диазота. Например, облучение диазиринов ультрафиолетовым светом приводит к внедрению карбена в различные C−H , N-H и связи O-H . [ 1 ] Таким образом, диазирины приобрели популярность как небольшие фотореактивные реагенты сшивающие . [ 2 ] Их часто используют в исследованиях фотоаффинного мечения для наблюдения различных взаимодействий, включая взаимодействия лиганд -рецептор, лиганд- фермент , белок-белок и белок- нуклеиновая кислота . [ 3 ]
Синтез
[ редактировать ]В литературе существует ряд методов получения диазиринов, которые начинаются с использованием различных реагентов. [ 4 ]
Синтез из кетонов
[ редактировать ]Как правило, синтетические схемы, начинающиеся с кетонов ( >C=O ) включают превращение кетона с желаемыми заместителями в диазиридины ( >CN 2 H 2 ). Эти диазиридины затем впоследствии окисляются с образованием желаемых диазиринов.
Диазиридины можно получить из кетонов путем оксимации с последующим тозилированием (или мезилированием ) и, наконец, обработкой аммиаком ( НХ 3 ). Обычно реакции оксимации осуществляются путем взаимодействия кетона с хлоридом гидроксиламмония ( NH3NH3OH − кл. + ) при нагревании в присутствии такого основания , как пиридин . [ 5 ] [ 6 ] Последующее тозилирование или мезилирование альфа-замещенного кислорода тозил- или мезилхлоридом в присутствии основания дает тозил- или мезилоксим . [ 7 ] Окончательная обработка тозила или мезилоксима аммиаком дает диазиридин. [ 1 ] [ 3 ] [ 7 ] [ 8 ]

Диазиридины также можно получать непосредственно реакцией кетонов с аммиаком в присутствии аминирующего агента, такого как монохлорамин или гидроксиламин О-сульфоновой кислоты. [ 9 ]
Диазиридины можно окислить до диазиринов рядом методов. К ним относятся окисление реагентами на основе хрома , такое как окисление Джонса , [ 10 ] окисление йодом и триэтиламином , [ 5 ] окисление оксидом серебра , [ 11 ] окисление оксалилхлоридом, [ 7 ] или даже электрохимическое окисление на платиново-титановом аноде. [ 12 ]

Синтез по реакции Грэма
[ редактировать ]Альтернативно диазирины можно получить в однореакторном процессе с использованием реакции Грэма , начиная с амидинов . [ 13 ] В результате этой реакции образуется галогенированный диазирин, галоген которого может быть заменен различными нуклеофильными реагентами. [ 14 ]
Химия
[ редактировать ]При облучении УФ-светом диазирины образуют реакционноспособные карбеновые формы. Карбен может существовать в синглетной форме, в которой два свободных электрона занимают одну и ту же орбиталь, или в триплетной форме с двумя неспаренными электронами на разных орбиталях.
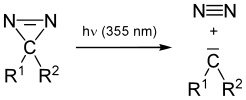
Продукты триплетного и синглетного карбена
[ редактировать ]Заместители в диазирине влияют на то, какие виды карбенов образуются при облучении и последующем фотолитическом расщеплении. Диазириновые заместители, которые по своей природе являются электронодонорными, могут отдавать электронную плотность пустой p-орбитали образующегося карбена и, следовательно, могут стабилизировать синглетное состояние. Например, фенилдиазирин образует фенилкарбен в состоянии синглетного карбена. [ 15 ] тогда как 3-хлор-3-[(4-нитрофенил)метил]диазирин или трифторметилфенилдиазирин образуют соответствующие триплетные карбеновые продукты. [ 16 ] [ 17 ]
Электронодонорные заместители также могут способствовать фотоизомеризации в линейное диазосоединение. [ 18 ] а не синглетный карбен, и, следовательно, эти соединения неблагоприятны для использования в биологических анализах. [ 19 ] С другой стороны, трифторарилдиазирины особенно проявляют благоприятную стабильность и фотолитические свойства. [ 19 ] и чаще всего используются в биологических приложениях. [ 1 ]

Карбены, полученные из диазиринов, быстро гасятся в результате реакции с молекулами воды. [ 20 ] и, следовательно, выходы фотореактивных анализов сшивки часто бывают низкими. Тем не менее, поскольку эта особенность сводит к минимуму неспецифическую маркировку, на самом деле это является преимуществом использования диазиринов.
Использование в фотореактивном сшивании.
[ редактировать ]Диазирины часто используются в качестве фотореактивных сшивающих реагентов, поскольку реакционноспособные карбены, которые они образуют при облучении УФ-светом, могут внедряться в связи CH, NH и OH. Это приводит к зависимому от близости мечению других видов соединением, содержащим диазирин.
Диазирины часто предпочтительнее других фотореактивных сшивающих реагентов из-за их меньшего размера, большей длины волны облучения, короткого требуемого периода облучения и стабильности в присутствии различных нуклеофилов, как в кислых, так и в основных условиях. [ 21 ] Бензофеноны , которые при облучении образуют реакционноспособные триплетные карбонильные группы, часто требуют длительных периодов облучения, что может привести к неспецифическому мечению, и, кроме того, часто инертны к различным полярным растворителям. [ 22 ] Арилазиды требуют облучения с низкой длиной волны, которое может повредить исследуемые биологические макромолекулы.
Примеры исследований по мечению рецепторов
[ редактировать ]Диазирины широко используются в исследованиях по мечению рецепторов. Это связано с тем, что диазиринсодержащие аналоги различных лигандов можно синтезировать и инкубировать с соответствующими рецепторами, а затем подвергать воздействию света для получения реакционноспособных карбенов. Карбен ковалентно связывается с остатками в сайте связывания рецептора. Карбеновое соединение может включать биоортогональную метку или ручку, с помощью которой можно выделить интересующий белок. Затем белок можно переварить и секвенировать с помощью масс-спектрометрии, чтобы определить, с какими остатками связан карбенсодержащий лиганд, и, следовательно, идентифицировать сайт связывания в рецепторе.
Примеры диазиринов, используемых в исследованиях по мечению рецепторов, включают:
- Открытие Киношитой и соавт. брассиностероидного рецептора брассиностероидных растительных гормонов. Исследователи использовали аналог растительного гормона с диазириновой сшивающей группой и биотиновой меткой для выделения и идентификации нового рецептора. [ 23 ] Это исследование привело к ряду аналогичных исследований, проведенных в отношении других растительных гормонов.

- Открытие новых каннабиноидных рецепторов, не относящихся к CB1/CB2, с использованием зондов-аналогов анандамида , содержащих группу диазирина, Balas et al. [ 24 ]
- Полость связывания снотворного агента пропофола в ГАМК А рецепторе с использованием диазиринсодержащего аналога пропофола. [ 25 ]
Примеры исследований фермент-субстрата
[ редактировать ]Аналогично мечению рецепторов, диазиринсодержащие соединения, являющиеся аналогами природных субстратов, также использовались для идентификации карманов связывания ферментов. Примеры включают в себя:
- Синтез диазиринсодержащего аналога этопозида , широко используемого противоракового препарата, нацеленного на топоизомеразу II , который обещает идентифицировать сайт связывания этопозида. [ 26 ]

- Открытие того, что ингибиторы гамма-секретазы капролактамного типа нацелены на субъединицу SPP гамма-секретазы , которая связана с болезнью Альцгеймера. [ 27 ]
Примеры исследований нуклеиновых кислот
[ редактировать ]Диазирины также использовались в экспериментах по фотоаффинному мечению с участием нуклеиновых кислот. Примеры включают в себя:
- Включение диазиринового фрагмента в нуклеозидный сахар в полимер ДНК для исследования взаимодействий между малой бороздкой ДНК и ДНК-полимеразами. [ 28 ]

- Включение диазиринового фрагмента в нуклеозидное основание в полимер ДНК для исследования способа репарации ДНК белками. [ 29 ]

Диазирины также использовались для изучения белково-липидных взаимодействий, например взаимодействия различных сфинголипидов с белками in vivo. [ 30 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с Дубинский, Люба; Кром, Бастиан П.; Мейлер, Майкл М. (15 января 2012 г.). «Фотоаффинная маркировка на основе диазирина». Биоорганическая и медицинская химия . Химическая протеомика. 20 (2): 554–570. дои : 10.1016/j.bmc.2011.06.066 . ПМИД 21778062 .
- ^ Хилл, Джеймс Р.; Робертсон, Аврил AB (2018). «Поиск мишеней для лекарств: фокус на синтезе диазиринового фотоаффинного зонда» . Журнал медицинской химии . 61 (16): 6945–6963. doi : 10.1021/acs.jmedchem.7b01561 . ПМИД 29683660 .
- ^ Перейти обратно: а б Синц, Андреа (1 апреля 2007 г.). «Исследование белок-лигандных взаимодействий методом масс-спектрометрии». ХимМедХим . 2 (4): 425–431. дои : 10.1002/cmdc.200600298 . ISSN 1860-7187 . ПМИД 17299828 . S2CID 23769515 .
- ^ Хилл, Джеймс Р.; Робертсон, Аврил AB (2018). «Поиск мишеней для лекарств: фокус на синтезе диазиринового фотоаффинного зонда» . Журнал медицинской химии . 61 (16): 6945–6963. doi : 10.1021/acs.jmedchem.7b01561 . ПМИД 29683660 .
- ^ Перейти обратно: а б Буркард, Надя; Бендер, Тобиас; Вестмайер, Йоханнес; Нардманн, Кристиан; Хасс, Маркус; Вечорек, Хельмут; Гронд, Стефани; Зезшвиц, Паультео (01 апреля 2010 г.). «Новые фтористые фотоаффинные метки (F-PAL) и их применение в исследованиях ингибирования V-АТФазы». Европейский журнал органической химии . 2010 (11): 2176–2181. дои : 10.1002/ejoc.200901463 . ISSN 1099-0690 .
- ^ Сун, Чжицюань; Чжан, Цишэн (5 ноября 2009 г.). «Реагенты для фотоаффинного мечения фторсодержащего арилдиазирина». Органические письма . 11 (21): 4882–4885. дои : 10.1021/ol901955y . ISSN 1523-7060 . ПМИД 19807115 .
- ^ Перейти обратно: а б с Кумар, Наг С.; Янг, Роберт Н. (1 августа 2009 г.). «Разработка и синтез универсальной 3-(1,1-дифторпроп-2-инил)-3H-диазирин-3-ильной функциональной группы для фотоаффинного мечения». Биоорганическая и медицинская химия . 17 (15): 5388–5395. дои : 10.1016/j.bmc.2009.06.048 . ПМИД 19604700 .
- ^ Гу, Мин; Ян, Цзяньбинь; Бай, Чжиян; Чен, Юэ-Тин; Лу, Вэй; Тан, Цзе; Дуань, Люшэн; Се, Даосинь; Нан, Фа-Цзюнь (01 мая 2010 г.). «Разработка и синтез меченных биотином фотоаффинных зондов жасмонатов». Биоорганическая и медицинская химия . 18 (9): 3012–3019. дои : 10.1016/j.bmc.2010.03.059 . ПМИД 20395151 .
- ^ Дубинский, Люба; Ярош, Люся М.; Амара, Нери; Криф, Пнина; Кравченко Владимир Владимирович; Кром, Бастиан П.; Мейлер, Майкл М. (24 ноября 2009 г.). «Синтез и проверка зонда для идентификации рецепторов, чувствительных к кворуму». Химические коммуникации (47): 7378–7380. дои : 10.1039/b917507e . ПМИД 20024234 .
- ^ Вагнер, Джеральд; Нолл, Вольфганг; Бобек, Майкл М.; Брекер, Лотар; ван Хервинен, Хендрикус В.Г.; Бринкер, Удо Х. (15 января 2010 г.). «Взаимоотношения структура-реактивность: реакции 5-замещенного азиадамантана в кавитанде на основе резорцина [4] арена». Органические письма . 12 (2): 332–335. дои : 10.1021/ol902667a . ISSN 1523-7060 . ПМИД 20017550 .
- ^ Аль-Омари, Мохаммед; Банерт, Клаус; Хагедорн, Манфред (1 января 2006 г.). «Би-3H-диазирин-3-илы как предшественники высоконапряженных циклоалкинов». Angewandte Chemie, международное издание . 45 (2): 309–311. дои : 10.1002/anie.200503124 . ISSN 1521-3773 . ПМИД 16372311 .
- ^ Vedenyapina, M. D.; Kuznetsov, V. V.; Nizhnikovskii, E. A.; Strel’tsova, E. D.; Makhova, N. N.; Struchkova, M. I.; Vedenyapin, A. A. (2006-11-01). "Electrochemical synthesis of pentamethylenediazirine". Russian Chemical Bulletin . 55 (11): 2013–2015. doi : 10.1007/s11172-006-0544-0 . ISSN 1066-5285 . S2CID 97472127 .
- ^ Грэм, Вашингтон (1 октября 1965 г.). «Галогенирование амидинов. I. Синтез 3-галоген- и других отрицательно замещенных диазиринов1». Журнал Американского химического общества . 87 (19): 4396–4397. дои : 10.1021/ja00947a040 . ISSN 0002-7863 .
- ^ Мосс, Роберт А. (9 февраля 2006 г.). «Диазирины: превосходные предшественники карбена». Отчеты о химических исследованиях . 39 (4): 267–272. дои : 10.1021/ar050155h . ISSN 0001-4842 . ПМИД 16618094 .
- ^ Чжан, Юньлун; Бурдзинский, Готар; Кубицки, Яцек; Платц, Мэтью С. (3 декабря 2008 г.). «Прямое наблюдение образования карбена и диазо из арилдиазиринов с помощью сверхбыстрой инфракрасной спектроскопии». Журнал Американского химического общества . 130 (48): 16134–16135. дои : 10.1021/ja805922b . ISSN 0002-7863 . ПМИД 18998681 .
- ^ Ноллер, Бастиан; Пуассон, Лайонел; Максименко, Романов; Гобер, Оливер; Фишер, Инго; Местдаг, Дж. М. (2 апреля 2009 г.). «Сверхбыстрая динамика изолированных фенилкарбенов с последующим получением карты скоростей с фемтосекундным разрешением». Журнал физической химии А. 113 (13): 3041–3050. Бибкод : 2009JPCA..113.3041N . дои : 10.1021/jp810974m . ISSN 1089-5639 . ПМИД 19245233 .
- ^ Ноллер, Бастиан; Хембергер, Патрик; Фишер, Инго; Алькарас, Кристиан; Гарсия, Густаво А.; Солди-Лозе, Элоиза (23 июня 2009 г.). «Фотоионизация двух фенилкарбенов и их предшественников диазиринов, исследованная с помощью синхротронного излучения» . Физическая химия Химическая физика . 11 (26): 5384–5391. Бибкод : 2009PCCP...11.5384N . дои : 10.1039/b823269e . ПМИД 19551206 .
- ^ Корнеев, Сергей М. (ноябрь 2011 г.). «Валентная изомеризация диазосоединений и диазиринов» . Европейский журнал органической химии . 2011 (31): 6153–6175. дои : 10.1002/ejoc.201100224 . ISSN 1434-193Х .
- ^ Перейти обратно: а б Бруннер, Дж.; Сенн, Х.; Ричардс, FM (25 апреля 1980 г.). «3-Трифторметил-3-фенилдиазирин. Новая карбенобразующая группа для реагентов для фотомечения» . Журнал биологической химии . 255 (8): 3313–3318. дои : 10.1016/S0021-9258(19)85701-0 . ISSN 0021-9258 . ПМИД 7364745 .
- ^ Ван, Джин; Кубицки, Яцек; Пэн, Хуолей; Платц, Мэтью С. (1 мая 2008 г.). «Влияние растворителя на скорость межсистемного перехода карбена». Журнал Американского химического общества . 130 (20): 6604–6609. дои : 10.1021/ja711385t . ISSN 0002-7863 . ПМИД 18433130 .
- ^ Хатанака, Ясумару; Садаканэ, Ютака (01 марта 2002 г.). «Фотоаффинная маркировка при открытии и разработке лекарств: химические ворота для выхода на протеомные рубежи». Актуальные темы медицинской химии . 2 (3): 271–288. дои : 10.2174/1568026023394182 . ISSN 1568-0266 . ПМИД 11944820 .
- ^ Прествич, Гленн Д.; Дорман, Дьёрдь; Эллиотт, Джон Т.; Маречак, Дейл М.; Чаудхари, Ану (1 февраля 1997 г.). «Бензофеноновые фотозонды для фосфоинозитидов, пептидов и лекарств». Фотохимия и фотобиология . 65 (2): 222–234. дои : 10.1111/j.1751-1097.1997.tb08548.x . ISSN 1751-1097 . ПМИД 9066302 . S2CID 12577596 .
- ^ Киносита, Тошинори; Каньо-Дельгадо, Ана; Сето, Хидехару; Хиранума, Сайоко; Фудзиока, Сёдзо; Ёсида, Сигео; Чори, Джоан (2005). «Связывание брассиностероидов с внеклеточным доменом киназы растительного рецептора BRI1». Природа . 433 (7022): 167–171. Бибкод : 2005Natur.433..167K . дои : 10.1038/nature03227 . ПМИД 15650741 . S2CID 4379617 .
- ^ Балас, Лоуренс; Дюран, Тьерри; Саха, Саттьябрата; Джонсон, Иннеке; Мукхопадьяй, Сомнатх (26 февраля 2009 г.). «Полный синтез фотоактивируемых или флуоресцентных анандамидных зондов: новые биоактивные соединения с ангиогенной активностью». Журнал медицинской химии . 52 (4): 1005–1017. дои : 10.1021/jm8011382 . ISSN 0022-2623 . ПМИД 19161308 .
- ^ Холл, Майкл А.; Си, Цзинь; Лор, Чонг; Дай, Шуйпин; Пирс, Роберт; Дейли, Уильям П.; Экенхофф, Родерик Г. (12 августа 2010 г.). «М-азипропофол (AziPm) — фотоактивный аналог внутривенного общего анестетика пропофола» . Журнал медицинской химии . 53 (15): 5667–5675. дои : 10.1021/jm1004072 . ISSN 0022-2623 . ПМК 2917171 . ПМИД 20597506 .
- ^ Чи, Гайк-Лин; Ялович, Джек С.; Боднер, Эндрю; У, Син; Хасинофф, Брайан Б. (15 января 2010 г.). «Фотоаффинный этопозидный зонд на основе диазирина для мечения топоизомеразы II» . Биоорганическая и медицинская химия . 18 (2): 830–838. дои : 10.1016/j.bmc.2009.11.048 . ПМЦ 2818565 . ПМИД 20006518 .
- ^ Фува, Харухико; Такахаси, Ясуко; Конно, Ю; Ватанабэ, Наото; Мияшита, Хироюки; Сасаки, Макото; Нацугари, Хидеаки; Кан, Тосиюки; Фукуяма, Тору (1 июня 2007 г.). «Дивергентный синтез многофункциональных молекулярных зондов для выяснения ферментативной специфичности дипептидных ингибиторов γ-секретазы». АКС Химическая биология . 2 (6): 408–418. дои : 10.1021/cb700073y . ISSN 1554-8929 . ПМИД 17530731 .
- ^ Либманн, Майке; Ди Паскуале, Франческа; Маркс, Андреас (4 декабря 2006 г.). «Новый фотоактивный строительный блок для исследования взаимодействий остова ДНК: фотоаффинная маркировка ДНК-полимеразы β человека». ХимБиоХим . 7 (12): 1965–1969. дои : 10.1002/cbic.200600333 . ISSN 1439-7633 . ПМИД 17106908 . S2CID 22908416 .
- ^ Виннакер, Мальте; Бригер, Саша; Штрассер, Ральф; Карелл, Томас (5 января 2009 г.). «Новые диазиринсодержащие ДНК-фотоаффинные зонды для исследования взаимодействий ДНК и белков». ХимБиоХим . 10 (1): 109–118. дои : 10.1002/cbic.200800397 . ISSN 1439-7633 . ПМИД 19012292 . S2CID 5605171 .
- ^ Ямамото, Тецуя; Хасэгава, Хироко; Хакоги, Тошиказу; Кацумура, Сигео (1 ноября 2006 г.). «Универсальный синтетический метод получения сфинголипидов и функционализированных производных сфингозина посредством перекрестного метатезиса олефинов». Органические письма . 8 (24): 5569–5572. дои : 10.1021/ol062258l . ISSN 1523-7060 . ПМИД 17107074 .