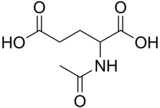
N -ацетилглутаминовая кислота
| |
| Имена | |
|---|---|
| Название ИЮПАК
2-ацетамидопентандиовая кислота [ 1 ]
| |
| Другие имена
Ацетилглутаминовая кислота [ нужна ссылка ]
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 3DMeet | |
| Сокращения |
|
| 1727473 С | |
| КЭБ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.024.899 |
| Номер ЕС |
|
| КЕГГ | |
| МеШ | N-ацетилглутамат |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 7 Н 11 Н О 5 | |
| Молярная масса | 189.167 g·mol −1 |
| Появление | Белые кристаллы |
| Плотность | 1 г мл −1 |
| Температура плавления | От 191 до 194 ° C (от 376 до 381 ° F; от 464 до 467 К) |
| 36 г л −1 | |
| Опасности | |
| Летальная доза или концентрация (LD, LC): | |
ЛД 50 ( средняя доза )
|
>7 г кг −1 (оральный, крыса) |
| Родственные соединения | |
Родственные алкановые кислоты
|
|
Родственные соединения
|
|
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
N -Ацетилглутаминовая кислота (также называемая N -ацетилглутамат , сокращенно НАГ , химическая формула C 7 H 11 NO 5 ) [ 2 ] биосинтезируется из глутамата и ацетилорнитина с помощью орнитинацетилтрансферазы и из глутаминовой кислоты и ацетил-КоА с помощью фермента N -ацетилглутаматсинтазы . Обратная реакция — гидролиз ацетильной группы — катализируется специфической гидролазой . Это первый промежуточный продукт, участвующий в биосинтезе аргинина у прокариот и простых эукариот, а также регулятор процесса, известного как цикл мочевины , который превращает токсичный аммиак в мочевину для выведения из организма у позвоночных.
Открытие
[ редактировать ]N -ацетилглутаминовая кислота представляет собой внеклеточный метаболит, выделенный из прокариот Rhizobium trifolii, который был охарактеризован с использованием многих методов определения структуры, таких как протонный ядерный магнитный резонанс ( 1 H ЯМР) спектроскопия, инфракрасная спектроскопия с преобразованием Фурье и газовая хроматография-масс-спектрометрия .
У Rhizobium внеклеточное накопление N -ацетилглутаминовой кислоты происходит за счет метаболизма с участием nod-фактора генов на симбиотической плазмиде . Когда nod-факторы мутируют, меньше N -ацетилглутаминовой кислоты. образуется [ 3 ]
Биосинтез
[ редактировать ]Прокариоты и простые эукариоты
[ редактировать ]У прокариот и простых эукариот N -ацетилглутаминовая кислота может продуцироваться N -ацетилглутаматсинтазой (NAGS) или орнитинацетилтрансферазой (ОАТ).
Синтез орнитинацетилтрансферазы (ОАТ)
[ редактировать ]ОАТ синтезирует N -ацетилглутаминовую кислоту из глутамата и ацетилорнитина и является методом выбора для производства у прокариот, которые обладают способностью синтезировать соединение орнитин . [ 4 ]
Синтез N -ацетилглутаматсинтазы (NAGS)
[ редактировать ]N -ацетилглутаматсинтаза представляет собой фермент, который служит пополнителем N -ацетилглутаминовой кислоты для восполнения любой N -ацетилглутаминовой кислоты, потерянной клеткой в результате митоза или деградации. NAGS синтезирует N -ацетилглутаминовую кислоту, катализируя присоединение ацетильной группы ацетил-кофермента А к глутамату . У прокариот с нециклической продукцией орнитина NAGS является единственным методом синтеза N- ацетилглутаминовой кислоты и ингибируется аргинином. [ 4 ] Считается, что ацетилирование глутамата предотвращает использование глутамата в биосинтезе пролина . [ 5 ]
Позвоночные животные
[ редактировать ]В отличие от прокариот, NAGS у млекопитающих усиливается аргинином и протаминами . Ингибируется N -ацетилглутаминовой кислотой и ее аналогами (другими N -ацетилированными соединениями). [ 4 ]
Мозг также содержит N -ацетилглутаминовую кислоту в следовых количествах, однако экспрессия NAGS не обнаружена. Это говорит о том, что N -ацетилглутаминовая кислота вырабатывается другим ферментом головного мозга, который еще предстоит определить. [ 4 ]
Биологические роли
[ редактировать ]Позвоночные животные и млекопитающие
[ редактировать ]В позвонках и млекопитающих N -ацетилглутаминовая кислота является аллостерической молекулой-активатором митохондриальной карбамилфосфатсинтетазы I (CPSI), которая является первым ферментом в цикле мочевины. [ 6 ] Он запускает выработку первого промежуточного продукта цикла мочевины — карбамилфосфата . CPSI неактивен в N отсутствие -ацетилглутаминовой кислоты. В печени и тонком кишечнике CPSI, зависимый от N -ацетилглутаминовой кислоты, производит цитруллин , второй промежуточный продукт в цикле мочевины. -ацетилглутаминовой кислоты в клетках печени Распределение N является самым высоким в митохондриях: 56% от общей доступности N -ацетилглутаминовой кислоты, 24% в ядре и оставшиеся 20% в цитозоле. Аминоацилаза I в клетках печени и почек расщепляет N -ацетилглутаминовую кислоту до глутамата и ацетата. [ 7 ] Напротив, N -ацетилглутаминовая кислота не является аллостерическим кофактором карбамилфосфатсинтетазы, обнаруженной в цитоплазме, которая участвует в синтезе пиримидина . [ 8 ]
Концентрации N -ацетилглутаминовой кислоты увеличиваются при увеличении потребления белка из-за накопления аммиака, который должен секретироваться в цикле мочевины, что подтверждает роль N -ацетилглутаминовой кислоты как кофактора для CPSI. Кроме того, N -ацетилглутаминовую кислоту можно найти во многих часто потребляемых продуктах, таких как соя, кукуруза и кофе, причем какао-порошок содержит особенно высокую концентрацию. [ 9 ]
Дефицит N -ацетилглутаминовой кислоты у человека является аутосомно-рецессивным заболеванием, которое приводит к блокировке выработки мочевины, что в конечном итоге увеличивает концентрацию аммиака в крови ( гипераммониемия ). Дефицит может быть вызван дефектами гена, кодирующего NAGS, или дефицитом предшественников, необходимых для синтеза. [ 4 ]
Бактерии
[ редактировать ]N -ацетилглутаминовая кислота является вторым промежуточным продуктом в пути производства аргинина в Escherichia coli и вырабатывается посредством NAGS. [ 5 ] В этом пути киназа N -ацетилглутаминовой кислоты (NAGK) катализирует фосфорилирование гамма-(третьей) карбоксильной группы N -ацетилглутаминовой кислоты с использованием фосфата, образующегося при ( АТФ гидролизе аденозинтрифосфата ). [ 10 ]
Корни рассады клевера белого
[ редактировать ]Ризобии могут вступать в симбиотические отношения с корнями проростков клевера белого и образовывать колонии. Внеклеточная N -ацетилглутаминовая кислота, продуцируемая этими бактериями, оказывает три морфологических эффекта на корни проростков клевера белого: ветвление корневых волосков, набухание кончиков корней и увеличение количества клеточных делений в недифференцированных клетках, обнаруженных в самом внешнем клеточном слое. корня. Это позволяет предположить, что N -ацетилглутаминовая кислота участвует в стимуляции митоза. Те же самые эффекты наблюдались на клевере земляничном , но не на бобовых . Воздействие N -ацетилглутаминовой кислоты на виды клевера было более сильным, чем воздействие глютамина , глутамата, аргинина или аммиака . [ 4 ]
Структура
[ редактировать ]
N -ацетилглутаминовая кислота состоит из двух групп карбоновой кислоты и амидной группы, выступающей от второго углерода. В структуре N -ацетилглутаминовой кислоты при физиологическом pH (7,4) все карбоксильные группы депротонированы .
Протонная ЯМР-спектроскопия
[ редактировать ]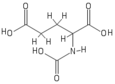

Молекулярная структура N -ацетилглутаминовой кислоты определена методом протонной ЯМР-спектроскопии . [ 3 ] Протонный ЯМР выявляет наличие и расположение функциональных групп протонов на основе химических сдвигов, зарегистрированных в спектре. [ 11 ]
13 C ЯМР-спектроскопия
[ редактировать ]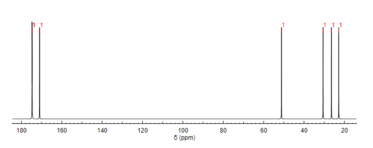
Как и протонный ЯМР, углерод-13 ( 13 В) ЯМР-спектроскопия - это метод, используемый для определения молекулярной структуры. 13 ЯМР 1С выявляет типы углерода, присутствующие в молекуле, на основе химических сдвигов, которые соответствуют определенным функциональным группам. В N- ацетилглутаминовой кислоте наиболее отчетливо присутствуют карбонильные атомы углерода благодаря трем карбонилсодержащим заместителям. [ 12 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ « N -Ацетил- DL -глутаминовая кислота. Краткое описание соединений» . Пабхим соединение . США: Национальный центр биотехнологической информации. 25 марта 2005 г. Идентификация . Проверено 25 июня 2012 г.
- ^ Пубхим. « N -Ацетил L -глутаминовая кислота» . pubchem.ncbi.nlm.nih.gov . Проверено 3 июня 2018 г.
- ^ Jump up to: а б Филип-Холлингсворт С., Холлингсворт Р.И., Даззо Ф.Б. (сентябрь 1991 г.). « N -ацетилглутаминовая кислота: внеклеточный сигнал Rhizobium trifolii ANU843, который вызывает ветвление корневых волосков и клубенькообразные зачатки в корнях белого клевера» . Журнал биологической химии . 266 (25): 16854–8. дои : 10.1016/S0021-9258(18)55380-1 . ПМИД 1885611 .
- ^ Jump up to: а б с д и ж Калдович Л., Тачман М. (июнь 2003 г.). « N -ацетилглутамат и его меняющаяся роль в ходе эволюции» . Биохимический журнал . 372 (Часть 2): 279–90. дои : 10.1042/BJ20030002 . ПМЦ 1223426 . ПМИД 12633501 .
- ^ Jump up to: а б Кальдара М., Дюпон Дж., Лерой Ф., Голдбетер А., Де Вюйст Л., Кунин Р. (март 2008 г.). «Биосинтез аргинина в Escherichia coli : экспериментальное возмущение и математическое моделирование» . Журнал биологической химии . 283 (10): 6347–58. дои : 10.1074/jbc.M705884200 . ПМИД 18165237 .
- ^ Аудиторе, Джозеф В.; Уэйд, Литтлтон; Олсон, Эрик Дж. (ноябрь 1966 г.). «Появление N -ацетил- L -глутаминовой кислоты в мозге человека». Журнал нейрохимии . 13 (11): 1149–1155. дои : 10.1111/j.1471-4159.1966.tb04272.x . ISSN 0022-3042 . ПМИД 5924663 . S2CID 43263361 .
- ^ Харпер М.С., Аманда Шен З., Барнетт Дж.Ф., Крсманович Л., Мире А., Делани Б. (ноябрь 2009 г.). « N -ацетилглутаминовая кислота: оценка острой и 28-дневной пероральной токсичности и генотоксичности при повторных дозах». Пищевая и химическая токсикология . 47 (11): 2723–9. дои : 10.1016/j.fct.2009.07.036 . ПМИД 19654033 .
- ^ Пелли Дж.В. (2007). «Глава 14: Пурин, пиримидин и одноуглеродный обмен». Интегрированная биохимия Elsevier . Эльзевир. стр. 117–122. дои : 10.1016/b978-0-323-03410-4.50020-1 . ISBN 978-0-323-03410-4 .
- ^ Хессион А.О., Эсри Э.Г., Крус Р.А., Максвелл К.А. (октябрь 2008 г.). « N -Ацетилглутамат и N -ацетиласпартат в соевых бобах ( Glycine max L.), кукурузе ( Zea mays L.), [исправленном] и других пищевых продуктах». Журнал сельскохозяйственной и пищевой химии . 56 (19): 9121–6. дои : 10.1021/jf801523c . ПМИД 18781757 .
- ^ Хиль Ортис Ф, Рамон Майкес С, Фита И, Рубио В (август 2003 г.). «Ход фосфора в реакции N -ацетил- L -глутаматкиназы, определенный по строению кристаллических комплексов, в том числе комплекса с AlF −
4 имитатор переходного состояния». Journal of Molecular Biology . 331 (1): 231–44. doi : 10.1016/S0022-2836(03)00716-2 . PMID 12875848 . - ^ "Предсказывать 1 Спектры ЯМР протонов H» . www.nmrdb.org . Проверено 3 июня 2018 г.
- ^ "Предсказывать 13 Спектры ЯМР углерода C» . www.nmrdb.org . Проверено 3 июня 2018 г.