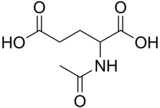
N -ацетилглютамическая кислота
| |
| Имена | |
|---|---|
| Имя IUPAC
2-ацетамидопентановая кислота [ 1 ]
| |
| Другие имена
Ацетилглютамическая кислота [ Цитация необходима ]
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 3dmet | |
| Сокращения |
|
| 1727473 с | |
| Чеби | |
| Chemspider | |
| Наркоман | |
| Echa Infocard | 100.024.899 |
| ЕС номер |
|
| Кегг | |
| Сетка | N-ацетилглютамат |
PubChem CID
|
|
| Rtecs номер |
|
| НЕКОТОРЫЙ |
|
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 7 H 11 N O 5 | |
| Молярная масса | 189.167 g·mol −1 |
| Появление | Белые кристаллы |
| Плотность | 1 г мл −1 |
| Точка плавления | 191–194 ° C (от 376 до 381 ° F; от 464 до 467 K) |
| 36 г л −1 | |
| Опасности | |
| Смертельная доза или концентрация (LD, LC): | |
Ld 50 ( средняя доза )
|
> 7 г кг −1 (устная крыса) |
| Связанные соединения | |
Связанные алкановые кислоты
|
|
Связанные соединения
|
|
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
N -ацетилглютамическая кислота (также называемая N -ацетилглютаматом , сокращенным NAG , химическая формула C 7 H 11 № 5 ) [ 2 ] биосинтезируется из глутамата и ацетилорнитина орнитинцетилтрансферазой и из глутаминовой кислоты и ацетил -КоА ферментом N -ацетилглютаматом синтазы . Обратная реакция, гидролиз ацетильной группы, катализируется специфической гидролазой . Это первое промежуточное соединение, участвующее в биосинтезе аргинина у прокариот и простых эукариот и регулятор в процессе, известного как цикл мочевины , который преобразует токсичный аммиак в мочевину для выведения из тела у позвоночных.
Открытие
[ редактировать ]N -ацетилглютамическая кислота является внеклеточным метаболитом, прокариота выделенным из Trifolii ризобия , который был охарактеризован с использованием множества методов определения структуры, таких как ядерный магнитный резонанс протона ( 1 H ЯМР) спектроскопия, инфракрасная спектроскопия Фурье и спектрометрия газовой хроматографии .
У ризобия внеклеточное наращивание N -ацетилглютамической кислоты обусловлено метаболизмом, включающим гены фактора NOD на симбиотической плазмиде . Когда коэффициенты модны мутированы, меньше N -ацетилглютамической кислоты. образуется [ 3 ]
Биосинтез
[ редактировать ]Прокариоты и простые эукариоты
[ редактировать ]У прокариот и простых эукариот N -ацетилглютаминовая кислота может быть получена с помощью N -ацетилглютаматсинтазы (NAGS) или орнитинцетилтрансферазы (OAT).
Синтез орнитин ацетилтрансферазы (овса)
[ редактировать ]Овсяный синтезирует N -ацетилглютамическую кислоту из глутамата и ацетилорнитина и является методом выбора для производства у прокариот, которые способны синтезировать соединение орнитина . [ 4 ]
N -ацетилглютаматсинтаза (NAGS)
[ редактировать ]N -ацетилглютамат -синтаза представляет собой фермент, который служит пополнителем N -ацетилглютамической кислоты для дополнения любой N -ацетилглютамической кислоты, потерянной клеткой за счет митоза или деградации. NAGS синтезирует N -ацетилглютамическую кислоту, катализируя добавление ацетильной группы из ацетил -кофермента А в глутамат . У прокариот с нециклическим производством орнитина NAGS является единственным методом синтеза N -ацетилглютамической кислоты и ингибируется аргинином. [ 4 ] Считается, что ацетилирование глутамата предотвращает использование глутамата с помощью биосинтеза пролина . [ 5 ]
Позвоночные
[ редактировать ]В отличие от прокариот, NAG у млекопитающих усиливается аргинином, наряду с протамининами . Он ингибируется N -ацетилглютамической кислотой и ее аналогами (другие N -ацетилированные соединения). [ 4 ]
Мозг также содержит N -ацетилглютамическую кислоту в следовых количествах, однако не обнаружено экспрессии NAG. Это говорит о том, что N -ацетилглютамическая кислота продуцируется другим ферментом в мозге, который еще предстоит определить. [ 4 ]
Биологические роли
[ редактировать ]Позвоночные и млекопитающие
[ редактировать ]У позвонков и млекопитающих н -ацетилглютамическая кислота является аллостерическая активаторная молекула для митохондриальной карбамилфосфат -синтетазы I (CPSI), которая является первым ферментом в цикле мочевины. [ 6 ] Это запускает производство первого промежуточного цикла мочевины, карбамилфосфата . CPSI неактивен, когда N -ацетилглютамическая кислота отсутствует. В печени и тонкой кишечнике N -ацетилглютаминовая кислота CPSI продуцирует цитруллин , второе промежуточное соединение в цикле мочевины. Распределение клеток печени N -ацетилглютамической кислоты является самым высоким в митохондриях в 56% от общей доступности N -ацетилглютамической кислоты, 24% в ядре и оставшихся 20% в цитозоле. Аминоацилаза I в клетках печени и почек разрушает н -ацетилглютамическую кислоту до глутамата и ацетата. [ 7 ] Напротив, N -ацетилглютамическая кислота не является аллостерической кофактором к карбамилфосфат -синтетазе, обнаруженной в цитоплазме, которая участвует в синтезе пиримидина . [ 8 ]
Концентрации N -ацетилглютамической кислоты увеличиваются, когда потребление белка увеличивается из -за накопления аммиака, которое должно быть секретироваться через цикл мочевины, что подтверждает роль N -ацетилглютамической кислоты в качестве кофактора CPSI. Кроме того, N -ацетилглютамическая кислота можно найти во многих часто потребляемых продуктах, таких как соя, кукуруза и кофе, с какао -порошком, содержащим особенно высокую концентрацию. [ 9 ]
Дефицит N -ацетилглютамической кислоты у людей является аутосомно -рецессивным расстройством, которое приводит к блокировке продукции мочевины, что в конечном итоге увеличивает концентрацию аммиака в крови ( гипераммонемия ). Дефицит может быть вызван дефектами в гене, кодирующем NAG, или с дефицитами в предшественниках, необходимых для синтеза. [ 4 ]
Бактерии
[ редактировать ]N -ацетилглютамическая кислота является вторым промежуточным в пути производства аргинина в Escherichia coli и производится через NAG. [ 5 ] В этом пути н -ацетилглютаминовая кислота киназа (NAGK) катализирует фосфорилирование гамма -карбоксильной группы N -ацетилглутамической кислоты с использованием фосфата, продуцируемого гидролизом аденозинового триперифата (ATP). [ 10 ]
Белые корни саженцев клевера
[ редактировать ]Ризобий может сформировать симбиотическую связь с белого клевера корнями и формировать колонии. Внеклеточная н -ацетилглютамическая кислота, продуцируемая этими бактериями корня. Это говорит о том, что N -ацетилглютамическая кислота участвует в стимуляции митоза. Те же эффекты наблюдались на клубничном клевере , но не в бобовых . Влияние N -ацетилглютамической кислоты на виды клеверов было более мощным, чем эффекты глутамина , глутамата, аргинина или аммиака . [ 4 ]
Структура
[ редактировать ]
N -ацетилглютамическая кислота состоит из двух групп карбоновой кислоты и амидной группы, выступающей от второго углерода. Структура N -ацетилглютамической кислоты при физиологическом рН (7,4) имеет все карбоксильные группы депротонированы .
Протон ЯМР спектроскопия
[ редактировать ]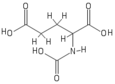

Молекулярную структуру N -ацетилглютамической кислоты определяли с использованием спектроскопии ЯМР протона . [ 3 ] Протон ЯМР выявляет присутствие и функциональную группу местоположения протонов на основе химических сдвигов, записанных в спектре. [ 11 ]
13 C ЯМР -спектроскопия
[ редактировать ]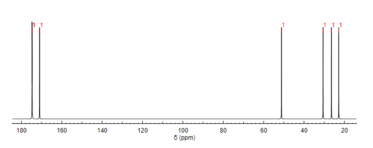
Как Proton ЯМР, Carbon-13 ( 13 C) ЯМР -спектроскопия - это метод, используемый при определении молекулярной структуры. 13 C ЯМР выявляет типы углеродов, присутствующих в молекуле на основе химических сдвигов, которые соответствуют определенным функциональным группам. N -ацетилглютамическая кислота имеет карбонильные углероды, наиболее отчетливо из -за трех заместителей карбонила. [ 12 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ « N -ацетил -дл -глютамическая кислота - краткое изложение» . Pubchem Compound . США: Национальный центр биотехнологической информации. 25 марта 2005 г. Идентификация . Получено 25 июня 2012 года .
- ^ Pubchem. « N -ацетил L -глютамическая кислота» . pubchem.ncbi.nlm.nih.gov . Получено 2018-06-03 .
- ^ Jump up to: а беременный Philip-Hollingsworth S, Hollingsworth RI, Dazzo FB (сентябрь 1991 г.). « N -ацетилглютамическая кислота: внеклеточный сигнал NOD Rhizobium trifolii anu843, который вызывает разветвление корневых волос и нордоподобные зачатки в белых корнях клевера» . Журнал биологической химии . 266 (25): 16854–8. doi : 10.1016/s0021-9258 (18) 55380-1 . PMID 1885611 .
- ^ Jump up to: а беременный в дюймовый и фон Caldovic L, Tuchman M (июнь 2003 г.). « N -ацетилглютамат и его изменяющаяся роль посредством эволюции» . Биохимический журнал . 372 (Pt 2): 279–90. doi : 10.1042/bj20030002 . PMC 1223426 . PMID 12633501 .
- ^ Jump up to: а беременный Caldara M, Dupont G, Leroy F, Goldbeter A, De Vuyst L, Cunin R (март 2008 г.). «Биосинтез аргинина в Escherichia coli : экспериментальное возмущение и математическое моделирование» . Журнал биологической химии . 283 (10): 6347–58. doi : 10.1074/jbc.m705884200 . PMID 18165237 .
- ^ Auditore, Joseph v.; Уэйд, Литтлтон; Олсон, Эрик Дж. (Ноябрь 1966 г.). «Появление n -ацетил -гглутаминовой кислоты в мозге человека». Журнал нейрохимии . 13 (11): 1149–1155. doi : 10.1111/j.1471-4159.1966.tb04272.x . ISSN 0022-3042 . PMID 5924663 . S2CID 43263361 .
- ^ Харпер М.С., Аманда Шен З., Барнетт Дж.Ф., Крсманович Л., Мире А., Делани Б. (ноябрь 2009 г.). « N -ацетил-глутаминовая кислота: оценка острой и 28-дневной повторной дозы пероральной токсичности и генотоксичности». Пищевая и химическая токсикология . 47 (11): 2723–9. doi : 10.1016/j.fct.2009.07.036 . PMID 19654033 .
- ^ Пелли Дж.В. (2007). «Глава 14: пуриновый, пиримидин и одноуглеродистый метаболизм». Интегрированная биохимия Elsevier . Elsevier. С. 117–122. doi : 10.1016/b978-0-323-03410-4.50020-1 . ISBN 978-0-323-03410-4 .
- ^ Hession AO, Esrey EG, Croes RA, Maxwell CA (октябрь 2008 г.). « N -ацетилглютамат и N -ацетиласпарт в соевых бобах ( глицин Max L.), кукуруза ( Zea Mays L.), [исправлено] и другие продукты питания». Журнал сельскохозяйственной и пищевой химии . 56 (19): 9121–6. doi : 10.1021/jf801523c . PMID 18781757 .
- ^ Гил Ортис Ф., Рамон Мейкес С., Фита I, Рубио V (август 2003 г.). "Курс фосфора в реакции N -ацетил -л -глютаматкиназы, определенной из структур кристаллических комплексов, включая комплекс с альф −
4 переходного состояния имитации ». Журнал молекулярной биологии . 331 (1): 231–44. DOI : 10.1016/S0022-2836 (03) 00716-2 . PMID 128758448 . - ^ "Предсказывать 1 H Proton NMR Spectra " . Www.nmrdb.org . Получено 2018-06-03 .
- ^ "Предсказывать 13 C Carbon NMR Spectra » . Www.nmrdb.org . Получено 2018-06-03 .