Глушитель (генетика)

В генетике сайленсером , называют последовательность ДНК способную связывать факторы регуляции транскрипции , называемые репрессорами . ДНК содержит гены и обеспечивает матрицу для производства информационной РНК (мРНК). Эта мРНК затем транслируется в белки. Когда белок-репрессор связывается с молчащим участком ДНК, РНК-полимераза не может транскрибировать последовательность ДНК в РНК. При блокированной транскрипции трансляция РНК в белки невозможна. Таким образом, сайленсеры предотвращают экспрессию генов в виде белков. [1]
РНК-полимераза, ДНК-зависимый фермент, транскрибирует последовательности ДНК, называемые нуклеотидами , в направлении от 3’ к 5’, в то время как комплементарная РНК синтезируется в направлении от 5’ к 3’. РНК похожа на ДНК, за исключением того, что РНК содержит урацил вместо тимина, который образует пару оснований с аденином. Важным регионом активности репрессии и экспрессии генов, обнаруженным в РНК, является 3'-нетранслируемый регион . Это область на 3'-конце РНК, которая не транслируется в белок, но включает множество регуляторных областей.
О глушителях пока мало что известно, но ученые продолжают исследования в надежде классифицировать больше типов, мест в геноме и заболеваний, связанных с глушителями. [2] [3]
Функциональность
[ редактировать ]Места внутри генома
[ редактировать ]
Сайленсером называют последовательность-специфичный элемент, который оказывает негативное влияние на транскрипцию конкретного гена. Существует множество положений, в которых элемент-сайлентер может располагаться в ДНК. Наиболее распространенное положение находится выше целевого гена, где оно может помочь подавить транскрипцию гена. [4] Это расстояние может сильно варьироваться от примерно -20 до -2000 п.н. перед геном. Определенные сайленсеры можно обнаружить после промотора, расположенного внутри интрона или экзона самого гена. Сайленсеры также были обнаружены в 3-м нетранслируемом участке (3'-UTR) мРНК. [5]
Типы
[ редактировать ]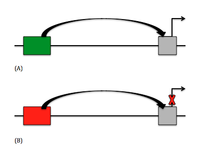
В настоящее время в ДНК существует два основных типа сайленсеров: классический сайленсер и неклассический негативный регуляторный элемент (NRE). В классических сайленсерах ген активно репрессируется элементом сайленсера, в основном за счет вмешательства в сборку общего транскрипционного фактора (GTF). [5] NRE пассивно репрессируют ген, обычно путем ингибирования других элементов, находящихся выше гена. Среди NRE существуют определенные сайленсеры, которые зависят от ориентации, что означает, что фактор связывания связывается в определенном направлении относительно других последовательностей. Зависимые от промотора сайленсеры понимаются как элементы сайленсера, поскольку они зависят от положения и ориентации, но также должны использовать фактор, специфичный для промотора. [5] Недавно были открыты элементы ответа группы Polycomb (PRE), которые могут разрешать и ингибировать репрессию в зависимости от связанного с ним белка и наличия некодирующей транскрипции. [4]
Механизмы
[ редактировать ]
Для классических глушителей сигнальный путь относительно прост. Поскольку репрессия активна, элементы сайленсера нацелены на сборку GTF, необходимых для транскрипции гена. Эти элементы-глушители в основном расположены выше гена и могут находиться на разных расстояниях как на коротких, так и на больших расстояниях. Было замечено, что в случае сайленсеров дальнего действия ДНК образует петлю, чтобы приблизить глушитель к промотору и замкнуть мешающую ДНК. [4] Сайленсеры также нацелены на участки геликазы в ДНК, которые богаты аденином и тимином (АТ) и склонны к раскручиванию ДНК, освобождая место для инициации транскрипции. Подавление активности геликазы приводит к ингибированию транскрипции. Это обычно наблюдается в промоторе гена тиротропина-β человека . NRE могут вызывать изгиб в промоторной области, чтобы блокировать взаимодействия, как это видно, когда NRE связывается с Инь-Ян 1 ( YY1 ), [5] а также фланговые регуляторные сигналы или области промотора. Когда область сайленсера расположена внутри интрона, могут быть два типа репрессии. Во-первых, может произойти физическая блокировка места сращивания. Во-вторых, в ДНК может возникнуть изгиб, который будет ингибировать процессинг РНК. [5]
Когда глушитель расположен в экзоне или нетранслируемой области, он в основном будет классическим или позиционно-зависимым. Однако эти сайленсеры могут осуществлять свою активность до транскрипции. [5] Большинство сайленсеров конститутивно экспрессируются в организмах, позволяя активировать ген только путем ингибирования сайленсера или активации области энхансера. Лучшим примером этого является нейронально-рестриктивный фактор сайленсера (NRSF), который вырабатывается геном REST . Ген REST продуцирует NRSF, чтобы подавить транскрипцию нейрональных генов, которые необходимы для локализации нейрональной ткани. Когда сайленсеры подавляют REST , NRSF также ингибируется, обеспечивая транскрипцию нейрональных генов. [5]
Сходства с усилителями
[ редактировать ]Другим регуляторным элементом, расположенным выше гена, является энхансер . Энхансеры действуют как переключатель «включения» экспрессии генов и активируют промоторную область определенного гена, тогда как сайленсеры действуют как переключатель «выключения». Хотя эти два регуляторных элемента действуют друг против друга, оба типа последовательностей влияют на промоторную область очень схожим образом. [4] Поскольку глушители не были тщательно идентифицированы и проанализированы, обширные исследования энхансеров помогли биологам понять механику глушителя. Энхансеры можно обнаружить во многих из тех же областей, что и сайленсеры, например, выше промотора на много пар тысяч оснований или даже ниже внутри интрона гена. [4] Зацикливание ДНК также является модельной функцией, используемой энхансерами для сокращения близости промотора к энхансеру. Энхансеры также функционируют с факторами транскрипции, чтобы инициировать экспрессию, так же, как сайленсеры могут действовать с репрессорами. [4]
У прокариот и эукариот
[ редактировать ]Прокариоты
[ редактировать ]
Существует несколько различий в регуляции метаболического контроля у эукариот и прокариот. Прокариоты варьируют количество специфических ферментов, вырабатываемых в их клетках, чтобы регулировать экспрессию генов, что представляет собой медленный метаболический контроль, а также регулировать ферментативные пути посредством таких механизмов, как ингибирование по обратной связи и аллостерическая регуляция , то есть быстрый метаболический контроль. [6] Гены прокариот сгруппированы по сходным функциям в единицы, называемые оперонами , которые состоят из промотора и оператора . Оператор является местом связывания репрессора и, таким образом, имеет функцию, эквивалентную области сайленсера в эукариотической ДНК. Когда белок-репрессор связан с оператором, РНК-полимераза не может связаться с промотором, чтобы инициировать транскрипцию оперона.
Репрессия lac оперона
[ редактировать ]Лак - оперон у прокариот E. coli состоит из генов, которые производят ферменты, расщепляющие лактозу. Его оперон является примером прокариотического глушителя. Три функциональных гена этого оперона — это lacZ, lacY и lacA. [6] Ген-репрессор lacI будет продуцировать белок-репрессор LacI, который находится под аллостерической регуляцией. Эти гены активируются наличием в клетке лактозы, которая действует как эффекторная молекула, связывающаяся с LacI. Когда репрессор связан с лактозой, он не связывается с оператором, что позволяет РНК-полимеразе связываться с промотором и инициировать транскрипцию оперона. Когда аллостерический сайт репрессора не связан с лактозой, его активный сайт будет связываться с оператором, чтобы предотвратить транскрипцию РНК-полимеразой генов lac- оперона.
Эукариоты
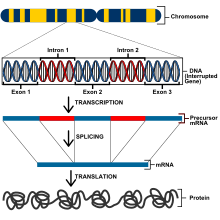
[ редактировать ]Эукариоты имеют гораздо больший геном и, следовательно, имеют другие методы регуляции генов, чем у прокариот. Все клетки эукариотического организма имеют одинаковую ДНК, но определяются посредством дифференциальной экспрессии генов — феномен, известный как генетическая тотипотентность . [7] Однако для того, чтобы клетка экспрессировала гены для правильного функционирования, гены должны тщательно регулироваться, чтобы проявлять правильные свойства. Гены у эукариот контролируются на транскрипционном , посттранскрипционном , трансляционном и посттрансляционном уровнях. [8] На уровне транскрипции экспрессия генов регулируется путем изменения скорости транскрипции. Гены, кодирующие белки, включают экзоны, которые будут кодировать полипептиды, интроны, которые удаляются из мРНК перед трансляцией белков, сайт начала транскрипции, с которым связывается РНК-полимераза, и промотор. [9]
Репрессии против ящика ТАТА
[ редактировать ]Гены эукариот содержат верхний промотор и основной промотор, также называемый базальным промотором. Распространенным базальным промотором является последовательность TATAAAAAAA, известная как ТАТА-бокс . ТАТА-бокс представляет собой комплекс с несколькими различными белками, включая фактор транскрипции II D (TFIID), который включает ТАТА-связывающий белок (TBP), который связывается с ТАТА-боксом, а также 13 других белков, связывающихся с ТБФ. Белки, связывающие ТАТА-бокс, также включают фактор транскрипции II B (TFIIB), который связывается как с ДНК-, так и с РНК-полимеразами. [9]
Сайленсеры у эукариот контролируют экспрессию генов на уровне транскрипции , на котором мРНК не транскрибируется. Эти последовательности ДНК могут действовать как сайленсеры или энхансеры на основе фактора транскрипции, который связывается с последовательностью, и связывание этой последовательности будет предотвращать связывание промоторов, таких как ТАТА-бокс, с РНК-полимеразой. [7] Белок-репрессор может иметь области, которые связываются с последовательностью ДНК, а также области, которые связываются с факторами транскрипции, собранными на промоторе гена, что создает механизм образования петель хромосомы. [9] Зацикливание приближает сайленсеры к промоторам, чтобы гарантировать совместную работу групп белков, необходимых для оптимальной экспрессии генов.

Мутировавшие глушители, наследственные заболевания и их последствия
[ редактировать ]Генетические мутации возникают, когда изменяются нуклеотидные последовательности в организме. Эти мутации приводят не только к заметным фенотипическим влияниям на человека, но и к изменениям, которые фенотипически не обнаруживаются. Источниками этих мутаций могут быть ошибки при репликации, спонтанные мутации, а также химические и физические мутагены ( УФ и ионизирующее излучение , тепло). [10] Сайленсеры, закодированные в геноме, подвержены таким изменениям, которые во многих случаях могут привести к тяжелым фенотипическим и функциональным нарушениям. В общих чертах, мутации в элементах или регионах сайленсера могут привести либо к ингибированию действия сайленсера, либо к стойкой репрессии необходимого гена. Затем это может привести к проявлению или подавлению нежелательного фенотипа, который может повлиять на нормальное функционирование определенных систем организма. Среди многих элементов и белков-сайлентеров REST/NSRF является важным фактором-сайлентером, который оказывает разнообразное влияние не только на нейронные аспекты развития. Фактически, во многих случаях REST/NSRF действует совместно с RE-1/NRSE, подавляя и влияя на ненейрональные клетки. [11] Его воздействие варьируется от лягушек ( Xenopus laevis ) до человека, с многочисленными эффектами на фенотип, а также на развитие. У Xenopus laevis нарушение или повреждение REST/NRSF связано с аномальным формированием эктодермального паттерна во время развития и значительными последствиями для нервной трубки, краниальных ганглиев и развития глаз. [12] У людей дефицит элемента-сайленсера REST/NSRF коррелирует с болезнью Хантингтона из-за снижения транскрипции BDNF .
Кроме того, текущие исследования показывают, что NRSE участвует в регуляции гена ANP, чрезмерная экспрессия которого может привести к гипертрофии желудочков . [13] Мутации в комплексах Polycomb-группы (PcG) также приводят к значительным изменениям в физиологических системах организмов. Следовательно, модификация элементов и последовательностей глушителей может привести либо к разрушительным, либо к незаметным изменениям.
REST/NRSF у Xenopus laevis
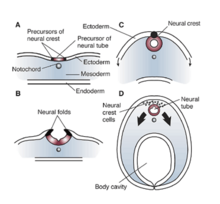
[ редактировать ]Эффекты и влияния RE1/NRSE и REST/NRSF значительны в ненейрональных клетках, которым требуется репрессия или подавление нейрональных генов. Эти элементы-глушители также регулируют экспрессию генов, которые не индуцируют нейрон-специфические белки, и исследования показали, что эти факторы оказывают обширное влияние на клеточные процессы. У Xenopus laevis дисфункция или мутация RE1/NRSE и REST/NRSF продемонстрировали значительное влияние на нервную трубку , краниальные ганглии и развитие глаз. [12] Все эти изменения можно объяснить неправильным формированием рисунка эктодермы во время развития Xenopus. Таким образом, мутация или изменение либо в области молчания RE1/NRSE, либо в сайленсере факторе REST/NRSF может нарушить правильную дифференцировку и спецификацию нейроэпителиального домена, а также препятствовать образованию кожи или эктодермы. [12] Отсутствие этих факторов приводит к снижению выработки костного морфогенетического белка (BMP), что приводит к недостаточному развитию нервного гребня . [12] Следовательно, эффекты NRSE и NRSF имеют фундаментальное значение для нейрогенеза развивающегося эмбриона, а также на ранних стадиях формирования эктодермального паттерна. В конечном счете, неадекватное функционирование этих факторов может привести к аберрантному развитию нервной трубки, краниальных ганглиев и развитию глаз у Xenopus .
REST/NSRF и болезнь Хантингтона
[ редактировать ]Болезнь Хантингтона (БГ) — наследственное нейродегенеративное заболевание, симптомы которого появляются в середине взрослой жизни человека. Наиболее заметными симптомами этого прогрессирующего заболевания являются когнитивные и двигательные нарушения, а также изменения в поведении. [14] Эти нарушения могут перерасти в деменцию , хорею и, в конечном итоге, в смерть. На молекулярном уровне БХ возникает в результате мутации белка хантингтина (Htt). Точнее, происходит аномальное повторение последовательности CAG по направлению к 5'-концу гена, что затем приводит к развитию токсичного полиглутаминового (polyQ) участка белка. Мутировавший белок Htt влияет на собственные нервные функции человека, ингибируя действие REST/NRSF.
REST/NRSF является важным элементом-сайлентером, который связывается с регуляторными областями и контролирует экспрессию определенных белков, участвующих в нервных функциях. Механистическое действие хантингтина до сих пор полностью не изучено, но при развитии БГ существует корреляция между Htt и REST/NRSF. Присоединяясь к REST/NRSF, мутантный белок хантингтин ингибирует действие сайленсера и удерживает его в цитозоле. Таким образом, REST/NRSF не может проникнуть в ядро и связаться с регуляторным элементом RE-1/NRSE из 21 пары оснований. Адекватная репрессия конкретных генов-мишеней имеет фундаментальное значение, поскольку многие из них участвуют в правильном развитии нейрональных рецепторов, нейротрансмиттеров , белков синаптических везикул и белков каналов. Дефицит правильного развития этих белков может вызвать нервные дисфункции, наблюдаемые при болезни Хантингтона. Помимо отсутствия репрессии из-за неактивности REST/NRSF, мутировавший белок хантингтин также может снижать транскрипцию Ген нейротропного фактора головного мозга (BDNF). BDNF влияет на выживание и развитие нейронов центральной нервной системы, а также периферической нервной системы. Эта аномальная репрессия происходит, когда область RE1/NRSE в области промотора BDNF активируется связыванием REST/NRSF, что приводит к отсутствию транскрипции гена BDNF. [15] Следовательно, аномальная репрессия белка BDNF предполагает значительное влияние на болезнь Хантингтона.
Текущие исследования REST/NRSF и гипертрофии желудочков у млекопитающих
[ редактировать ]REST/NRSF в сочетании с RE1/NRSE также действуют вне нервной системы как регуляторы и репрессоры. Текущие исследования связали активность RE1/NRSE с регуляцией экспрессии гена предсердного натрийуретического пептида ( ANP ). [13] Регуляторная область NRSE присутствует в 3'-нетранслируемой области гена ANP и действует как медиатор для его соответствующей экспрессии. Белок, кодируемый геном ANP , важен во время эмбрионального развития для созревания и развития кардиомиоцитов . Однако в раннем детстве и на протяжении всей взрослой жизни экспрессия ANP в желудочке подавляется или сводится к минимуму. Таким образом, аномальная индукция гена ANP может привести к гипертрофии желудочков и тяжелым сердечным последствиям. Чтобы поддерживать репрессию гена, NRSF (нейрон-рестриктивный сайленсер фактор) или REST связывается с областью NRSE в 3'-нетранслируемой области гена ANP . Кроме того, комплекс NRSF-NRSE рекрутирует транскрипционный корепрессор, известный как mSin3. [13] Это приводит к активности деацетилазы гистонов в этом регионе и репрессии гена. Таким образом, исследования выявили корреляцию между REST/NRSF и RE1/NRSE в регуляции экспрессии гена ANP в миоцитах желудочков. Мутация либо в NRSF, либо в NRSE может привести к нежелательному развитию желудочковых миоцитов из-за отсутствия репрессии, что затем может вызвать гипертрофию желудочков. Например, гипертрофия левого желудочка увеличивает вероятность внезапной смерти человека из-за желудочковой аритмии, возникающей в результате увеличения массы желудочка. [16] Помимо влияния на ген ANP , последовательность NRSE регулирует и другие кардиальные эмбриональные гены, такие как мозговой натрийуретический пептид BNP, скелетный α-актин и α3-субъединицу Na,K – АТФазы. [13] Следовательно, регуляторная активность как NRSE, так и NRSF у млекопитающих предотвращает не только нервные дисфункции, но также физиологические и фенотипические аномалии в других ненейрональных областях тела.

Мутации в элементах ответа полисотовой группы (PRE)
[ редактировать ]Регуляторные комплексы группы Polycomb (PcG) известны своим влиянием на эпигенетическую регуляцию стволовых клеток.особенно в гемопоэтических стволовых клетках. Репрессивный комплекс Polycomb 1 (PRC 1) непосредственно участвует в процессе кроветворения и функционирует совместно, например, с геном PcG « Bmi1 ». Исследования на мышах показывают, что организмы с мутированным «Bmi1» демонстрируют недостаточное функционирование митохондрий, а также препятствуют способности гемопоэтических клеток к самообновлению. Аналогично, мутации в генах PRC2 были связаны с гематологическими заболеваниями, такими как острый лимфобластный лейкоз (ОЛЛ), который является формой лейкемии. Следовательно, гены и белки группы Polycomb участвуют в правильном поддержании кроветворения в организме. [17]
Ссылки
[ редактировать ]- ^ Панг Б., ван Верд Дж. Х., Хамоен Флорида, член парламента Снайдера. «Идентификация некодирующих элементов-сайленсеров и их регуляция экспрессии генов». Nature Reviews Молекулярно-клеточная биология (2022) https://doi.org/10.1038/s41580-022-00549-9
- ^ Джаявелу Н.Д., Джаджодиа А., Мишра А., Хокинс Р.Д. «Кандидатные элементы-глушители для геномов человека и мыши». Природные коммуникации 11:1061 (2020) https://doi.org/10.1038/s41467-020-14853-5
- ^ Панг, Б., Снайдер, член парламента «Систематическая идентификация глушителей в клетках человека». Нат Жене 52, 254–263 (2020). https://doi.org/10.1038/s41588-020-0578-5
- ^ Jump up to: а б с д и ж Мастон, Гленн; Сара Эванс; Майкл Грин (23 мая 2006 г.). «Элементы регуляции транскрипции в геноме человека» (PDF) . Ежегодный обзор геномики и генетики человека . 7 : 29–59. дои : 10.1146/annurev.genom.7.080505.115623 . ПМИД 16719718 . Проверено 2 апреля 2013 г.
- ^ Jump up to: а б с д и ж г Огборн, Стивен; Тони Анталис (1998). «Транскрипционный контроль и роль сайленсеров в регуляции транскрипции у эукариот» . Биохим. Дж . 331 (1): 1–14. дои : 10.1042/bj3310001 . ПМЦ 1219314 . ПМИД 9512455 .
- ^ Jump up to: а б «Контроль генетических систем у прокариот и эукариот» . Университет Иллинойса в Чикаго . Проверено 2 апреля 2013 г.
- ^ Jump up to: а б «Контроль эукариотических генов» . Кеньонский колледж . Проверено 1 апреля 2013 г.
- ^ «Регуляция генов у эукариот» . Университет Восточного Мичигана . Проверено 7 апреля 2013 г.
- ^ Jump up to: а б с «Регуляция генов у эукариот» . Страницы биологии Кимбалла . Проверено 7 апреля 2013 г.
- ^ Браун, Т.А. (2002). «Мутация, репарация и рекомбинация». Геномы . Оксфорд: Вили-Лисс.
- ^ Шенгерр, CJ; Андерсон DJ (3 марта 1995 г.). «Нейрон-рестриктивный сайленсер-фактор (NRSF): координатный репрессор множества нейрон-специфичных генов». Наука . 267 (5202): 1360–3. Бибкод : 1995Sci...267.1360S . дои : 10.1126/science.7871435 . ПМИД 7871435 . S2CID 25101475 .
- ^ Jump up to: а б с д Ольгин, Патрисио; Пабло Отейса; Эдуардо Гамбоа; Хосе Луис Гомес-Скармета; Мануэль Кукулян (8 марта 2006 г.). «RE-1 Глушитель транскрипции/нейронрестриктивный глушитель модулирует эктодермальный паттерн во время развития Xenopus» (PDF) . Журнал неврологии . 26 (10): 2820–2829. doi : 10.1523/JNEUROSCI.5037-05.2006 . ПМК 6675167 . ПМИД 16525062 . Проверено 3 апреля 2013 г.
- ^ Jump up to: а б с д Кувахара, Коитиро; Ёсихико Сайто; Эмико Огава; Нобуки Такахаси; Ясуаки Накагава; Ёсихиса Нарусэ; Масаки Харада; Ичиро Хаманака; Такэхико Идзуми; Ёсихиро Миямото; Ичиро Кишимото; Рика Каваками; Мичио Наканиси; Нозому Мори; Кадзува Накао (21 марта 2001 г.). «Нейрон-рестриктивный глушитель - система нейрон-рестриктивных глушителей регулирует базальную и эндотелин-1-индуцируемую экспрессию генов предсердного натрийуретического пептида в миоцитах желудочков» . Молекулярная и клеточная биология . 21 (6): 2085–97. дои : 10.1128/MCB.21.6.2085-2097.2001 . ПМК 86819 . ПМИД 11238943 .
- ^ Уокер, Ф.О. (20 января 2007 г.). «Болезнь Хантингтона». Ланцет . 369 (9557): 218–28. дои : 10.1016/S0140-6736(07)60111-1 . ПМИД 17240289 . S2CID 46151626 .
- ^ Зуккато, К; Беляев Н; Конфорти П; Оой Л; Тартари М; Пападиму Э; Макдональд М; Фоссейл Э; Цейтлин С; Бакли Н; Каттанео Э. (27 июня 2007 г.). «Широко распространенное нарушение присутствия репрессорного элемента-1, подавляющего фактор транскрипции/нейрон-рестриктивного сайленсера, в генах-мишенях при болезни Хантингтона» . Журнал неврологии . 27 (26): 6972–6983. doi : 10.1523/JNEUROSCI.4278-06.2007 . ПМК 6672230 . ПМИД 17596446 . Проверено 21 марта 2013 г.
- ^ Риалс, Сет; Ин Ву; Нэнси Форд; Феррел Дж. Паулетто; Сандра В. Абрамсон; Эндрю М. Рубин; Роджер А. Маринчак; Питер Р. Коуи (1995). «Влияние гипертрофии левого желудочка и ее регрессии на электрофизиологию желудочков и уязвимость к индуцируемой аритмии в сердце кошек» . Тираж . 91 (2): 426–430. дои : 10.1161/01.cir.91.2.426 . ПМИД 7805247 . Проверено 3 апреля 2013 г.
- ^ Сашида, Горо; Ивама, Ацуши (2012). «Эпигенетическая регуляция кроветворения» . Международный журнал гематологии . 96 (4): 405–412. дои : 10.1007/s12185-012-1183-x . ПМИД 23054647 .
Внешние ссылки
[ редактировать ]- Silencer + Elements в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)