Запертая нуклеиновая кислота
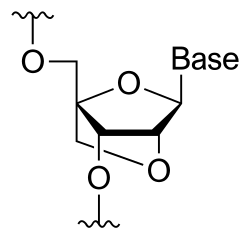
Запертая нуклеиновая кислота ( LNA ), также известная как мостиковая нуклеиновая кислота (BNA), [1] и часто называемый недоступной РНК , представляет собой модифицированный РНК нуклеотид , в котором рибоза модифицирована дополнительным мостиком, соединяющим 2'-кислород и 4'-углерод. Мостик «запирает» рибозу в 3'- эндо (Норт) конформации, которая часто встречается в дуплексах А-формы . Эта структура обеспечивает повышенную стабильность против ферментативной деградации. [2] [3] [4] [5] LNA также обеспечивает улучшенную специфичность и сродство при спаривании оснований в качестве мономера или компонента олигонуклеотида. [6] Нуклеотиды LNA могут быть смешаны с остатками ДНК или РНК в олигонуклеотиде.
Синтез
[ редактировать ]Обика и др. были первыми, кто химически синтезировал LNA в 1997 году, [7] независимо, за которым в 1998 году последовала группа Йеспера Венгеля. [8] Это стало возможным после того, как в 1978 году Замечник и Стивенсон заложили основу возможности того, что олигонуклеотиды могут быть отличными агентами для контроля экспрессии генов. [9] На сегодняшний день было показано, что два разных подхода, называемые соответственно линейной и конвергентной стратегией, позволяют создавать высокодоходные и эффективные LNA. Линейная стратегия синтеза впервые была подробно описана в работах Обики с соавт. [7] В этом подходе уридин (или любой легкодоступный нуклеозид в качестве исходного материала можно использовать РНК). Конвергентная стратегия требует синтеза промежуточного сахарного продукта, который служит донором гликозила, необходимым для связывания с нуклеиновыми основаниями . Обычно D-глюкоза используется для получения промежуточного сахарного продукта, который впоследствии вступает в реакцию с азотистыми основаниями с использованием модифицированной процедуры Форбрюгена, позволяющей осуществлять стереоселективное связывание. [10]
Добавление различных фрагментов остается возможным при сохранении ключевых физико-химических свойств, таких как высокое сродство и специфичность, очевидные для первоначально синтезированного LNA. [8] Такие олигомеры синтезируются химическим путем и коммерчески доступны.
Включение в ДНК/РНК
[ редактировать ]LNA может быть включен в ДНК и РНК с помощью различных ДНК- и РНК-полимераз. ДНК-полимераза Phusion, коммерчески разработанный фермент на основе ДНК-полимеразы Pfu , эффективно включает LNA в ДНК. [11]
Характеристики
[ редактировать ]LNA обеспечивает повышенную биостабильность по сравнению с биологическими нуклеиновыми кислотами . LNA-модифицированные олигонуклеотиды продемонстрировали улучшенную термодинамику при гибридизации с РНК , оцДНК и дцДНК . [11]
Приложения
[ редактировать ]LNAзимы
[ редактировать ]ДНКзимы могут быть модифицированы путем включения остатков LNA, образуя LNAзимы (LNA-модифицированные ДНКзимы). Эти модифицированные олигонуклеотиды, как и их родственники ДНКзимов, обычно представляют собой эндонуклеазы , которые связываются со специфическими целевыми последовательностями РНК и расщепляют фосфодиэфирную связь , существующую между нуклеотидами. [12] Однако они демонстрируют более эффективное расщепление фосфодиэфирных связей по сравнению со своими немодифицированными аналогами. [13] Модификация плеч ДНКзимов, LNA распознающих субстраты, мономерами дает LNAзим, который узнает вирус Коксаки A21 (CAV-21) и расщепляет его целевую последовательность РНК, аналогичную той, что находится в 5'-нетранслируемой области (5'-UTR) человеческого риновируса -14 ( ВСР-14); последовательность, нераспознаваемая немодифицированными ДНКзимами. [14]
Терапия
[ редактировать ]Использование олигонуклеотидов на основе LNA в терапевтических целях является новой областью биотехнологии . [15] Различные олигонуклеотиды LNA были оценены на предмет их фармакокинетических профилей и токсичности. Исследования пришли к выводу, что токсичность LNA, как правило, не зависит от последовательности олигонуклеотидов и демонстрирует предпочтительный профиль безопасности для переводимых терапевтических применений. [8]
LNA исследовали на предмет его терапевтических свойств при лечении рака и инфекционных заболеваний. Антисмысловая молекула фосфоротиоата заблокированной нуклеиновой кислоты, названная SPC2996, была разработана для воздействия на мРНК , кодирующую онкопротеин Bcl-2, белок, который ингибирует апоптоз в клетках хронического лимфоцитарного лейкоза (ХЛЛ). Клинические испытания фазы I и II продемонстрировали дозозависимое снижение количества циркулирующих клеток ХЛЛ примерно у 30% выборки, что предполагает дальнейшее исследование SPC2996. [16]
LNA также была применена к Миравирсену , экспериментальному терапевтическому средству, предназначенному для лечения гепатита С , представляющему собой 15-нуклеотидную фосфоротиоатную последовательность со специфичностью связывания с МиР-122 ( миРНК, экспрессируемая в гепатоцитах ). [17] [18]
Обнаружение и диагностика
[ редактировать ]Аллель-специфическая ПЦР с использованием LNA позволяет создавать более короткие праймеры без ущерба для специфичности связывания. [19]
LNA был включен во флуоресцентную гибридизацию in situ (FISH) . [20] FISH — это распространенный метод, используемый для визуализации генетического материала в различных клетках, но исследования показали, что этот метод ограничен низкой эффективностью гибридизации зондов. И наоборот, зонды, содержащие LNA, продемонстрировали повышенную эффективность гибридизации как в ДНК , так и в РНК . Повышенная эффективность FISH с включением LNA привела к FISH-анализу человеческой хромосомы, нескольких типов нечеловеческих клеток и микрочипов. [20]
Также были проведены анализы генотипирования LNA, в частности, для обнаружения мутации в аполипопротеине B. [20]
Из-за своей высокой способности к распознаванию несовпадений LNA изучался на предмет его применения в диагностических инструментах. Иммобилизованные зонды LNA были использованы в мультиплексном анализе генотипирования SNP . [15]
Редактирование генов
[ редактировать ]LNA-модифицированные ssODN (синтетические одноцепочечные ДНК-олигонуклеотиды) можно использовать, как и обычные ssODN, для одноосновного редактирования генов. Использование LNA в предполагаемом месте модификации или рядом с ним позволяет избежать восстановления несоответствия ДНК из-за более высокой термодинамической стабильности, которую он имеет. [21]
Ссылки
[ редактировать ]- ^ Элаяди, Анисса Н.; Брааш, Дуэйн А.; Кори, Дэвид Р. (август 2002 г.). «Последствия высокоаффинной гибридизации с помощью олигомеров заблокированных нуклеиновых кислот для ингибирования теломеразы человека †» . Биохимия . 41 (31): 9973–9981. дои : 10.1021/bi025907j . ISSN 0006-2960 . ПМИД 12146961 .
- ^ Куррек, Дж. (1 мая 2002 г.). «Дизайн антисмысловых олигонуклеотидов, стабилизированных заблокированными нуклеиновыми кислотами» . Исследования нуклеиновых кислот . 30 (9): 1911–1918. дои : 10.1093/нар/30.9.1911 . ПМЦ 113840 . ПМИД 11972327 .
- ^ Фриден, М. (1 ноября 2003 г.). «Расширение горизонта проектирования антисмысловых олигонуклеотидов с помощью альфа-L-LNA» . Исследования нуклеиновых кислот . 31 (21): 6365–6372. дои : 10.1093/нар/gkg820 . ISSN 1362-4962 . ПМК 275462 . PMID 14576324 .
- ^ Фриден, Мириам; Хансен, Хенрик Ф.; Кох, Троэльс (октябрь 2003 г.). «Нуклеазная стабильность LNA-олигонуклеотидов и LNA-ДНК-химер» . Нуклеозиды, нуклеотиды и нуклеиновые кислоты . 22 (5–8): 1041–1043. дои : 10.1081/NCN-120022731 . ISSN 1525-7770 . ПМИД 14565339 . S2CID 10631717 .
- ^ Морита, К.; Хасэгава, К.; Канеко, М.; Цуцуми, С.; Соне, Дж.; Исикава, Т.; Иманиши, Т.; Коидзуми, М. (1 ноября 2001 г.). «2'-O, 4'-C-этиленовые нуклеиновые кислоты (ENA) с устойчивостью к нуклеазам и высоким сродством к РНК» . Серия симпозиумов по нуклеиновым кислотам . 1 (1): 241–242. дои : 10.1093/насс/1.1.241 . ISSN 0261-3166 . ПМИД 12836354 .
- ^ Виду, Ракеш; Венгель, Йеспер (2011). Медицинская химия нуклеиновых кислот . John Wiley & Sons, Inc., стр. 335–337. ISBN 978-0470596685 .
- ^ Jump up to: а б Обика, Сатоши; Нанбу, Дайшу; Хари, Ёсиюки; Морио, Кен-итиро; Ин, Ясуко; Исида, Тосимаса; Иманиши, Такеши (15 декабря 1997 г.). «Синтез 2'-O,4'-C-метиленуридина и -цитидина. Новые бициклические нуклеозиды, имеющие фиксированное сморщивание C3, -эндо-сахара» . Буквы тетраэдра . 38 (50): 8735–8738. дои : 10.1016/S0040-4039(97)10322-7 . ISSN 0040-4039 .
- ^ Jump up to: а б с Орум, Мириам Фриден и Хенрик (31 марта 2008 г.). «Запертая нуклеиновая кислота перспективна в лечении рака» . Текущий фармацевтический дизайн . 14 (11): 1138–1142. дои : 10.2174/138161208784246234 . ПМИД 18473860 . Проверено 6 октября 2020 г.
- ^ Замечник, ПК; Стивенсон, ML (1 января 1978 г.). «Ингибирование репликации вируса саркомы Рауса и трансформации клеток специфическим олигодезоксинуклеотидом» . Труды Национальной академии наук . 75 (1): 280–284. Бибкод : 1978PNAS...75..280Z . дои : 10.1073/pnas.75.1.280 . ISSN 0027-8424 . ПМК 411230 . ПМИД 75545 .
- ^ Кошкин, Алексей А.; Фенсхольдт, Джеф; Пфундхеллер, Хенрик М.; Ломхольт, Кристиан (1 декабря 2001 г.). «Упрощенный и эффективный путь получения 2'-O, 4'-C-метилен-связанных бициклических рибонуклеозидов (запертой нуклеиновой кислоты)» . Журнал органической химии . 66 (25): 8504–8512. дои : 10.1021/jo010732p . ISSN 0022-3263 . ПМИД 11735531 .
- ^ Jump up to: а б Виду, Ракеш Н.; Вестер, Бирте; Венгель, Йеспер (26 марта 2007 г.). «Ферментативное включение нуклеотидов LNA в цепи ДНК» . ХимБиоХим . 8 (5): 490–492. дои : 10.1002/cbic.200600501 . ПМИД 17315250 . S2CID 10206060 .
- ^ Брейкер, Р.Р.; Джойс, Г.Ф. (декабрь 1994 г.). «ДНК-фермент, расщепляющий РНК» . Химия и биология . 1 (4): 223–229. дои : 10.1016/1074-5521(94)90014-0 . ISSN 1074-5521 . ПМИД 9383394 .
- ^ Вестер, Бирте; Лундберг, Ларс Бо; Соренсен, Мадс Д.; Бабу, Б. Равиндра; Даутвейт, Стивен; Венгель, Йеспер (ноябрь 2002 г.). «LNAзимы: включение мономеров LNA-типа в ДНКзимы заметно увеличивает расщепление РНК» . Журнал Американского химического общества . 124 (46): 13682–13683. дои : 10.1021/ja0276220 . ISSN 0002-7863 . ПМИД 12431091 .
- ^ Шуберт, Штеффен; Фюрсте, Йенс П; Работай, Дениз; Грюнерт, Ганс Петер; Цайххардт, Хайнц; Эрдманн, Фолькер А; Куррек, Йенс (май 2004 г.). «Получение целевого доступа к дезоксирибозимам». Журнал молекулярной биологии . 339 (2): 355–363. дои : 10.1016/j.jmb.2004.03.064 . ПМИД 15136038 .
- ^ Jump up to: а б Петерсен М., Венгель Дж. (февраль 2003 г.). «LNA: универсальный инструмент для терапии и геномики». Тенденции в биотехнологии . 21 (2): 74–81. дои : 10.1016/S0167-7799(02)00038-0 . ПМИД 12573856 .
- ^ Дюриг, Дж.; Дюрсен, У.; Кляйн-Хитпасс, Л.; Ворм, Дж.; Хансен, Дж. Б. Роде; Орум, Х.; Виссенбах, М. (апрель 2011 г.). «Новый антисмысловой ингибитор Bcl-2 SPC2996 вызывает быстрое выведение лейкозных клеток и иммунную активацию при хроническом лимфоцитарном лейкозе». Лейкемия . 25 (4): 638–647. дои : 10.1038/leu.2010.322 . ISSN 1476-5551 . ПМИД 21358717 .
- ^ Геберт, Лука ФР; Ребхан, Марио А.Е.; Кривелли, Сильвия EM; Дензлер, Реми; Стоффель, Маркус; Холл, Джонатан (1 января 2014 г.). «Миравирсен (SPC3649) может ингибировать биогенез миР-122» . Исследования нуклеиновых кислот . 42 (1): 609–621. дои : 10.1093/нар/gkt852 . ISSN 0305-1048 . ПМЦ 3874169 . ПМИД 24068553 .
- ^ Бонно, Э.; Невё, Б.; Константин Е.; Цонгалис, Г.Дж.; Де Гуайр, В. (24 июня 2019 г.). «Насколько микроРНК близки к клинической практике? Взгляд на диагностический и терапевтический рынок» . EJIFCC . 30 (2): 114–127. ISSN 1650-3414 . ПМК 6599191 . ПМИД 31263388 .
- ^ Бонетта Л (2005). «Прайм-тайм для ПЦР в реальном времени» . Нат. Методы . 2 (4): 305–312. дои : 10.1038/nmeth0405-305 . S2CID 17711047 .
- ^ Jump up to: а б с Кубота, Кенго; Охаси, Акиёси; Имачи, Хироюки; Харада, Хидеки (август 2006 г.). «Повышение эффективности гибридизации in situ с помощью зондов ДНК, содержащих заблокированные нуклеиновые кислоты» . Прикладная и экологическая микробиология . 72 (8): 5311–5317. дои : 10.1128/АЕМ.03039-05 . ISSN 0099-2240 . ПМЦ 1538721 . ПМИД 16885281 .
- ^ ван Равестейн, ТВ; Деккер, М; Рыба, А; Сиксма, ТК; Уолтерс, А; Деккер, Р.Дж.; Те Риле, HP (12 апреля 2016 г.). «LNA-модификация одноцепочечных ДНК-олигонуклеотидов позволяет осуществлять тонкую модификацию генов в клетках, способных репарировать ошибочные спаривания» . Труды Национальной академии наук Соединенных Штатов Америки . 113 (15): 4122–7. дои : 10.1073/pnas.1513315113 . ПМЦ 4839440 . ПМИД 26951689 .