Энхансерная РНК
Энхансерные РНК (еРНК) представляют собой класс относительно длинных некодирующих молекул РНК (50–2000 нуклеотидов), транскрибируемых с последовательности ДНК энхансерных участков. Впервые они были обнаружены в 2010 году с помощью полногеномных методов, таких как RNA-seq и ChIP-seq . [1] [2] еРНК можно разделить на два основных класса: 1D-еРНК и 2D-еРНК, которые различаются в первую очередь размером, состоянием полиаденилирования и направленностью транскрипции. [3] Экспрессия данной эРНК коррелирует с активностью ее соответствующего энхансера в генах-мишенях. [4] Все больше данных свидетельствует о том, что eRNAs активно играют роль в регуляции транскрипции в цис и транс , и хотя механизмы их действия остаются неясными, было предложено несколько моделей. [3]
Открытие
[ редактировать ]Энхансеры как сайты внегенной транскрипции были первоначально обнаружены в полногеномных исследованиях, которые идентифицировали энхансеры как общие области связывания РНК-полимеразы II (RNA pol II) и некодирующей РНК транскрипции . [1] [2] Было обнаружено, что уровень взаимодействия РНК pol II с энхансером и образование транскрипта РНК сильно различаются в этих первоначальных исследованиях. Используя явные пики сигнатур хроматина , было обнаружено, что значительная часть (~ 70%) сайтов начала транскрипции экстрагенной РНК Pol II перекрывает энхансеров сайты в мышиных макрофагах . [5] Было обнаружено, что из 12 000 нейрональных энхансеров в мыши геноме почти 25% сайтов связывают РНК Pol II и генерируют транскрипты . [6] В параллельных исследованиях 4588 сайтов связывания экстрагенной РНК Pol II с высокой степенью достоверности были идентифицированы в мышиных макрофагах, стимулированных липополисахаридом- медиатором воспаления для индукции транскрипции. [2] Эти эРНК, в отличие от информационных РНК (мРНК), не подвергались модификациям путем полиаденилирования , обычно были короткими, некодирующими и транскрибировались в двух направлениях. Более поздние исследования выявили транскрипцию другого типа эРНК, генерируемую посредством однонаправленной транскрипции, которые были длиннее и содержали поли-А-хвост . [7] Более того, уровни эРНК коррелировали с уровнями мРНК близлежащих генов , что указывает на потенциальную регуляторную и функциональную роль этих некодирующих энхансерной РНК молекул . [1]
Биогенез
[ редактировать ]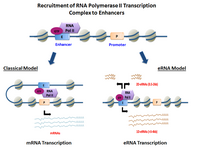
Краткое содержание
[ редактировать ]еРНК транскрибируются с ДНК выше и ниже экстрагенных последовательностей энхансерных областей. [8] Ранее несколько модельных энхансеров продемонстрировали способность напрямую рекрутировать РНК Pol II и общие факторы транскрипции преинициативный комплекс (PIC) до места начала транскрипции на промоторе генов и формировать . В определенных клеток типах активированные энхансеры продемонстрировали способность как рекрутировать РНК Pol II , так и обеспечивать матрицу для активной транскрипции их локальных последовательностей . [2] [1]
В зависимости от направленности транскрипции энхансерные транскриптов области генерируют два разных типа некодирующих . : 1D-еРНК и 2D-еРНК Природа преинициаторного комплекса и специфические факторы транскрипции , рекрутированные в энхансер, могут контролировать тип генерируемых eRNA. После транскрипции большинство эРНК остается в ядре . [9] В целом эРНК очень нестабильны и активно разрушаются ядерной экзосомой . Не все энхансеры транскрибируются: количество нетранскрибируемых энхансеров значительно превышает количество транскрибируемых, порядка десятков тысяч в каждом данном типе клеток . [5]
1D эРНК
[ редактировать ]В большинстве случаев однонаправленная транскрипция энхансерных областей приводит к образованию длинных (>4 т.п.н.) и полиаденилированных эРНК. Энхансеры , которые генерируют полиА+ эРНК, имеют более низкое соотношение H3K4me1 /me3 в своей сигнатуре хроматина , чем 2D-еРНК. [7] ПолиА+ эРНК отличаются от длинных мультиэкзонных политранскриптов (мРНК), которые генерируются путем инициации транскрипции внутригенными энхансерами . Эти длинные некодирующие РНК, которые точно отражают структуру гена хозяина , за исключением альтернативного первого экзона , демонстрируют плохой кодирующий потенциал. [10] В результате полиА+ 1D-еРНК могут представлять собой смешанную группу истинных энхансерных РНК и мультиэкзонных РНК.
2D эРНК
[ редактировать ]Двунаправленная транскрипция на сайтах энхансеров генерирует сравнительно более короткие (0,5-2 т.п.н.) и неполиаденилированные эРНК. Энхансеры , которые генерируют полиА-еРНК, имеют характер хроматина с более высоким соотношением H3K4me1/me3, чем 1D-еРНК. В целом, энхансера транскрипция и продукция двунаправленных эРНК демонстрируют сильную корреляцию активности энхансера с транскрипцией генов . [11]
Частота и время экспрессии эРНК
[ редактировать ]Арнер и др. [12] идентифицировали 65 423 транскрибируемых энхансера (продуцирующих эРНК) среди 33 различных типов клеток в разных условиях и в разное время стимуляции. Транскрипция энхансеров обычно предшествует транскрипции транскрипционных факторов , которые, в свою очередь, обычно предшествуют информационной РНК транскрипции генов (мРНК).
Карулло и др. [13] исследовали один конкретный тип клеток, нейроны (из первичных культур нейронов). Они обнаружили 28 492 предполагаемых энхансера, генерирующих эРНК. Эти эРНК часто транскрибировались с обеих цепей ДНК-энхансера в противоположных направлениях. Карулло и др. [13] использовали эти культивированные нейроны, чтобы изучить время появления специфических энхансерных эРНК по сравнению с мРНК их целевых генов. Культивированные нейроны активировали и из этих нейронов выделяли РНК через 0, 3,75, 5, 7,5, 15, 30 и 60 минут после активации. В этих экспериментальных условиях они обнаружили, что 2 из 5 энхансеров немедленного раннего гена (IEG) FOS , то есть энхансер FOS 1 и энхансер FOS 3, активировались и инициировали транскрипцию своих eRNA (eRNA1 и eRNA3). Уровень экспрессии eRNA1 и eRNA3 FOS значительно повышался в течение 7,5 минут, тогда как уровень мРНК FOS повышался только через 15 минут после стимуляции. Сходные закономерности наблюдались у IEGs FOSb и NR4A1 , что указывает на то, что для многих IEG индукция eRNA предшествует индукции мРНК в ответ на активацию нейронов.
Хотя некоторые энхансеры могут активировать свои целевые промоторы в своих целевых генах без транскрипции эРНК, большинство активных энхансеров транскрибируют эРНК во время активации своих целевых промоторов. [14]
Функции эРНК, обнаруженные в период с 2013 по 2021 год
[ редактировать ]Описанные ниже функции эРНК были описаны в различных биологических системах, часто демонстрируемых с помощью небольшого количества специфических пар генов-энхансеров-мишеней. Неясно, в какой степени описанные здесь функции eRNA могут быть обобщены на большинство eRNA.
эРНК в формировании петли
[ редактировать ]
Петли хромосомы, показанные на рисунке, подводящие энхансер к промотору его гена-мишени, могут быть направлены и сформированы эРНК, транскрибируемой с энхансера после активации энхансера.
Транскрибируемая энхансерная РНК (еРНК), взаимодействующая с комплексом белков-медиаторов (см. рисунок), особенно с субъединицей 12-медиатора ( MED12 ), по-видимому, играет важную роль в формировании петли хромосомы, которая приводит энхансер в тесную ассоциацию с промотором гена-мишени. энхансера в случае пяти генов, изученных Lai et al. [15] [16] [17] Хоу и Краус, [18] описать два других исследования, сообщающих о подобных результатах. Арнольд и др. [19] рассмотрим еще 5 случаев, когда эРНК активно участвует в формировании петли энхансер-промотор.
эРНК взаимодействуют с белками, влияя на транскрипцию
[ редактировать ]Одной из хорошо изученных эРНК является эРНК энхансера, который взаимодействует с промотором гена простатического специфического антигена (ПСА). [20] еРНК ПСА сильно регулируется андрогенным рецептором . В этом случае эРНК с высоким уровнем ПСА имеет эффект домино. РНК ПСА связывается с белковым комплексом положительного фактора элонгации транскрипции P-TEFb и активирует его , который затем может фосфорилировать РНК-полимеразу II (РНКП II), инициируя ее активность по производству мРНК . P-TEFb также может фосфорилировать фактор отрицательной элонгации NELF (который приостанавливает РНКП II в пределах 60 нуклеотидов после начала инициации мРНК). Фосфорилированный NELF высвобождается из RNAP II, что позволяет RNAP II осуществлять продуктивную прогрессию мРНК (см. Рисунок). Таким образом, повышенная регуляция эРНК ПСА увеличивает экспрессию 586 генов, чувствительных к андрогенным рецепторам. Нокдаун эРНК ПСА или удаление набора нуклеотидов из эРНК ПСА приводит к уменьшению присутствия фосфорилированной (активной) РНКП II в этих генах, что приводит к снижению их транскрипции.
Белок отрицательного фактора элонгации NELF также может высвобождаться в результате взаимодействия с РНКП II путем прямого взаимодействия с некоторыми эРНК. Шаукович и др. [21] показали, что eRNA двух непосредственных ранних генов (IEG) напрямую взаимодействовали с белком NELF, высвобождая NELF из RNAP II, приостановленного на промоторах этих двух генов, позволяя затем экспрессировать эти два гена.
Кроме того, эРНК, по-видимому, взаимодействуют с 30 другими белками. [19] [17] [18]
Предлагаемые механизмы функционирования до 2013 г.
[ редактировать ]
Представления о том, что не все энхансеры транскрибируются одновременно и что транскрипция eRNA коррелирует со специфичной для энхансера активностью, подтверждают идею о том, что отдельные eRNA несут различные и значимые биологические функции. [3] Однако до сих пор нет единого мнения о функциональном значении eRNA. Более того, эРНК могут легко разрушаться посредством экзосом и нонсенс-опосредованного распада , что ограничивает их потенциал в качестве важных регуляторов транскрипции. [22] На сегодняшний день предложены четыре основные модели функции эРНК: [3] каждое из них подкреплено различными экспериментальными данными .
Транскрипционный шум
[ редактировать ]Поскольку многочисленные исследования показали, что РНК Pol II можно обнаружить в очень большом количестве экстрагенных областей, возможно, что эРНК просто представляют собой продукт случайной «протекающей» транскрипции и не несут никакой функциональной значимости. [5] Неспецифическая активность РНК Pol II, следовательно, допускает появление экстрагенного транскрипционного шума в сайтах, где хроматин уже находится в открытом и транскрипционно компетентном состоянии. Это могло бы объяснить даже тканеспецифическую экспрессию эРНК. [23] поскольку открытые участки также тканеспецифичны.
Транскрипционно-зависимые эффекты
[ редактировать ]РНК Pol II, , опосредованная гена Транскрипция индуцирует локальное открытие состояния хроматина за счет привлечения гистон-ацетилтрансфераз и других модификаторов гистонов , которые способствуют образованию эухроматина . Было высказано предположение, что присутствие этих ферментов может также вызывать открытие хроматина в энхансерных областях, которые обычно присутствуют в отдаленных местах, но могут быть рекрутированы на целевые гены посредством закольцовывания ДНК . [24] Таким образом, в этой модели эРНК экспрессируются в ответ на транскрипцию РНК Pol II и, следовательно, не несут никакой биологической функции.
Функциональная активность в цис
[ редактировать ]Хотя две предыдущие модели предполагали, что eRNA не являются функционально значимыми, этот механизм утверждает, что eRNA являются функциональными молекулами , которые проявляют цис- активность. В этой модели эРНК могут локально рекрутировать регуляторные белки в своем собственном сайте синтеза. В поддержку этой гипотезы полагают, что транскрипты, происходящие от энхансеров выше гена Cyclin D1, служат адаптерами для рекрутирования гистон-ацетилтрансфераз . Было обнаружено, что истощение этих eRNA приводит к подавлению транскрипции Cyclin D1 . [9]
Функциональная активность в транс
[ редактировать ]Последняя модель включает регуляцию транскрипции с помощью eRNA в удаленных хромосомных местоположениях. Посредством дифференциального рекрутирования белковых комплексов eRNAs могут влиять на транскрипционную компетентность специфических локусов . Evf-2 представляет собой хороший пример такой трансрегуляторной эРНК, поскольку она может индуцировать экспрессию Dlx2, что, в свою очередь, может увеличивать активность энхансеров Dlx5 и Dlx6 . [25] Транс-действующие еРНК могут также работать в цис- и наоборот.
Экспериментальное обнаружение
[ редактировать ]Обнаружение эРНК появилось сравнительно недавно (2010 г.) и стало возможным благодаря использованию полногеномных методов исследования, таких как секвенирование РНК ( RNA-seq ) и иммунопреципитационное секвенирование хроматина ( ChIP-seq ). [1] RNA-seq позволяет напрямую идентифицировать эРНК путем сопоставления обнаруженного транскрипта с соответствующей последовательностью энхансера посредством биоинформатического анализа. [26] [4] ChIP-seq представляет собой менее прямой способ оценки энхансеров транскрипции , но также может предоставить важную информацию, поскольку определенные метки хроматина связаны с активными энхансерами . [27] Хотя некоторые данные остаются противоречивыми, в литературе сходятся во мнении, что лучшая комбинация посттрансляционных модификаций гистонов в активных энхансерах состоит из H2AZ , H3K27ac и высокого соотношения H3K4me1 по сравнению с H3K4me3 . [27] [28] [29] ChIP- эксперименты также можно проводить с антителами , распознающими РНК Pol II , которую можно обнаружить в местах активной транскрипции . [5] Экспериментальное обнаружение eRNA осложняется их низкой эндогенной стабильностью, обусловленной деградацией экзосом и нонсенс-опосредованным распадом . [22] Сравнительное исследование показало, что анализы, обогащенные кэпированными и возникающими РНК (с такими стратегиями, как продолжение ядер и выбор размера), могут улавливать больше эРНК по сравнению с каноническим секвенированием РНК . [30] Эти анализы включают глобальный/прецизионный анализ с отбором кэпа (GRO/PRO-cap), секвенирование кэпированных малых РНК (csRNA-seq), анализ экспрессии генов с использованием нативного удлиненного транскрипта (NET-CAGE) и прецизионный анализ. Секвенирование Run-On (PRO-seq). [31] Тем не менее, тот факт, что eRNAs имеют тенденцию экспрессироваться с помощью активных энхансеров, может сделать их обнаружение полезным инструментом для различения активных и неактивных энхансеров .
Влияние на развитие и болезни
[ редактировать ]Доказательства того, что eRNAs оказывают последующие эффекты на эффективность активации энхансеров и транскрипции генов, предполагают их функциональные возможности и потенциальную важность. энхансерные области и Было продемонстрировано, что фактор транскрипции p53 связывает генерирует эРНК p53 -зависимым образом. [32] При раке , р53 играет центральную роль в подавлении опухоли поскольку мутации этого гена появляются в 50% опухолей . [33] эти р53 -связанные энхансерные Показано, что области (p53BER) взаимодействуют с множеством локальных и дистальных генов- мишеней, участвующих в и выживании клеток пролиферации . Кроме того, показано, что эРНК, генерируемые в результате активации p53BER, необходимы для эффективной транскрипции генов p53 мишеней - , что указывает на, вероятно, важную регуляторную роль эРНК в подавлении опухолей и раке . В целом было показано, что мутации в эРНК демонстрируют сходное фенотипическое поведение при онкогенезе по сравнению с РНК, кодирующей белок. [34]
Вариации энхансеров связаны с заболеваниями человека , но терапевтический подход к управлению активностью энхансеров в настоящее время невозможен. С появлением еРНК в качестве важных компонентов энхансерной активности мощные терапевтические инструменты, такие как РНКи, могут обеспечить многообещающие пути целевого нарушения экспрессии генов.
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и Ким Т.К., Хемберг М., Грей Дж.М., Коста А.М., Беар Д.М., Ву Дж. и др. (май 2010 г.). «Распространенная транскрипция энхансеров, регулируемых активностью нейронов» . Природа . 465 (7295): 182–187. Бибкод : 2010Natur.465..182K . дои : 10.1038/nature09033 . ПМК 3020079 . ПМИД 20393465 .
- ^ Jump up to: а б с д Де Санта Ф., Бароцци И., Миеттон Ф., Гислетти С., Поллетти С., Туси Б.К. и др. (май 2010 г.). «Большая часть сайтов транскрипции экстрагенной РНК pol II перекрывает энхансеры» . ПЛОС Биология . 8 (5): e1000384. дои : 10.1371/journal.pbio.1000384 . ПМЦ 2867938 . ПМИД 20485488 .
- ^ Jump up to: а б с д Натоли Г, Андрау Дж. К. (2012). «Некодирующая транскрипция энхансеров: общие принципы и функциональные модели». Ежегодный обзор генетики . 46 : 1–19. doi : 10.1146/annurev-genet-110711-155459 . ПМИД 22905871 .
- ^ Jump up to: а б Беррен О.С., Рубио Гарсиа А., Хавьер Б.М., Рэйнбоу Д.Б., Кэрнс Дж., Купер Н.Дж. и др. (сентябрь 2017 г.). «Хромосомные контакты в активированных Т-клетках идентифицируют гены-кандидаты аутоиммунных заболеваний» . Геномная биология . 18 (1): 165. дои : 10.1186/s13059-017-1285-0 . ПМК 5584004 . ПМИД 28870212 .
- ^ Jump up to: а б с д Де Санта Ф, Бароцци И, Миеттон Ф, Гислетти С, Поллетти С, Туси БК и др. (май 2010 г.). Мэттик Дж.С. (ред.). «Большая часть сайтов транскрипции экстрагенной РНК pol II перекрывает энхансеры» . ПЛОС Биология . 8 (5): e1000384. дои : 10.1371/journal.pbio.1000384 . ПМЦ 2867938 . ПМИД 20485488 .
- ^ Хайнцман Н.Д., Стюарт Р.К., Хон Г., Фу Ю., Чинг К.В., Хокинс Р.Д. и др. (март 2007 г.). «Отличные и прогнозируемые хроматиновые сигнатуры промоторов и энхансеров транскрипции в геноме человека». Природная генетика . 39 (3): 311–318. дои : 10.1038/ng1966 . ПМИД 17277777 . S2CID 1595885 .
- ^ Jump up to: а б Кох Ф., Фенуил Р., Гут М., Коши П., Альберт Т.К., Закариас-Кабеса Дж. и др. (июль 2011 г.). «Платформы инициации транскрипции и рекрутирование GTF на тканеспецифичных энхансерах и промоторах». Структурная и молекулярная биология природы . 18 (8): 956–963. дои : 10.1038/nsmb.2085 . ПМИД 21765417 . S2CID 12778976 .
- ^ Федосеева Д.М., Кретова О.В., Чуриков Н.А. (2012). «Молекулярный анализ энхансерных РНК и модификаций хроматина в области их синтеза в клетках дрозофилы, обладающих генетическими конструкциями». Доклады. Биохимия и биофизика . 442 : 7–11. дои : 10.1134/S1607672912010012 . ПМИД 22419084 . S2CID 14304312 .
- ^ Jump up to: а б Ван Х, Араи С., Сонг Х, Райхарт Д., Ду К., Паскуаль Г. и др. (июль 2008 г.). «Индуцированные нкРНК аллостерически модифицируют РНК-связывающие белки в цис-дисплее, чтобы ингибировать транскрипцию» . Природа . 454 (7200): 126–130. Бибкод : 2008Natur.454..126W . дои : 10.1038/nature06992 . ПМЦ 2823488 . ПМИД 18509338 .
- ^ Ковальчик М.С., Хьюз Дж.Р., Гаррик Д., Линч М.Д., Шарп Дж.А., Слоан-Стэнли Дж.А. и др. (февраль 2012 г.). «Внутригенные энхансеры действуют как альтернативные промоторы» . Молекулярная клетка . 45 (4): 447–458. doi : 10.1016/j.molcel.2011.12.021 . hdl : 2318/97658 . ПМИД 22264824 .
- ^ Ван Д., Гарсиа-Бассет И., Беннер С., Ли В., Су Х, Чжоу Ю. и др. (май 2011 г.). «Перепрограммирование транскрипции с помощью различных классов энхансеров, функционально определяемых эРНК» . Природа . 474 (7351): 390–394. дои : 10.1038/nature10006 . ПМК 3117022 . ПМИД 21572438 .
- ^ Арнер Э., Дауб К.О., Виттинг-Серуп К., Андерссон Р., Лилье Б., Драблёс Ф. и др. (февраль 2015 г.). «Транскрибируемые энхансеры возглавляют волны скоординированной транскрипции в переходных клетках млекопитающих» . Наука . 347 (6225): 1010–1014. Бибкод : 2015Sci...347.1010A . дои : 10.1126/science.1259418 . ПМЦ 4681433 . ПМИД 25678556 .
- ^ Jump up to: а б Карулло Н.В., Филлипс III Р.А., Саймон Р.К., Сото С.А., Хиндс Дж.Э., Солсбери А.Дж. и др. (сентябрь 2020 г.). «Энхансерные РНК предсказывают регуляторные связи между энхансером и геном и имеют решающее значение для функции энхансера в нейрональных системах» . Исследования нуклеиновых кислот . 48 (17): 9550–9570. дои : 10.1093/nar/gkaa671 . ПМЦ 7515708 . ПМИД 32810208 .
- ^ Михайличенко О., Бондаренко В., Харнетт Д., Шор И.Е., Малес М., Виалес Р.Р., Ферлонг Э.Э. (январь 2018 г.). «Степень активности энхансера или промотора отражается уровнями и направленностью транскрипции эРНК» . Гены и развитие . 32 (1): 42–57. дои : 10.1101/gad.308619.117 . ПМЦ 5828394 . ПМИД 29378788 .
- ^ Лай Ф., Ором У.А., Чезарони М., Берингер М., Таатжес Д.Д., Блобель Г.А., Шихаттар Р. (февраль 2013 г.). «Активирующие РНК связываются с медиатором для улучшения архитектуры и транскрипции хроматина» . Природа . 494 (7438): 497–501. Бибкод : 2013Natur.494..497L . дои : 10.1038/nature11884 . ПМК 4109059 . ПМИД 23417068 .
- ^ Аллен Б.Л., Taatjes DJ (март 2015 г.). «Медиаторный комплекс: центральный интегратор транскрипции» . Обзоры природы. Молекулярно-клеточная биология . 16 (3): 155–166. дои : 10.1038/nrm3951 . ПМЦ 4963239 . ПМИД 25693131 .
- ^ Jump up to: а б Сарторелли В., Лауберт С.М. (июнь 2020 г.). «Энхансерные РНК являются важным регуляторным слоем эпигенома» . Структурная и молекулярная биология природы . 27 (6): 521–528. дои : 10.1038/s41594-020-0446-0 . ПМЦ 7343394 . ПМИД 32514177 .
- ^ Jump up to: а б Хоу Т.Ю., Краус В.Л. (февраль 2021 г.). «Духи в материальном мире: РНК-энхансеры в регуляции транскрипции» . Тенденции биохимических наук . 46 (2): 138–153. дои : 10.1016/j.tibs.2020.08.007 . ПМК 7855021 . ПМИД 32888773 .
- ^ Jump up to: а б Арнольд П.Р., Уэллс А.Д., Ли XC (2019). «Разнообразие и новая роль энхансерной РНК в регуляции экспрессии генов и судьбы клеток» . Границы клеточной биологии и биологии развития . 7 : 377. дои : 10.3389/fcell.2019.00377 . ПМК 6971116 . ПМИД 31993419 .
- ^ Чжао Ю., Ван Л., Рен С., Ван Л., Блэкберн П.Р., МакНалти М.С. и др. (апрель 2016 г.). «Активация P-TEFb энхансерными РНК, регулируемыми андрогенными рецепторами, при устойчивом к кастрации раке простаты» . Отчеты по ячейкам . 15 (3): 599–610. дои : 10.1016/j.celrep.2016.03.038 . ПМЦ 5395199 . ПМИД 27068475 .
- ^ Шаукович К., Джу Дж.Й., Лю Икс, Уоттс Дж.К., Мартинес С., Ким Т.К. (октябрь 2014 г.). «Энхансерная РНК способствует высвобождению NELF из ранних ранних генов» . Молекулярная клетка . 56 (1): 29–42. doi : 10.1016/j.molcel.2014.08.023 . ПМК 4186258 . ПМИД 25263592 .
- ^ Jump up to: а б Уайерс Ф., Ружмейл М., Бадис Дж., Руссель Дж.К., Дюфур М.Э., Буле Дж. и др. (июнь 2005 г.). «Загадочные транскрипты pol II разрушаются путем ядерного контроля качества с участием новой поли(А)-полимеразы» . Клетка . 121 (5): 725–737. дои : 10.1016/j.cell.2005.04.030 . ПМИД 15935759 .
- ^ Рен Б (май 2010 г.). «Транскрипция: энхансеры создают некодирующую РНК» . Природа . 465 (7295): 173–174. Бибкод : 2010Natur.465..173R . дои : 10.1038/465173a . ПМИД 20463730 .
- ^ Обрдлик А., Кукалев А., Луве Э., Фаррантс А.К., Капуто Л., Перципалле П. (октябрь 2008 г.). «Гистон-ацетилтрансфераза PCAF связывается с актином и hnRNP U для транскрипции РНК-полимеразы II» . Молекулярная и клеточная биология . 28 (20): 6342–6357. дои : 10.1128/MCB.00766-08 . ПМЦ 2577438 . ПМИД 18710935 .
- ^ Фэн Дж., Би С., Кларк Б.С., Мэди Р., Шах П., Коц Дж.Д. (июнь 2006 г.). «Некодирующая РНК Evf-2 транскрибируется из ультраконсервативной области Dlx-5/6 и действует как коактиватор транскрипции Dlx-2» . Гены и развитие . 20 (11): 1470–1484. дои : 10.1101/gad.1416106 . ПМЦ 1475760 . ПМИД 16705037 .
- ^ Ван З., Герштейн М., Снайдер М. (январь 2009 г.). «RNA-Seq: революционный инструмент для транскриптомики» . Обзоры природы. Генетика . 10 (1): 57–63. дои : 10.1038/nrg2484 . ПМЦ 2949280 . ПМИД 19015660 .
- ^ Jump up to: а б Барски А., Каддапа С., Цуй К., Ро Т.И., Шонес Д.Е., Ван З. и др. (май 2007 г.). «Профилирование метилирования гистонов в геноме человека с высоким разрешением» . Клетка . 129 (4): 823–837. дои : 10.1016/j.cell.2007.05.009 . ПМИД 17512414 .
- ^ Мельгар М.Ф., Коллинз Ф.С., Сетупати П. (ноябрь 2011 г.). «Открытие активных энхансеров посредством двунаправленной экспрессии коротких транскриптов» . Геномная биология . 12 (11): Р113. дои : 10.1186/gb-2011-12-11-r113 . ПМЦ 3334599 . ПМИД 22082242 .
- ^ Крейтон М.П., Ченг А.В., Уэлстед Г.Г., Куистра Т., Кэри Б.В., Стайн Э.Дж. и др. (декабрь 2010 г.). «Гистон H3K27ac отделяет активные энхансеры от готовых и прогнозирует состояние развития» . Труды Национальной академии наук Соединенных Штатов Америки . 107 (50): 21931–21936. дои : 10.1073/pnas.1016071107 . ПМК 3003124 . ПМИД 21106759 .
- ^ Яо Л., Лян Дж., Озер А., Люнг А.К., Лис Дж.Т., Ю Х. (июль 2022 г.). «Сравнение экспериментальных анализов и аналитических методов полногеномной идентификации активных энхансеров» . Природная биотехнология . 40 (7): 1056–1065. дои : 10.1038/s41587-022-01211-7 . ПМЦ 9288987 . ПМИД 35177836 .
- ^ Махат Д.Б., Квак Х., Бут Г.Т., Джонкерс И.Х., Данко К.Г., Патель Р.К. и др. (август 2016 г.). «Полногеномное картирование активных РНК-полимераз с использованием точного ядерного анализа (PRO-seq)» . Протоколы природы . 11 (8): 1455–1476. дои : 10.1038/нпрот.2016.086 . ПМК 5502525 . ПМИД 27442863 .
- ^ Мело К.А., Дрост Дж., Вейчерс П.Дж., ван де Веркен Х., де Вит Э., Оуде Врилинк Дж.А. и др. (февраль 2013 г.). «eRNA необходимы для p53-зависимой активности энхансера и транскрипции генов» . Молекулярная клетка . 49 (3): 524–535. doi : 10.1016/j.molcel.2012.11.021 . ПМИД 23273978 .
- ^ Вусден К.Х., Лу X (август 2002 г.). «Живи или дай умереть: реакция клетки на р53» . Обзоры природы. Рак . 2 (8): 594–604. дои : 10.1038/nrc864 . ПМИД 12154352 . S2CID 6412605 .
- ^ Чжан, Трой; Ю, Хуэй; Цзян, Лимин; Бай, Юншэн; Лю, Сяои; Го, Ян (январь 2024 г.). «Комплексные закономерности плотности панраковых мутаций в энхансерной РНК» . Международный журнал молекулярных наук . 25 (1): 534. doi : 10.3390/ijms25010534 . ISSN 1422-0067 . ПМЦ 10778997 . ПМИД 38203707 .
Внешние ссылки
[ редактировать ]- База данных расширений Vista
- Проект Mouse ENCODE, заархивированный 13 декабря 2012 г. на Wayback Machine.
- Проект ENCODE в UCSC
- ПЕДБ