Тиамин пирофосфат

| |
| Имена | |
|---|---|
| Название ИЮПАК
2-[3-[(4-амино-2-метилпиримидин-5-ил)метил]-4-метил-1,3-тиазол-3-ий-5-ил]этилфосфоногидрофосфат
| |
| Другие имена
Тиамин дифосфат
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХимическийПаук | |
| КЕГГ | |
| МеШ | Тиамин+пирофосфат |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 12 Ч 19 Н 4 О 7 П 2 С + | |
| Молярная масса | 425.314382 g/mol |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Тиаминпирофосфат ( TPP или ThPP ), или тиаминдифосфат ( ThDP ), или кокарбоксилаза [ 1 ] представляет собой тиамина (витамина B 1 ) производное , которое вырабатывается ферментом тиаминдифосфокиназой . Тиаминпирофосфат — кофактор , присутствующий во всех живых системах, в которых он катализирует ряд биохимических реакций.
Тиаминпирофосфат синтезируется в цитозоле и необходим в цитозоле для активности транскетолазы и в митохондриях для активности пируват-, оксоглутарат- и дегидрогеназ кетокислот с разветвленной цепью. На сегодняшний день дрожжевой носитель ThPP (Tpc1p), человеческий Tpc и Drosophila melanogaster, идентифицирован как ответственный за митохондриальный транспорт ThPP и ThMP. [ 2 ] [ 3 ] [ 4 ] Впервые он был обнаружен в качестве незаменимого питательного вещества ( витамина ) у людей благодаря его связи с периферической нервной системы заболеванием бери-бери , которое возникает в результате дефицита тиамина в рационе . [ 5 ]
TPP действует как кофермент во многих ферментативных реакциях, таких как:
- пируватдегидрогеназы Комплекс [ 6 ]
- Пируватдекарбоксилаза в ферментации этанола
- Альфа-кетоглутаратдегидрогеназный комплекс
- аминокислот с разветвленной цепью Дегидрогеназный комплекс
- 2-гидроксифитаноил-КоА-лиаза
- Транскетолаза
Химия
[ редактировать ]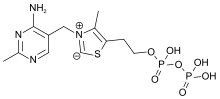
Химически TPP состоит из пиримидинового кольца, которое соединено с тиазольным кольцом, которое, в свою очередь, связано с пирофосфатной (дифосфатной) функциональной группой .
Частью молекулы ТФП, которая чаще всего участвует в реакциях, является тиазольное кольцо, содержащее азот и серу . Таким образом, тиазольное кольцо является «реагентной частью» молекулы. C2 этого кольца способен действовать как кислота , отдавая свой протон и образуя карбанион . [ 7 ] Обычно реакции с образованием карбанионов крайне неблагоприятны, но положительный заряд четырехвалентного азота, примыкающего к карбаниону, стабилизирует отрицательный заряд, делая реакцию намного более благоприятной. [ 7 ] Соединение с положительными и отрицательными зарядами на соседних атомах называется илидом , поэтому иногда карбанионную форму ТФП называют «илидной формой». [ 5 ] [ 8 ]
Механизмы реакции
[ редактировать ]В нескольких реакциях, включая реакцию пируватдегидрогеназы, альфа-кетоглутаратдегидрогеназы и транскетолазы, TPP катализирует обратимую реакцию декарбоксилирования (то есть расщепление соединения-субстрата по углерод-углеродной связи, соединяющей карбонильную группу с соседней реакционноспособной группой - обычно карбоксильной). кислота или спирт ). Это достигается за четыре основных этапа:
- Карбанион илида ТПП нуклеофильно атакует карбонильную группу субстрата. (Это образует одинарную связь между TPP и подложкой.)
- Целевая связь на подложке разрывается, и ее электроны выталкиваются в сторону ТПП. Это создает двойную связь между углеродом подложки и углеродом TPP и полностью выталкивает электроны двойной связи NC в TPP на атом азота, восстанавливая его из положительной формы в нейтральную.
- По сути, это противоположно второму шагу: электроны отталкиваются в противоположном направлении, образуя новую связь между углеродом подложки и другим атомом. (В случае декарбоксилаз это создает новую углерод-водородную связь. В случае транскетолазы это атакует новую молекулу субстрата с образованием новой углерод-углеродной связи.)
- На этапе, обратном первому, связь TPP-субстрат разрывается, образуя илид TPP и карбонил субстрата.
Тиазолиевое кольцо TPP может быть депротонировано по положению C2 с образованием илида :
Полный обзор ТЭЦ. Стрелка указывает на кислый протон.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Петржак I (1995). «[Витаминные нарушения при хронической почечной недостаточности. I. Водорастворимые витамины]». Медицинское обозрение (на польском языке). 52 (10): 522–5. ПМИД 8834846 .
- ^ Мароббио, CMT; Возза, А.; Хардинг, М.; Бисачча, Ф.; Пальмиери, Ф.; Уокер, Дж. Э. (1 ноября 2002 г.). «Идентификация и восстановление дрожжевого митохондриального переносчика тиаминпирофосфата» . Журнал ЭМБО . 21 (21): 5653–5661. дои : 10.1093/emboj/cdf583 . ISSN 0261-4189 . ПМК 131080 . ПМИД 12411483 .
- ^ Якопетта, Доменико; Карризи, Кьяра; Де Филиппис, Джузеппина; Кальканьиле, Валерия М.; Каппелло, Анна Р.; Чименто, Адель; Курсио, Розита; Санторо, Антонелла; Возза, Анджело (01 марта 2010 г.). «Биохимические свойства митохондриального переносчика тиаминпирофосфата Drosophila melanogaster» . Журнал ФЭБС . 277 (5): 1172–1181. дои : 10.1111/j.1742-4658.2009.07550.x . ISSN 1742-4658 . ПМИД 20121944 .
- ^ Линдхерст, Марджори Дж.; Фьермонте, Джузеппе; Сун, Шивэй; Стройс, Эдуард; Леонардис, Франческо Де; Шварцберг, Памела Л.; Чен, Эми; Кастенья, Алессандра; Верховен, Нанда (24 октября 2006 г.). «Нокаут Slc25a19 вызывает истощение митохондриального тиаминпирофосфата, эмбриональную летальность, пороки развития ЦНС и анемию» . Труды Национальной академии наук . 103 (43): 15927–15932. Бибкод : 2006PNAS..10315927L . дои : 10.1073/pnas.0607661103 . ISSN 0027-8424 . ПМК 1595310 . ПМИД 17035501 .
- ^ Перейти обратно: а б Павиа, Дональд Л., Гэри М. Лэмпман, Джордж С. Криц, Рэндалл Г. Энгель (2006). Введение в органические лабораторные методы (4-е изд.) . Томсон Брукс/Коул. стр. 304–5. ISBN 978-0-495-28069-9 .
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ «PDB для биохимии» . Государственный университет Джорджии. Архивировано из оригинала 16 июля 2011 г. Проверено 7 февраля 2009 г.
- ^ Перейти обратно: а б Бегли, Тадг П.; Илик, Стивен Э. (01 января 2010 г.), Лю, Хун-Вэнь (Бен); Мандер, Лью (ред.), «7.15 - Биосинтез тиамина» , Comprehensive Natural Products II , Oxford: Elsevier, стр. 547–559, doi : 10.1016/b978-008045382-8.00148-9 , ISBN 978-0-08-045382-8 , получено 16 декабря 2020 г.
- ^ Воэт, Дональд; Джудит Воэт; Шарлотта Пратт (2008). Основы биохимии . John Wiley & Sons Inc. с. 508 . ISBN 978-0-470-12930-2 .


