Гексадегидро реакция Дильса – Альдера
В органической химии органическую химическую реакцию между реакция гексадегидро-Дильса-Альдера (HDDA) представляет собой диином ( 2 алкиновые функциональные группы, расположенные в сопряженной системе ) и алкином с образованием реакционноспособных разновидностей бензона через [4+2] реакция циклоприсоединения . [ 1 ] [ 2 ] [ 3 ] Этот промежуточный бензол затем реагирует с подходящим улавливающим агентом с образованием замещенного ароматического продукта. Эта реакция является производной известной реакции Дильса-Альдера и протекает по аналогичному механизму [4+2]-циклоприсоединения. Реакция HDDA особенно эффективна для образования сильно функционализированных ароматических систем и систем с несколькими кольцами за одну синтетическую стадию.

Механизм реакции
[ редактировать ]В зависимости от выбранного субстрата реакция HDDA может быть инициирована термически или добавлением подходящего катализатора , часто переходного металла . [ 1 ] [ 2 ] [ 4 ] [ 5 ] Преобладающим механизмом термически инициируемой реакции HDDA является [4+2]-циклоприсоединение между сопряженным диином (1,3-диалкином) и алкином (часто называемым диинофилом по аналогии с диенофилом Дильса-Альдера ) с образованием орто . - бензиновая разновидность [ 1 ] [ 2 ] Считается, что катализируемый металлами HDDA протекает по аналогичному пути, образуя стабилизированный металлом бензин, который затем улавливается.
Самая простая модель реакции HDDA - это циклоприсоединение бутадиина и ацетилена с образованием орто-бензина (о-бензина, показанного ниже). [ 6 ] Этот реакционноспособный промежуточный продукт (обозначен скобками) впоследствии реагирует с обобщенным улавливающим реагентом, который состоит из нуклеофильного (Nu-) и электрофильного (El-) центра, образуя показанный бензоидный продукт.
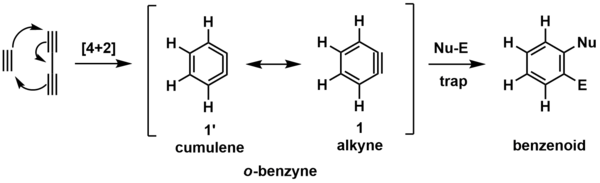
Промежуточное соединение о-бензина можно визуализировать в двух резонансных (химических) формах, показанных выше. Наиболее часто изображаемой формой является алкин ( 1 ), но кумуленовая форма ( 1' ) может быть полезна для визуализации образования кольца путем [4+2] циклоприсоединения.
Термодинамика и кинетика
[ редактировать ]Реакция HDDA часто термодинамически выгодна ( экзотермична ), но может иметь значительный кинетический барьер для реакции (высокая энергия активации ). Расчеты показали, что образование незамещенного о-бензина (из бутадиина и ацетилена, см. выше) имеет энергию активации 36 ккал моль. −1 , но является термодинамически благоприятным, по оценкам, экзотермическим на -51 ккал моль. −1 . [ 6 ] В результате более высокой энергии активации некоторые реакции HDDA требуют нагрева до повышенных температур (> 100 ° C), чтобы инициироваться. [ 1 ] [ 2 ]
Кроме того, стадия улавливания бензола также является термодинамически выгодной, поскольку, по расчетам, она требует дополнительных затрат -73 ккал на моль. −1 для улавливания эфирзамещенного о-бензина трет-бутанолом . [ 1 ]

Циклоприсоединение HDDA [4+2] может происходить либо по согласованному пути, либо по ступенчатой реакции , дирадикальному пути. Эти два пути могут различаться по энергии активации в зависимости от субстрата и реакционной системы. Компьютерные исследования показали, что, хотя оба пути сопоставимы по энергии активации для неактивированных (незамещенных) диинофилов, ступенчатый путь имеет более низкий энергетический барьер активации, и поэтому является доминирующим путем для активированных диинофилов. [ 6 ] [ 7 ]
региохимия
[ редактировать ]Региохимию несимметричного захвата бензола, производного HDDA, можно объяснить комбинацией эффектов электронного и кольцевого искажения. [ 1 ] Согласно расчетам, более тупой угол ( a ) соответствует более электронодефицитному (δ+) углероду бензола, что приводит к атаке нуклеофильного компонента в этом месте. Следовательно, электрофильный компонент добавляется к более богатому электронами (δ-) участку ( b ).

Терминология
[ редактировать ]Реакция HDDA является производной классической реакции Дильса-Альдера и механически связана с ней. Как описали Хой и его коллеги, реакцию HDDA концептуально можно рассматривать как часть серии перициклических реакций с увеличением ненасыщенности (путем постепенного удаления пар водорода ). [ 1 ] Дескриптор «гексадегидро» получен из этой интерпретации, поскольку простейший продукт реакции HDDA (о-бензин, 4 атома водорода) имеет на 6 атомов водорода меньше, чем простейший продукт реакции Дильса-Альдера ( циклогексен , 10 атомов водорода).

Формально реакция гексадегидро Дильса-Альдера описывает только образование бензона, но этот вид представляет собой нестабильный промежуточный продукт, который легко реагирует с множеством партнеров-ловушек, включая растворители реакции . Таким образом, на практике реакция HDDA представляет собой двухстадийную каскадную реакцию образования и улавливания бензона с получением конечного продукта.
Историческое развитие
[ редактировать ]О первых примерах реакции HDDA сообщили независимо в 1997 году группы Уэды и Джонсона. [ 2 ] [ 8 ] [ 9 ] [ 10 ] Джонсон и его коллеги наблюдали циклизацию 1,3,8-нонатриина при флэш-вакуумном термолизе (600 °C, 10 −2 торр) с образованием двух продуктов, индана и продукта дегидрирования индена , с общим выходом 95%. Исследования по мечению дейтерием показали, что продукт образовался в результате [4+2] циклоприсоединения к промежуточному бензолу с последующим восстановлением in-situ с образованием наблюдаемых продуктов. [ 8 ] Уэда и его коллеги заметили, что ациклические тетраины циклизуются при комнатной температуре с образованием производных 5H-флуоренола. Образование промежуточного бензола было определено с помощью исследований по улавливанию бензола или антрацена для улавливания бензола в виде аддукта Дильса-Альдера. [ 10 ] Уэда и его коллеги подробно остановились на этом методе в последующих отчетах, улавливая бензон с помощью различных нуклеофилов (кислорода, азота и серы), а также синтезируя более крупные ароматические системы с конденсированными кольцами. [ 11 ] [ 12 ] [ 13 ] [ 14 ] [ 15 ]
Реакция HDDA, известная уже более десяти лет, не получила более широкого синтетического использования до 2012 года, когда Хой и его коллеги провели тщательное исследование масштабов и полезности этого циклоприсоединения. [ 1 ] В этой статье эта реакция диин-диинофил называлась «гексадегидрореакцией Дильса-Альдера (HDDA) , и с тех пор эта терминология получила более широкое распространение. С 2012 года реакция HDDA стала областью нового интереса и привлекла дальнейшее изучение ряда исследовательских групп. [ 4 ] [ 5 ] [ 7 ] [ 16 ]
Объем реакции
[ редактировать ]Одним из основных преимуществ реакции HDDA перед другими методами получения бензолов является простота реакционной системы. Реакция HDDA триинов или тетраинов образует бензоны без прямого образования побочных продуктов. Для сравнения, образование бензола путем удаления орто-заместителей на аренах приводит к образованию стехиометрических количеств побочных продуктов от этих заместителей. Например, при образовании бензола из 1 моля 2-триметилсилилфенилтрифторметансульфоната ( трифлата ) образуется 1 моль триметилсилилфторида и 1 моль трифлат-иона. Побочные продукты могут конкурировать с другими реагентами за улавливание бензона, вызывать побочные реакции и могут требовать дополнительной очистки.
Кроме того, реакция HDDA может быть полезна для субстратов с чувствительной функциональностью, которые могут быть непереносимы другими условиями образования бензола (например, сильным основанием). Было показано, что термически инициируемая реакция HDDA переносит сложные эфиры , кетоны , защищенные амиды , простые эфиры , защищенные амины , арилгалогениды , алкилгалогениды , алкены и циклопропаны . [ 1 ] [ 4 ] [ 17 ]
Зеленая химия
[ редактировать ]Реакция HDDA может соответствовать нескольким принципам зеленой химии .
- Экономия атомов . Все атомы в субстрате HDDA остаются в продукте после реакции, а атомы улавливающего реагента включаются в продукт.
- Сокращение отходов . При образовании бензола не образуются стехиометрические побочные продукты. Продукты часто образуются с высоким выходом и небольшим количеством побочных продуктов.
- Катализ – реакция HDDA происходит термически или с использованием субстехиометрического количества катализатора .
Синтетические приложения
[ редактировать ]Внутримолекулярный захват
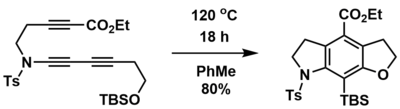
[ редактировать ]Реакция HDDA может быть использована для синтеза мультициклических кольцевых систем из линейных предшественников, содержащих диин, диинофил и захватывающую группу. Например, Хой и его коллеги смогли синтезировать конденсированные трициклические кольцевые системы из линейных предшественников триинов за одну стадию и с высокими выходами посредством термически инициируемой внутримолекулярной реакции HDDA. [ 1 ] Кроме того, как азотсодержащие, так и кислородсодержащие гетероциклы могут быть включены с использованием подходящего предшественника. В этом случае подвесной илиловый эфир обеспечивает захватывающую группу посредством ретро- перегруппировки Брука .
Межмолекулярный захват
[ редактировать ]Бензины, генерируемые HDDA, также можно захватывать межмолекулярно с помощью различных улавливающих реагентов. Тщательный выбор улавливающего реагента может добавить дополнительную функциональность, включая арилгалогениды, арилгетероатомы ( фенолы и производные анилина ) и системы с несколькими кольцами. [ 1 ] [ 18 ]

Эне реакции
[ редактировать ]Реакцию HDDA можно использовать в каскадной последовательности реакций с еновыми реакциями , такими как реакция Альдера ена и реакция ароматического ена. [ 16 ] [ 19 ] Бензин, образуемый HDDA, можно захватить подходящим донором ена, который ковалентно связан с бензолом. Бензин служит энофилом, а ен может представлять собой алкен (ен Альдера) или ароматическое кольцо (ароматический ен). Ли и его коллеги продемонстрировали каскадную реакцию HDDA-Альдера, которая может давать множество продуктов, включая конденсированные кольца среднего размера, спироциклы и аллены . [ 16 ]

Хой и его коллеги продемонстрировали термически инициируемый тройной каскад HDDA-ароматический ен-альдерен, который приводит к образованию сильно функционализированных продуктов за одну стадию без дополнительных реагентов или побочных продуктов. [ 19 ]

Дегидрирование
[ редактировать ]Также было показано, что бензоны, полученные из HDDA, дегидрируют насыщенные алканы с образованием алкенов . [ 20 ] В отсутствие внешних улавливающих реагентов промежуточный бензол может отрывать вицинальные (химические) атомы водорода от подходящего донора, часто растворителя реакции (такого как тетрагидрофуран или циклооктан ). Это обесцвечивает донорный алкан, образуя алкен , и захватывает бензол в дигидробензеноидный продукт. Изотопная маркировка и компьютерные исследования позволяют предположить, что механизм двойного переноса водорода происходит по согласованному пути и что скорость реакции сильно зависит от конформации донора алкана. [ 20 ] Эту реакцию можно использовать для доступа к 1,2,3,4-тетразамещенным ароматическим кольцам - схеме замещения, доступ к которой может быть затруднен с помощью других синтетических методологий.

Активация CH
[ редактировать ]Реакцию HDDA также можно использовать в качестве метода активации CH , когда боковая алкановая связь CH промежуточный продукт , образующий комплекс с металлом захватывает ариновый . Ли и его коллеги заметили, что катализаторы на основе переходных металлов индуцируют реакцию HDDA тетраинов, которые внутримолекулярно захватываются кулоном sp. 3 облигация CH. [ 4 ] Первичные, вторичные и третичные связи CH были реакционноспособными партнерами по захвату, причем соли серебра были наиболее эффективными катализаторами. Эксперименты по мечению дейтерия показывают, что (sp 3 ) разрыв связи CH и (sp 2 ) Реакции образования связи CH протекают согласованно.

Фторирование
[ редактировать ]катализируемая серебром, также использовалась для синтеза фторорганических соединений с использованием фторсодержащего Реакция HDDA , противоиона . [ 17 ] Промежуточный арин, образующий комплекс с металлом, может быть захвачен противоионом с образованием арильных колец с фтор-, трифторметильными или трифторметилтиоловыми заместителями. Нестабильные противоионы, такие как CF 3. − , может быть изготовлен на месте.

Реакция домино HDDA
[ редактировать ]Было показано, что правильно разработанный полииновый субстрат подвергается эффективному каскадному сетчатому [4+2] циклоприсоединениям просто при нагревании. [ 21 ] Эта реакция домино гексадегидро Дильса-Альдера инициируется образованием бензина, ограничивающим скорость. Проходя через промежуточные соединения нафтина, антрацина и/или тетрацина, в результате происходит быстрый восходящий синтез высококонденсированных полициклических ароматических соединений.

Реакция аза HDDA
[ редактировать ]Нитрилы также могут участвовать в реакциях HDDA с образованием промежуточных пиридиновых соединений. [ 22 ] Захват пиридинов in situ приводит к образованию сильнозамещенных и функционализированных производных пиридина, что дополняет другие классические подходы к построению этого важного класса гетероциклов.

Радиальные реакции HDDA
[ редактировать ]Конструкторские мультиины, расположенные на общей центральной матрице, подвергаются последовательным множественным реакциям циклоизомеризации для получения архитектурно новых полициклических соединений за одну операцию. [ 23 ] Доступны разнообразные топологии продуктов: от высококонденсированных полициклических ароматических соединений (PAC) до архитектур со структурно сложными плечами, украшающими центральные фениленовые или расширенные фениленовые ядра.

Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж к Хой, TR; Бэр, Б.; Ню, Д.; Уиллоби, штат Пенсильвания; Вудс, BP Nature , 2012 , 490 , 208 [1]
- ^ Jump up to: а б с д и Холден, К.; Грини, М.Ф. Энджью. хим. Межд. Эд. англ. , 2014 , 53 , 5746 [2]
- ^ Йомен, JTS; Райсман, ГП Природа , 2012 , 490 , 179
- ^ Jump up to: а б с д Юн, С.Ю.; Ван, К.-П.; Ли, Северная Каролина; Мамидипалли, П.; Ли, DJ Am. Ткань. Соц. , 2013 , 135 , 4668 [3]
- ^ Jump up to: а б Вандаваси, Дж. К.; Ху, В.-П.; Сяо, Коннектикут; Сенади, GC; Ван, Ж.-Ж. РСК Адв. , 2014 , 4 , 57547 [4]
- ^ Jump up to: а б с Аджаз, А.; Брэдли, Аризона; Баррелл, Колорадо; Ли, WHH; Хотя, Кей Джей; Бови, LB; ДиРико, К.Дж.; Джонсон, RRJ Org. хим. , 2011 , 76 , 9320 [5]
- ^ Jump up to: а б Лян, Ю.; Хонг, X.; Ага.; Хоук, К.Н. Орг. Летт. , 2014 , 16 , 5702 [6]
- ^ Jump up to: а б Брэдли, Аризона; Джонсон, Р.П. Дж. Ам. хим. Соц. , 1997 , 119 , 9917 [7]
- ^ Кэхилл, К.Дж.; Аджаз, А.; Джонсон, Р.П. Ауст. Дж. Хим. , 2010 , 63 , 1007 [8]
- ^ Jump up to: а б Мияваки, К.; Кавано, Т.; Уэда, И. Tetrahedron Lett. , 1997 , 38 , 3943 [9].
- ^ Уэда, И.; Сакурай, Ю.; Кавано, Т.; Вада, Ю.; Футай, М. Тетраэдр Летт. , 1999 , 40 , 319 [10]
- ^ Мияваки, К.; Кавано, Т.; Уэда, И. Тетраэдр Летт. , 2000 , 41 ,
- ^ К. Мияваки, Ф. Уэно, И. Уэда, Гетероциклы , 2001 , 54 , 887 [12]
- ^ Торкей, К.; Оцука, Ю.; Нисимура, М.; Сумида, М.; Каваи, Т.; Секигути, К.; Уэда, И. Биоорг. Мед. хим. , 2008 , 16 , 5441 [13]
- ^ Кимура, Х.; Торикай, К.; Мияваки, К.; Уэда, И. Хим. Летт. , 2008 , 37 , 662 [14] [ постоянная мертвая ссылка ]
- ^ Jump up to: а б с Кармакар, Р.; Мамидипалли, П.; Юн, С.Ю.; Ли, Д. Орг. Летт. , 2013 , 15 , 1938 [15]
- ^ Jump up to: а б Wang, K.-P.; Yun, S. Y.; Mamidipalli, P.; Lee, D. Chem. Sci. , 2013 , 4 , 3205 [16]
- ^ Ню, Д.; Ван, Т.; Вудс, BP; Хой, TR Org. Летт. , 2014 , 16 , 254 [17]
- ^ Jump up to: а б Niu, D.; Hoye, T. R. Nat. Chem. , 2014 , 6 , 34
- ^ Jump up to: а б Ню, Д.; Уиллоби, штат Пенсильвания; Вудс, BP; Бэр, Б.; Хой, TR Nature , 2013 , 501, 531 [18]
- ^ Сяо, Сяо; Хой, Томас Р. (20 июля 2018 г.). «Реакция домино гексадегидро-Дильса-Альдера превращает полиины в бензины, затем нафтины, антрацины и тетрацины (и далее?)» . Природная химия . 10 (8): 838–844. Бибкод : 2018НатЧ..10..838Х . дои : 10.1038/s41557-018-0075-y . ISSN 1755-4349 . ПМК 6284823 . ПМИД 30030536 .
- ^ Томпсон, Северин К.; Хой, Томас Р. (01 декабря 2019 г.). «Аза-гексадегидро-Дильса-Альдера» . Журнал Американского химического общества . 141 (50): 19575–19580. дои : 10.1021/jacs.9b11243 . ISSN 0002-7863 . ПМК 6921493 . ПМИД 31789026 .
- ^ Ли, Дэниел; Росс, Шон П.; Сяо, Сяо; Хой, Томас Р. (9 сентября 2021 г.). «Радиальные гексадегидро-реакции Дильса-Альдера» . Хим . 7 (9): 2527–2537. дои : 10.1016/j.chempr.2021.08.010 . ISSN 2451-9294 . ПМЦ 8797013 . ПМИД 35097238 .