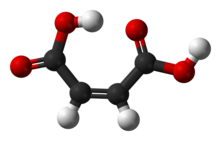
Малеиновая кислота

| |
| |
| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
(2 Z )-Бут-2-эндиовая кислота | |
| Другие имена
( Z )-Бутендиовая кислота; цис -бутендиовая кислота; Маленовая кислота; Малеиновая кислота; Токсичная кислота
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 3DMeet | |
| 605762 | |
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Лекарственный Банк | |
| Информационная карта ECHA | 100.003.403 |
| Номер ЕС |
|
| 49854 | |
| КЕГГ | |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 4 Н 4 О 4 | |
| Молярная масса | 116.072 g·mol −1 |
| Появление | Белый твердый |
| Плотность | 1,59 г/см 3 [ 1 ] |
| Температура плавления | 135 ° C (275 ° F, 408 К) (разлагается) [ 2 ] |
| 478,8 г/л при 20°С [ 2 ] | |
| Кислотность ( pKa ) | от р до а1 = 1,90 р к а2 = 6,07 [ 3 ] |
| -49.71·10 −6 см 3 /моль | |
| Опасности | |
| СГС Маркировка : | |

| |
| Предупреждение | |
| Х302 , Х315 , Х317 , Х319 , Х335 | |
| P261 , P264 , P270 , P271 , P272 , P280 , P301+P312 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P330 , P332+P313 , П333+П313 , П337+П313 , П362 , П363 , П403+П233 , П405 , П501 | |
| NFPA 704 (огненный алмаз) | |
| Паспорт безопасности (SDS) | Паспорт безопасности от JT Baker |
| Родственные соединения | |
Родственные карбоновые кислоты
|
фумаровая кислота янтарная кислота кротоновая кислота |
Родственные соединения
|
малеиновый ангидрид мужские имена |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Малеиновая кислота или цис -бутендиовая кислота представляет собой органическое соединение , представляющее собой дикарбоновую кислоту , молекулу с двумя карбоксильными группами. Его химическая формула: HO 2 CCH=CHCO 2 H. Малеиновая кислота является цис -изомером бутендиовой кислоты, тогда как фумаровая кислота является транс -изомером. Он в основном используется в качестве предшественника фумаровой кислоты и относительно его исходного малеинового ангидрида , который имеет множество применений. [ 4 ]
Физические свойства
[ редактировать ]Малеиновая кислота имеет теплоту сгорания -1,355 кДж/моль., [ 5 ] на 22,7 кДж/моль выше, чем у фумаровой кислоты. Малеиновая кислота более растворима в воде, чем фумаровая кислота . Температура плавления малеиновой кислоты (135 °С) также намного ниже, чем у фумаровой кислоты (287 °С). Как подтверждено рентгеноструктурным анализом , малеиновая кислота плоская. две нормальные водородные связи Наблюдаются : одна внутримолекулярная и одна межмолекулярная. Кристаллографический анализ показывает, что внутримолекулярная водородная связь в монокалиевой соли нарушена незначительно. [ 6 ]
Производство и промышленное применение
[ редактировать ]В промышленности малеиновую кислоту получают гидролизом малеинового ангидрида последний получают окислением бензола , причем или бутана . [ 4 ]
Малеиновая кислота — промышленное сырье для производства глиоксиловой кислоты методом озонолиза . [ 7 ]
Малеиновую кислоту можно использовать для образования кислотно-аддитивных солей с лекарствами, чтобы сделать их более стабильными, например малеата индакатерола.
Малеиновая кислота также используется в качестве усилителя адгезии для различных подложек, таких как нейлон и металлы с цинковым покрытием, например, оцинкованная сталь, в клеях на основе метилметакрилата.
Изомеризация в фумаровую кислоту
[ редактировать ]Основное промышленное использование малеиновой кислоты — ее преобразование в фумаровую кислоту . Это преобразование, изомеризация , катализируется различными реагентами, такими как минеральные кислоты и тиомочевина . Опять же, большая разница в растворимости в воде облегчает очистку фумаровой кислоты.
Изомеризация — популярная тема в школах. Малеиновая кислота и фумаровая кислота не подвергаются самопроизвольному взаимному превращению, поскольку вращение вокруг двойной связи углерода и углерода энергетически невыгодно. Однако превращение цис- изомера в транс -изомер возможно путем фотолиза в присутствии небольшого количества брома . [ 8 ] Свет превращает элементарный бром в радикал брома , который атакует алкен в реакции радикального присоединения к бромалкановому радикалу; и теперь возможно вращение одинарных связей. Радикалы брома рекомбинируют и образуется фумаровая кислота. В другом методе (используемом в качестве демонстрации в классе) малеиновая кислота превращается в фумаровую кислоту в процессе нагревания малеиновой кислоты в растворе соляной кислоты . Обратимое присоединение (H + ) приводит к свободному вращению вокруг центральной связи CC и образованию более стабильной и менее растворимой фумаровой кислоты.
Некоторые бактерии вырабатывают фермент малеат-изомеразу , который используется бактериями в метаболизме никотината . Этот фермент катализирует изомеризацию фумарата и малеата.
Другие реакции
[ редактировать ]Хотя это и не практикуется в коммерческих целях, малеиновую кислоту можно превратить в малеиновый ангидрид путем дегидратации , в яблочную кислоту путем гидратации и в янтарную кислоту путем гидрирования ( этанол / палладий на угле ). [ 9 ] Он реагирует с тионилхлоридом или пентахлоридом фосфора с образованием хлорида малеиновой кислоты (выделить хлорангидрид монокислоты невозможно). Малеиновая кислота, будучи электрофильной, участвует в качестве диенофила во многих Дильса-Альдера реакциях .
Малеаты
[ редактировать ]Малеат -ион представляет собой ионизированную форму малеиновой кислоты. Ион малеата полезен в биохимии как ингибитор трансаминазных реакций. малеиновой кислоты Эфиры также называют малеатами, например диметилмалеат .
Использование в фармацевтических препаратах
[ редактировать ]Многие лекарства, содержащие амины , поставляются в виде соли малеиновой кислоты , например карфеназин , хлорфенирамин , пириламин , метилэргоновин и тиэтилперазин . [ 10 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Будавари, Сьюзен, изд. (1996), Индекс Merck: Энциклопедия химических веществ, лекарств и биологических препаратов (12-е изд.), Merck, ISBN 0911910123
- ^ Jump up to: а б Запись в базе данных веществ ГЕСТИС Института охраны труда.
- ^ Справочник CRC по химии и физике, 73-е изд.; CRC Press: Бока-Ратон, Флорида, 1993 г.
- ^ Jump up to: а б Лобек, Курт; Хаферкорн, Герберт; Фурманн, Вернер; Федтке, Норберт (2000). «Малеиновая и фумаровая кислоты». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a16_053 . ISBN 9783527303854 .
- ^ Малеиновый ангидрид, малеиновая кислота и фумаровая кислота. Архивировано 2 ноября 2013 г. в Wayback Machine , Huntsman Petrochemical Corporation.
- ^ М. Н. Дж. Джеймс, Г. Дж. Б. Уильямс (1974). «Уточнение кристаллической структуры малеиновой кислоты» . Акта Кристаллографика . Б30 (5) (5): 1249–1275. Бибкод : 1974AcCrB..30.1249J . дои : 10.1107/S0567740874004626 .
- ^ Производство глиоксиловой кислоты DSM. Архивировано 30 ноября 2005 г. в Wayback Machine.
- ^ Эксперимент по легкой изомеризации. Архивировано 27 ноября 2005 г. в Wayback Machine (из Регенсбургского университета , с видео).
- ^ Квеси Амоа (2007). «Каталитическое гидрирование малеиновой кислоты при умеренном давлении. Лабораторная демонстрация». Журнал химического образования . 84 (12): 1948. Бибкод : 2007JChEd..84.1948A . дои : 10.1021/ed084p1948 .
- ^ «NCATS Inxight Drugs — Фумаровая кислота» . Drugs.ncats.io . Проверено 10 ноября 2023 г.
