Конъюгат антитело-лекарственное средство
Конъюгаты антитело-лекарство или ADC представляют собой класс биофармацевтических препаратов, разработанных для таргетной терапии лечения рака. [1] В отличие от химиотерапии , ADC предназначены для уничтожения опухолевых клеток, сохраняя при этом здоровые клетки. По состоянию на 2019 год около 56 фармацевтических компаний занимались разработкой ADC. [2]
ADC представляют собой сложные молекулы, состоящие из антитела, связанного с биологически активной цитотоксической (противораковой) нагрузкой или лекарством. [3] Конъюгаты антитело-лекарственное средство являются примером биоконъюгатов и иммуноконъюгатов .
ADC сочетают в себе таргетные свойства моноклональных антител с способностью цитотоксических препаратов уничтожать рак, предназначенными для различения здоровых и больных тканей. [4] [5]
Механизм действия
[ редактировать ]Противораковый препарат связан с антителом, нацеленным на конкретный опухолевый антиген (или белок ), который в идеале обнаруживается только внутри или на опухолевых клетках. Антитела прикрепляются к антигенам на поверхности раковых клеток. Биохимическая реакция, возникающая при прикреплении, запускает сигнал в опухолевой клетке, которая затем поглощает или интернализует антитело вместе со связанным цитотоксином. После интернализации ADC цитотоксин убивает рак. [6] Считалось, что их таргетная способность ограничивает побочные эффекты у онкологических больных и обеспечивает более широкий терапевтический диапазон , чем у других химиотерапевтических агентов, хотя это обещание еще не было реализовано в клинике. [7]
Технологии АЦП были описаны во многих публикациях, [8] [9] включая научные журналы.
История
[ редактировать ]Идея лекарств, которые будут воздействовать на опухолевые клетки и игнорировать другие, была задумана в 1900 году немецким лауреатом Нобелевской премии Паулем Эрлихом ; он назвал эти наркотики «волшебной пулей» из-за их таргетных свойств. [2]
В 2001 году (торговое название: Милотарг) компании Pfizer / Wyeth препарат Гемтузумаб озогамицин был одобрен на основании исследования с суррогатной конечной точкой посредством ускоренного процесса утверждения . В июне 2010 года, после того как были собраны доказательства отсутствия преимуществ и значительной токсичности, Управление по контролю за продуктами и лекарствами США (FDA) вынудило компанию отозвать его. [10] Он был повторно представлен на рынке США в 2017 году. [11]
Брентуксимаб ведотин (торговое название: Адцетрис, продается компаниями Seattle Genetics и Millennium/Takeda) [12] был одобрен для лечения рецидивирующей ЛХ и рецидивирующей системной анапластической крупноклеточной лимфомы FDA (сАЛКЛ) 19 августа 2011 г. и получил условное разрешение на продажу от Европейского агентства по лекарственным средствам в октябре 2012 г.
Трастузумаб эмтанзин (адо-трастузумаб эмтанзин или T-DM1, торговое название: Kadcyla, продается компаниями Genentech и Roche) был одобрен в феврале 2013 года для лечения людей с HER2-положительным метастатическим раком молочной железы (mРМЖ), которые ранее получали лечение трастузумабом. и таксановая химиотерапия. [13] [14]
Европейская комиссия одобрила Инотузумаб озогамицин [15] в качестве монотерапии для лечения взрослых с рецидивирующим или рефрактерным CD22-положительным В-клеточным предшественником острого лимфобластного лейкоза (ОЛЛ) 30 июня 2017 г. под торговым названием Besponsa® (Pfizer/Wyeth), [16] за ним последовало 17 августа 2017 г. FDA. [17]
Первый иммунологический конъюгат антитело-лекарственное средство (iADC), ABBV-3373, [18] показали улучшение активности заболевания в исследовании фазы 2а у пациентов с ревматоидным артритом. [19] и исследование со вторым iADC, ABBV-154. [20] [21] Оценка побочных эффектов и изменений активности заболевания у участников, получавших подкожную инъекцию ABBV-154, продолжается. [22]
В июле 2018 года компании Daiichi Sankyo Company, Limited и Glycotope GmbH подписали договор о сочетании исследовательского опухолеассоциированного антитела TA-MUC1 Glycotope гатипотузумаба и запатентованной технологии ADC Daiichi Sankyo для разработки конъюгата антитела гатипотузумаба с лекарственным средством. [23]
В 2019 году AstraZeneca согласилась выплатить до 6,9 миллиардов долларов США на совместную разработку DS-8201 с японской Daiichi Sankyo . Он призван заменить Герцептин при лечении рака молочной железы. DS8201 несет восемь полезных нагрузок вместо обычных четырех. [2]
Коммерческие продукты
[ редактировать ]Тринадцать ADC получили одобрение FDA на рынке – все для онкотерапии . Белантамаб мафодотин находится в процессе вывода из продажи в США.
| Лекарство | Торговое название | Создатель | Состояние |
|---|---|---|---|
| Гемтузумаб озогамицин | Милотарг | Пфайзер / Уайет | рецидив острого миелогенного лейкоза (ОМЛ) |
| Брентуксимаб ведотин | Ты догонишь | Сиэтл Генетикс , Миллениум/Такеда | Лимфома Ходжкина (ЛХ) и системная анапластическая крупноклеточная лимфома (АККЛ) |
| Трастузумаб эмтанзин | Кадсила | Генентек , Рош | HER2-положительный метастатический рак молочной железы (мРМЖ) после лечения трастузумабом и майтансиноидом |
| Инотузумаб озогамицин | Besponsa | Пфайзер / Уайет | рецидивирующий или рефрактерный CD22-положительный предшественник В-клеток, острый лимфобластный лейкоз |
| Полатузумаб ведотин | Поливи | Генентек , Рош | рецидивирующая или рефрактерная диффузная крупноклеточная В-клеточная лимфома (DLBCL) [24] |
| Энфортумаб ведотин | водопад | Астеллас / Сиэтл Дженетикс | взрослые пациенты с местно-распространенным или метастатическим раком уротелия, получившие ингибитор PD-1 или PD-L1 и терапию, содержащую Pt [25] |
| Трастузумаб дерукстекан | Энхерт | AstraZeneca / Даичи Санкё | взрослые пациенты с неоперабельным или метастатическим HER2-положительным раком молочной железы, которые ранее получали две или более схемы лечения на основе анти-HER2 [26] |
| Сацитузумаб говитекан | Тродельви | Иммуномедицина | взрослые пациенты с метастатическим тройным негативным раком молочной железы (мТНРМЖ), которые ранее получали как минимум два курса терапии для пациентов с рецидивирующим или рефрактерным метастатическим заболеванием [27] |
| Белантамаб мафодотин | Бленреп | ГлаксоСмитКляйн | пациенты с множественной миеломой, у которых заболевание прогрессировало, несмотря на предшествующее лечение иммуномодулирующим средством, ингибитором протеасом и антителом против CD38 [28] |
| Моксетумомаб пасудотокс | Люмоксит | АстраЗенека | рецидивирующий или рефрактерный волосатоклеточный лейкоз (HCL) |
| Эффект лонкастуксимаба | Зинлонта | АЦП Терапевтика | рецидивирующая или рефрактерная крупноклеточная B-клеточная лимфома (включая диффузную крупноклеточную B-клеточную лимфому (DLBCL), не уточненную иначе, DLBCL, возникающую из лимфомы низкой степени злокачественности и B-клеточную лимфому высокой степени злокачественности) после двух или более линий системной терапии |
| Тисотумаб ведотин-тфтв | Тивдак | Seagen Inc. , Генмаб | взрослые пациенты с рецидивирующим или метастатическим раком шейки матки с прогрессированием заболевания во время или после химиотерапии [29] |
| Мирветуксимаб соравтанзин | Элахере | Иммуноген | лечение взрослых пациентов с фолатным рецептором альфа (FRα)-положительным, платинорезистентным эпителиальным раком яичников, фаллопиевых труб или первичным раком брюшины, которые ранее получали от одной до трех схем системного лечения |
Компоненты АЦП
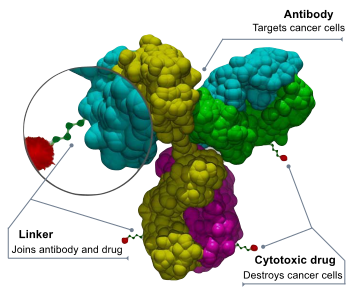
[ редактировать ]Конъюгат антитело-лекарственное средство состоит из трех компонентов: [30] [31]
- Антитела – нацелены на поверхность раковых клеток и могут также вызывать терапевтический ответ.
- Полезная нагрузка – вызывает желаемый терапевтический ответ.
- Линкер - прикрепляет полезную нагрузку к антителу и должен быть стабильным в обращении, высвобождая полезную нагрузку только в желаемой цели. Для прикрепления к антителу были разработаны и рассмотрены многочисленные подходы к конъюгации. [32] DAR представляет собой соотношение препарата и антитела и указывает уровень загрузки полезной нагрузки на ADC.
Полезная нагрузка
[ редактировать ]Многие полезные нагрузки для онкологических ADC (oADC) основаны на натуральных продуктах. [33] некоторые из них вступают в ковалентное взаимодействие со своей целью. [34] Полезные нагрузки включают ингибиторы микротубулина монометил ауристатин Е (MMAE), [35] монометил ауристатин F (MMAF) [36] и мертанзин , [37] ДНК-связывающий калихеамицин [38] и ингибиторы топоизомеразы 1 SN-38 [39] и экзатекан [40] что привело к возрождению полного синтеза натуральных продуктов. [41] Модуляторы глюкокортикоидных рецепторов (GRM) представляют собой наиболее активный класс полезной нагрузки для iADC. [ нужны разъяснения ] Подходы к выпуску на рынок молекул GRM, таких как дексаметазон. [42] [43] и будесонид [44] были разработаны. Модифицированные молекулы GRM [45] [46] Также были разработаны средства, позволяющие присоединять линкер с помощью термина ADCidified, описывающего медицинский химический процесс оптимизации полезной нагрузки для облегчения прикрепления линкера. [47] Альтернативы полезным нагрузкам малых молекул также были исследованы, например, siRNA . [48]
Линкеры
[ редактировать ]Стабильная связь между антителом и цитотоксическим (противораковым) агентом является важнейшим аспектом ADC. [49] Стабильный линкер ADC гарантирует, что меньшая часть цитотоксической нагрузки выпадет до того, как достигнет опухолевой клетки, что повышает безопасность и ограничивает дозы.
Линкеры основаны на химических мотивах, включая дисульфиды , гидразоны или пептиды (расщепляемые) или тиоэфиры (нерасщепляемые). В доклинических и клинических исследованиях была доказана безопасность расщепляемых и нерасщепляемых линкеров. Брентуксимаб ведотин включает чувствительный к ферментам расщепляемый линкер , который доставляет антимикротрубочковый агент монометил ауристатин Е или ММАЕ, синтетический противоопухолевый агент, к человеческим CD30-положительным злокачественным клеткам. ММАЭ ингибирует деление клеток, блокируя полимеризацию тубулина. Из-за своей высокой токсичности ММАЭ не может быть использован в качестве монотерапевтического химиотерапевтического препарата. Однако MMAE, связанный с моноклональным антителом против CD30 (cAC10, белком клеточной мембраны фактора некроза опухоли или рецептором TNF), был стабильным во внеклеточной жидкости. Он расщепляется катепсином и безопасен для терапии. Трастузумаб эмтанзин представляет собой комбинацию ингибитора образования микротрубочек мертанзина (DM-1) и антитела трастузумаба, в которой используется стабильный нерасщепляемый линкер .
Доступность лучших и более стабильных линкеров изменила функцию химической связи. Тип линкера, расщепляемый или нерасщепляемый , придает цитотоксическому препарату специфические свойства. Например, нерасщепляемый линкер удерживает лекарство внутри клетки. В результате все антитело, линкер и цитотоксический (противораковый) агент попадают в целевую раковую клетку, где антитело расщепляется до аминокислоты. Образующийся комплекс – аминокислота, линкер и цитотоксический агент – считается активным лекарственным средством. Напротив, расщепляемые линкеры отщепляются ферментами раковой клетки. Цитотоксическая полезная нагрузка может затем выйти из клетки-мишени и в процессе, называемом «убийством свидетеля», атаковать соседние клетки. [50]
Другой тип расщепляемого линкера, находящийся в настоящее время в разработке, добавляет дополнительную молекулу между цитотоксином и местом расщепления. Это позволяет исследователям создавать АЦП с большей гибкостью без изменения кинетики расщепления. Исследователи разрабатывают новый метод расщепления пептидов, основанный на деградации по Эдману — метод секвенирования аминокислот в пептиде. [51] Также в разработке находятся сайт-специфические конъюгации (TDC). [52] и новые методы конъюгации [53] [54] для дальнейшего улучшения стабильности и терапевтического индекса α-излучающих иммуноконъюгатов, [55] , конъюгированные с антителами наночастицы [56] и конъюгаты антитело-олигонуклеотиды . [57]
Любые конъюгаты лекарств
[ редактировать ]Поскольку сфера конъюгатов антитело-лекарственное средство стала более зрелой, более точным определением ADC теперь является конъюгат «что-нибудь-лекарственное средство». Альтернативы компоненту, нацеливающему антитела, теперь включают несколько более мелких фрагментов антител. [58] как диатела , [59] Потрясающе , [60] scFv , [61] и бициклические пептиды. [62]
Исследовать
[ редактировать ]Неприродные аминокислоты
[ редактировать ]В первом поколении используются технологии связывания, которые неселективно конъюгируют лекарства с остатками цистеина или лизина в антителе, что приводит к образованию гетерогенной смеси. Такой подход приводит к субоптимальной безопасности и эффективности и усложняет оптимизацию биологических, физических и фармакологических свойств. [52] Сайт-специфическое включение неприродных аминокислот создает сайт для контролируемого и стабильного прикрепления. Это позволяет производить гомогенные ADC, в которых антитело точно связано с лекарственным средством, и контролировать соотношение антител к лекарственному средству, что позволяет выбрать лучший в своем классе ADC. [52] Escherichia coli (OCFS) на основе Открытый бесклеточный синтез позволяет синтезировать белки, содержащие сайт-специфически включенные неприродные аминокислоты, и оптимизирован для предсказуемого высокопроизводительного синтеза и сворачивания белков. Отсутствие клеточной стенки позволяет добавлять в систему неприродные факторы для манипулирования транскрипцией, трансляцией и сворачиванием, обеспечивая точную модуляцию экспрессии белка. [63]
Другие области заболеваний
[ редактировать ]Большинство ADC, находящихся в разработке или клинических испытаниях, предназначены для онкологических и гематологических показаний. [64] Это в первую очередь обусловлено наличием моноклональных антител, нацеленных на различные виды рака. Однако некоторые разработчики стремятся распространить приложение на другие важные области заболеваний. [65] [66] [67]
См. также
[ редактировать ]Отраслевые конференции
[ редактировать ]- World ADC, Сан-Диего (ноябрь) – Самая продолжительная и самая всеобъемлющая в мире конференция по конъюгатам антител и лекарств.
- Всемирный ADC в Лондоне (март) — самое продолжительное и окончательное мероприятие по конъюгату антител и лекарств в Европе.
- World ADC Asia (июнь) – новаторские инновации и сотрудничество в разработке лекарств ADC в Азии
- Саммит ADC по линкерам и конъюгации (август) – внедрение инноваций в химию линкеров и технологии конъюгации
- Саммит конъюгатов нового поколения (февраль)
- Саммит аналитического развития ADC (апрель)
- Саммит ADC Payload (май)
- Саммит ADC по токсичности (июль)
- Саммит ADC по развитию процессов (сентябрь)
- Саммит ADC по фармакокинетике и клинической фармакологии (октябрь)
- Саммит ADC по выбору целей (декабрь)
Ссылки
[ редактировать ]- ^ Гамильтон GS (сентябрь 2015 г.). «Конъюгаты антитело-лекарство для терапии рака: технологические и нормативные проблемы разработки лекарственно-биологических гибридов» . Биологические препараты . 43 (5): 318–32. doi : 10.1016/j.biologicals.2015.05.006 . ПМИД 26115630 .
- ^ Перейти обратно: а б с Мацуяма К. (11 июня 2019 г.). «Препарат, заменяющий химиотерапию, может изменить подход к лечению рака» . БНН Блумберг . Проверено 14 июня 2019 г.
- ^ Фицпатрик-Даймонд ПФ (9 марта 2010 г.). «Конъюгаты антитело-лекарство возвращаются» . ОБЩ: Новости генной инженерии и биотехнологии .
- ^ ДиДжозеф Дж.Ф., Армеллино, Д.С., Богхарт Э.Р., Хандке К., Догер М.М., Шридхаран Л. и др. (март 2004 г.). «Направленная на антитела химиотерапия с CMC-544: CD22-нацеленный иммуноконъюгат калихеамицина для лечения B-лимфоидных злокачественных новообразований» . Кровь . 103 (5): 1807–14. дои : 10.1182/кровь-2003-07-2466 . ПМИД 14615373 . S2CID 17543492 .
- ^ Маллард А. (май 2013 г.). «Созревающий конвейер конъюгатов антитело-лекарственное средство достигает 30». Обзоры природы. Открытие наркотиков . 12 (5): 329–32. дои : 10.1038/nrd4009 . ПМИД 23629491 . S2CID 28757488 .
- ^ Чари Р.В., Мартелл Б.А., Гросс Дж.Л., Кук С.Б., Шах С.А., Блаттлер В.А. и др. (январь 1992 г.). «Иммуноконъюгаты, содержащие новые майтансиноиды: перспективные противораковые препараты». Исследования рака . 52 (1): 127–31. ПМИД 1727373 .
- ^ Коломбо Р., Джейми Р.Р. (ноябрь 2022 г.). «Терапевтическое окно конъюгатов антитело-лекарственное средство: догма, нуждающаяся в пересмотре» . Раковая клетка . 40 (11): 1255–1263. doi : 10.1016/j.ccell.2022.09.016 . ПМИД 36240779 .
- ^ Поллак А (31 мая 2012 г.). «Удар один-два» . Нью-Йорк Таймс .
- ^ «Перевозка лекарства в раковую клетку» . Нью-Йорк Таймс . 3 июня 2012 г.
- ^ «FDA: Pfizer добровольно отзывает препарат Mylotarg для лечения рака с рынка США» . Управление по контролю за продуктами и лекарствами США. Архивировано из оригинала 18 января 2017 г.
- ^ «Одобренные препараты > FDA одобрило гемтузумаб озогамицин для лечения CD33-положительного ОМЛ» . FDA.gov . Силвер-Спринг, США: Управление по контролю за продуктами и лекарствами США. 1 сентября 2017 года . Проверено 6 сентября 2017 г.
- ^ «Брентуксимаб ведотин (SGN35)]» . Обзор ADC/журнал конъюгатов антитело-лекарственное средство .
- ^ «FDA одобрило препарат Кадсила® (адо-трастузумаб эмтанзин) компании Genentech, первый конъюгат антитело-лекарственное средство для лечения Her2-положительного метастатического рака молочной железы» . Генентек. Архивировано из оригинала 17 июня 2019 г. Проверено 30 июня 2013 г.
- ^ «Адо-трастузумаб эмтанзин» . Министерство здравоохранения и социальных служб США, Национальные институты здравоохранения, Национальный институт рака.
- ^ «Инотузумаб озогамицин (описание препарата)» . Обзор ADC/журнал конъюгатов антитело-лекарственное средство .
- ^ «BESPONSA® одобрена в ЕС для взрослых пациентов с рецидивирующим или резистентным острым лимфобластным лейкозом-предшественником B-клеток» (пресс-релиз). 30 июня 2017 г.
- ^ «FDA США одобрило инотузумаб озогамицин для лечения пациентов с острым лимфобластным лейкозом, предшественником R/R B-клеток» . Обзор ADC/журнал конъюгатов антитело-лекарственное средство . 17 августа 2017 г.
- ^ Хобсон А.Д., Макферсон М.Дж., Хейс М.Э., Гесс С., Ли Х, Чжоу Дж., Ван З., Ю Ю, Ян Дж., Сунь Л., Чжан К., Цюй П., Ян С., Эрнандес А.младший, Брайант Ш., Матье С.Л., Бишофф АК, Фитцгиббонс Дж., Сантора Л.С., Ван Л., Ван Л., Феттис М.М., Ли Х, Марвин CC, Ван З., Патель М.В., Шмидт Д.Л., Ли Т., Рэндольф Дж.Т., Генри Р.Ф., Графф С., Тиан Ю., Агирре А.Л., Шреста А (декабрь 2022 г.). «Открытие ABBV-3373, конъюгата иммунологических антител и лекарственного средства, модулятора глюкокортикоидных рецепторов против TNF». Журнал медицинской химии . 65 (23): 15893–15934. doi : 10.1021/acs.jmedchem.2c01579 . ПМИД 36394224 .
- ^ Номер клинического исследования NCT03823391 «Исследование по оценке безопасности, переносимости, фармакокинетики и эффективности ABBV-3373 у участников с ревматоидным артритом от умеренной до тяжелой степени» на сайте ClinicalTrials.gov.
- ^ Хобсон А.Д., Сюй Дж., Марвин CC, Макферсон М.Дж., Холлманн М., Гаттнер М., Дзейк К., Феттис М.М., Бишофф А.К., Ван Л., Фитцгиббонс Дж., Ван Л., Саломон П., Эрнандес А.младший, Цзя Й., Сарвайя Х., Гесс Калифорния, Матье С.Л., Сантора LC (июль 2023 г.). «Оптимизация линкера лекарственного средства для обеспечения длительного хранения конъюгата антитело-лекарственное средство для подкожного дозирования». Журнал медицинской химии . 66 (13): 9161–9173. doi : 10.1021/acs.jmedchem.3c00794 . ПМИД 37379257 .
- ^ Хобсон А.Д., Сюй Дж., Уэлч Д.С., Марвин CC, Макферсон М.Дж., Гейтс Б., Ляо X, Холлманн М., Гаттнер М.Дж., Дзейк К., Сарвая Х., Шеной В.М., Феттис М.М., Бишофф А.К., Ван Л., Сантора Л.К., Ван Л. , Фитцгиббонс Дж., Саломон П., Эрнандес А.младший, Цзя Й., Гесс К.А., Матье С.Л., Брайант Ш., Ларсен М.Е., Куи Б., Тянь Ю. (сентябрь 2023 г.). «Открытие ABBV-154, конъюгата иммунологических антител и лекарственного средства, модулятора глюкокортикоидных рецепторов против TNF (iADC)». Журнал медицинской химии . 66 (17): 12544–12558. doi : 10.1021/acs.jmedchem.3c01174 . ПМИД 37656698 .
- ^ Номер клинического исследования NCT04888585 для «Исследования по оценке побочных эффектов и изменения активности заболевания у участников в возрасте от 18 до 75 лет, получавших подкожные (п/к) инъекции ABBV-154 при умеренной и тяжелой форме активного ревматоидного артрита (РА)» на сайте ClinicalTrials. .gov
- ^ «Объем рынка конъюгатов антител и лекарств, доля, тенденции, отчет об анализе роста, прикладная иммунотерапия, индустрия бизнес-возможностей, прогноз будущих тенденций на 2023 год |» . 24 сентября 2019 г.
- ^ Комиссар Управления (10.06.2019). «FDA одобрило первый режим химиоиммунотерапии для пациентов с рецидивирующей или рефрактерной диффузной крупноклеточной В-клеточной лимфомой» . FDA . Проверено 14 июня 2019 г.
- ^ «FDA выдает ускоренное одобрение энфортумабу ведотин-эйфв для лечения метастатического уротелиального рака» . FDA . 18 декабря 2019 г. Проверено 3 января 2020 г.
- ^ «FDA одобряет новый вариант лечения для пациентов с HER2-положительным раком молочной железы, у которых наблюдается прогресс при использовании доступных методов лечения» . FDA . 20 декабря 2019 г. Проверено 3 января 2020 г.
- ^ «FDA одобрило новый метод лечения тройного негативного рака молочной железы, который распространился и не ответил на другие методы лечения» . FDA . 22 апреля 2020 г. Проверено 24 апреля 2020 г.
- ^ «FDA выдало ускоренное одобрение белантамаба мафодотина-blmf для лечения множественной миеломы» . FDA . 06.08.2020 . Проверено 6 августа 2020 г.
- ^ «Seagen и Genmab объявляют об ускоренном одобрении FDA препарата TIVDAK™ (тисотумаб ведотин-тфтв) при ранее леченном рецидивирующем или метастатическом раке шейки матки» . Бизнесвайр .
- ^ Бек А., Гетч Л., Дюмонте С., Корвая Н. (март 2020 г.). «Достижения в разработке конъюгатов антитело-лекарственное средство: текущая клиническая ситуация и будущие инновации» . SLAS Дисков . 25 (8): 843–868. дои : 10.1177/2472555220912955 . ПМИД 28303026 . S2CID 214591000 .
- ^ Хонгорзул П., Линг С.Дж., Хан ФУ, Ихсан А.В., Чжан Дж. (январь 2020 г.). «Конъюгаты антитело-лекарственное средство: комплексный обзор». Мол Рак Рес . 18 (1): 3–19. дои : 10.1158/1541-7786.MCR-19-0582 . ПМИД 31659006 . S2CID 204952454 .
- ^ Кан М.С., Конг Т., Ху Дж., Ло Т.П. (октябрь 2021 г.). «Последние разработки в области стратегий химической конъюгации, нацеленных на нативные аминокислоты в белках, и их применение в конъюгатах антитело-лекарственное средство» . Химическая наука . 12 (41): 13613–13647. дои : 10.1039/D1SC02973H . ПМЦ 8549674 . ПМИД 34760149 . S2CID 240811966 .
- ^ Громек С.М., Балунас М.Ю. (2015). «Натуральные продукты как чрезвычайно мощные цитотоксические вещества для конъюгатов антитело-лекарственное средство». Curr Top Med Chem . 14 (24): 2822–2834. дои : 10.2174/1568026615666141208111253 . ПМИД 30879472 .
- ^ Васудеван А., Аргириади М.А., Баранчак А., Фридман М.М., Гаврилюк Дж., Хобсон А.Д., Халс Дж.Дж., Осман С., Уилсон Н.С. (март 2019 г.). «Глава первая. Ковалентные связующие в открытии лекарств». Прогресс Мед Хим . 58 (24): 2822–2834. дои : 10.1016/bs.pmch.2018.12.002 . ПМИД 25487009 . S2CID 81979586 .
- ^ Сентер П.Д., Сиверс Э.Л. (июль 2012 г.). «Открытие и разработка брентуксимаба ведотина для использования при рецидивирующей лимфоме Ходжкина и системной анапластической крупноклеточной лимфоме». Нат Биотехнология . 30 (7): 631–637. дои : 10.1038/nbt.2289 . ПМИД 22781692 . S2CID 5210967 .
- ^ Ван Б., Ву С., Чжун Ц., Лин Л., У З., Ю Б., Гао Х., Цзэн Х., Ян Д.Х. (ноябрь 2021 г.). «Белантамаб мафодотин для лечения множественной миеломы». Наркотики сегодня . 57 (11): 653–663. дои : 10.1358/точка.2021.57.11.3319146 . ПМИД 34821879 . S2CID 244418854 .
- ^ фон Минквиц Г, Хуанг К.С., Мано М.С., Лойбл С., Мамунас Э.П., Унч М., Вольмарк Н., Растоги П., Шнеевайс А., Редондо А., Фишер Х.Х., Жако В., Конлин А.К., Арсе-Салинас К., Вапнир И.Л., Джекиш К. , ДиДжованна М.П., Фашинг П.А., Краун Дж.П., Вюлфинг П., Шао З., Каремоли Э.Р., Ву Х., Лам Л.Х., Тесаровски Д., Смитт М., Даутвейт Х., Сингел С.М., Гейер-младший CE (февраль 2019 г.). «Трастузумаб эмтанзин при остаточном инвазивном HER2-положительном раке молочной железы» . N Engl J Med . 380 (7): 617–628. дои : 10.1056/NEJMoa1814017 . ПМИД 0516102 . S2CID 54524410 .
- ^ Годвин CD, Гейл Р.П., Уолтер Р.Б. (июнь 2017 г.). «Гемтузумаб озогамицин при остром миелолейкозе». Лейкемия . 31 (9): 1855–1868. дои : 10.1038/leu.2017.187 . ПМИД 28607471 . S2CID 33623791 .
- ^ [ PubMed ] Бардия А., Майер И.А., Вахдат Л.Т., Толани С.М., Исакофф С.Дж., Даймонд-младший, О'Шонесси Дж., Моруз Р.Л., Сантин А.Д., Абрамсон В.Г., Шах Н.К., Руго Х.С., Гольденберг Д.М., Свейдан А.М., Янноне Р., Вашковиц С., Шарки Р.М., Вегенер В.А., Калинский К. (февраль 2019 г.). «Сацитузумаб Говитекан при рефрактерном метастатическом трижды негативном раке молочной железы» . N Английский J Med 380 (8): 741–751. дои : 10.1056/NEJMoa1814213 . ПМИД 30786188 . S2CID 73489970 .
- ^ Огитани Ю, Аида Т, Хагихара К, Ямагути Дж, Исии С, Харада Н, Сома М, Окамото Х, Оитате М, Аракава С, Хираи Т, Ацуми Р, Накада Т, Хаякава И, Абэ Ю, Агацума Т (октябрь 2016 г.) ). «DS-8201a, новый ADC, нацеленный на HER2, с новым ингибитором ДНК-топоизомеразы I, демонстрирует многообещающую противоопухолевую эффективность с дифференцировкой от T-DM1» . Клин Рак Рес . 22 (20): 5097–5108. дои : 10.1158/1078-0432.CCR-15-2822 . ПМИД 27026201 . S2CID 12462981 .
- ^ Николау К.С., Ригол С. (август 2019 г.). «Роль органического синтеза в появлении и развитии конъюгатов антитело-лекарственное средство в качестве таргетной терапии рака». Angew Chem Int Ed Engl . 58 (33): 11206–11241. дои : 10.1002/anie.201903498 . ПМИД 31012193 . S2CID 128362562 .
- ^ Граверсен Дж. Х., Свендсен П., Дагнес-Хансен Ф., Даль Дж., Антон Г., Эцеродт А., Петерсен М.Д., Кристенсен П.А., Мёллер Х.Дж., Моэструп С.К. (август 2012 г.). «Нацеливание на рецептор-поглотитель гемоглобина CD163 в макрофагах значительно увеличивает противовоспалительную эффективность дексаметазона» . Мол Тер . 20 (8): 1550–1558. дои : 10.1038/mt.2012.103 . ПМЦ 3412497 . ПМИД 22643864 . S2CID 17457555 .
- ^ Свендсен П., Граверсен Дж.Х., Эцеродт А., Хагер Х., Рёге Р., Грёнбек Х., Кристенсен Э.И., Мёллер Х.Дж., Вилструп Х., Моэструп С.К. (март 2017 г.). «Направленное антителами глюкокортикоидное воздействие на CD163 в макрофагах типа М2 ослабляет воспалительные изменения печени, вызванные фруктозой» . Мол Тер Методы Клин Дев . 4 : 50–61. дои : 10.1016/j.omtm.2016.11.004 . ПМЦ 5363319 . ПМИД 28344991 . S2CID 18592917 .
- ^ Керн Дж.К., Дуни Д., Чжан Р., Лян Л., Брандиш П.Е., Ченг М., Фэн Дж., Бек А., Брессон Д., Фирдос Дж., Гейтли Д., Кнудсен Н., Манибусан А., Сунь Ю., Гарбаччо Р.М. (сентябрь 2016 г.). «Новые фосфат-модифицированные линкеры катепсина B: улучшение растворимости в воде и расширение области полезной нагрузки ADC». Биоконъюг Хим . 27 (9): 2081–2088. doi : 10.1021/acs.bioconjchem.6b00337 . ПМИД 27469406 .
- ^ Брандиш П.Е., Палмиери А., Антоненко С., Бомонт М., Бенсо Л., Канцлер М., Ченг М., Фаядат-Дилман Л., Фэн Г., Фигероа И., Фирдос Дж., Гарбаччо Р., Гарвин-Куин Л., Гейтли Д., Геда П., Хейнс. Хсей С., Ходжес Д., Керн Дж., Кнудсен Н., Кваснюк К., Лян Л., Ма Х., Манибусан А., Миллер П.Л., Мой Л.И., Ку Ю., Шах С., Шин Дж.С., Стиверс П., Сан Ю., Томазела Д., Ву ХК. , Заллер Д., Чжан С., Чжан Ю., Зильсторфф М. (июль 2018 г.). «Разработка конъюгатов антитело-лекарственное средство против CD74 для нацеливания глюкокортикоидов на иммунные клетки». Биоконъюг Хим . 29 (7): 2357–2369. doi : 10.1021/acs.bioconjchem.8b00312 . ПМИД 29923706 . S2CID 49310298 .
- ^ Хан А., Олсен О., Д'Суза С., Шан Дж., Чжао Ф., Янолатос Дж., Оганесян З., Хаджинасто С., Дельфино Ф., Олсон В. (август 2021 г.). «Разработка новых глюкокортикоидов для использования в конъюгатах антитело-лекарственное средство для лечения воспалительных заболеваний». J Med Chem . 64 (16): 11958–11971. doi : 10.1021/acs.jmedchem.1c00541 . ПМИД 34378927 . S2CID 236976999 .
- ^ Хобсон А.Д., Макферсон М.Дж., Вегелл В., Гесс К.А., Стоффель Р.Х., Ли Х, Чжоу Дж., Ван З., Ю Ю, Эрнандес-младший А., Брайант Ш., Матье С.Л., Бишофф А.К., Фитцгиббонс Дж., Павликовска М., Путенвитил С., Сантора LC, Ван Л., Ван Л., Марвин CC, Хейс М.Э., Шреста А., Саррис К.А., Ли Б (февраль 2022 г.). «Проектирование и разработка агонистов модулятора глюкокортикоидных рецепторов в качестве полезной нагрузки иммунологического конъюгата антитело-лекарственное средство (iADC)». J Med Chem . 65 (6): 4500–4533. doi : 10.1021/acs.jmedchem.1c02099 . ПМИД 35133822 . S2CID 246679075 .
- ^ Яриан Ф., Алибахши А., Эйвази С., Арезуманд Р., Ахангарзаде С. (август 2019 г.). «Терапевтические конъюгаты антитело-лекарственное средство: потенциал антитело-миРНК в терапии рака». J Клеточная Физиол . 234 (10): 16724–16738. дои : 10.1002/jcp.28490 . ПМИД 30908646 . S2CID 85515264 .
- ^ Бек А., Гетч Л., Дюмонте С., Корвая Н. (май 2017 г.). «Стратегии и проблемы для следующего поколения конъюгатов антител и лекарств». Обзоры природы. Открытие наркотиков . 16 (5): 315–337. дои : 10.1038/nrd.2016.268 . ПМИД 28303026 . S2CID 22045270 .
- ^ Ковтун Ю.В., Гольдмахер В.С. (октябрь 2007 г.). «Уничтожение клеток конъюгатами антитело-лекарственное средство». Письма о раке . 255 (2): 232–40. дои : 10.1016/j.canlet.2007.04.010 . ПМИД 17553616 .
- ^ Бончор Р., Ключик А., Стефанович П., Шевчук З. (август 2013 г.). «Новый метод расщепления пептидов, основанный на деградации по Эдману» . Молекулярное разнообразие . 17 (3): 605–11. дои : 10.1007/s11030-013-9453-y . ПМЦ 3713267 . ПМИД 23690169 .
- ^ Перейти обратно: а б с Аксап Дж.Ю., Баджжури К.М., Ритланд М., Хатчинс Б.М., Ким Ч.Х., Казане С.А. и др. (октябрь 2012 г.). «Синтез сайт-специфических конъюгатов антитело-лекарственное средство с использованием неприродных аминокислот» . Труды Национальной академии наук Соединенных Штатов Америки . 109 (40): 16101–6. Бибкод : 2012PNAS..10916101A . дои : 10.1073/pnas.1211023109 . ПМЦ 3479532 . ПМИД 22988081 .
- ^ Лион Р.П., Сеттер Дж.Р., Бови Т.Д., Доронина С.О., Хантер Дж.Х., Андерсон М.Е. и др. (октябрь 2014 г.). «Самогидролизующиеся малеимиды улучшают стабильность и фармакологические свойства конъюгатов антитело-лекарственное средство». Природная биотехнология . 32 (10): 1059–62. дои : 10.1038/nbt.2968 . ПМИД 25194818 . S2CID 5415162 .
- ^ Колодыч С., Коньев О., Баатархуу З., Боннефой Дж.Ю., Дебаен Ф., Чианферани С. и др. (февраль 2015 г.). «CBTF: новый реагент связывания амина с тиолом для приготовления конъюгатов антител с повышенной стабильностью в плазме». Биоконъюгатная химия . 26 (2): 197–200. дои : 10.1021/bc500610g . ПМИД 25614935 .
- ^ Вулбранд С, Зайдль С, Гертнер ФК, Брюхертсайфер Ф, Моргенштерн А, Эсслер М, Сенекович-Шмидтке Р (2013). Мультхофф Дж. (ред.). «Иммуноконъюгаты 213Bi-анти-EGFR, испускающие альфа-частицы, уничтожают опухолевые клетки независимо от оксигенации» . ПЛОС ОДИН . 8 (5): е64730. Бибкод : 2013PLoSO...864730W . дои : 10.1371/journal.pone.0064730 . ПМЦ 3665541 . ПМИД 23724085 .
- ^ Кардосо М.М., Песа И.Н., Роке АС (2012). «Конъюгированные с антителами наночастицы для терапевтического применения». Современная медицинская химия . 19 (19): 3103–27. дои : 10.2174/092986712800784667 . hdl : 10362/20689 . ПМИД 22612698 . S2CID 38141058 .
- ^ Довгань И., Коньев О., Колодич С., Вагнер А. (октябрь 2019 г.). «Конъюгаты антитело-олигонуклеотид как терапевтические средства, средства визуализации и обнаружения». Биоконъюгатная химия . 30 (10): 2483–2501. doi : 10.1021/acs.bioconjchem.9b00306 . ПМИД 31339691 . S2CID 198491258 .
- ^ Деонарайн, член парламента, Яхиоглу Г (июнь 2021 г.). «Текущие стратегии открытия и биоконъюгации более мелких целевых конъюгатов лекарств, предназначенных для терапии солидных опухолей». Экспертное мнение о лекарствах . 16 (6): 613–624. дои : 10.1080/17460441.2021.1858050 . ПМИД 33275475 . S2CID 227297067 .
- ^ Ли Кью, Барретт А, Виджаякришнан Б, Тибергиен А, Берд Р, Рикерт К.В., Аллен К.Л., Кристи Р.Дж., Марелли М., Харпер Дж., Ховард П., Ву Х, Далл'Аква В.Ф., Цуй П., Гао С., Боррок М.Дж. ( апрель 2019). «Улучшенное ингибирование роста опухоли конъюгатами диантило-лекарственное средство посредством продления периода полувыведения». Биоконъюг Хим . 30 (4): 1232–1243. doi : 10.1021/acs.bioconjchem.9b00170 . ПМИД 30912649 . S2CID 85517465 .
- ^ Хван Д., Рейдер С. (май 2020 г.). «Сайт-специфические конъюгаты антитело-лекарственное средство в формате Fab с тройным вариабельным доменом» . Биомолекулы . 10 (5): 764. doi : 10.3390/biom10050764 . ПМК 7278019 . ПМИД 32422893 .
- ^ Обри Н., Аллард-Ваннье Э., Мартин С., Брайден Ф., Летаст С., Колас С., Лахриф З., Коллине Н., Димье-Пуассон I, Чурпа I, Вио-Массюар М.К., Жубер Н. (ноябрь 2018 г.). «Сайт-специфическая конъюгация ауристатинов с сконструированным scFv с использованием малеимида второго поколения для воздействия на HER2-положительный рак молочной железы in vitro». Биоконъюг Хим . 29 (11): 3516–3521. doi : 10.1021/acs.bioconjchem.8b00668 . ПМИД 30352511 . S2CID 53027552 .
- ^ Хуров К, Лахденранта Дж, Упадхьяя П, Хейнс Э, Коэн Х, Репаш Е, Канакия Д, Ма Дж, Кристенссон Дж, Ю Ф, Кэмпбелл С, Уитти Д, Келли М, Блейкмор С, Джеффри П, МакДоннелл К, Брандиш П , Кин Н. (ноябрь 2021 г.). «BT7480, новый полностью синтетический агонист иммунных клеток Bicycle, нацеленный на опухоли (Bicycle TICA™), индуцирует локализованный в опухоли агонизм CD137» . J Иммунный рак . 9 (11): e002883. doi : 10.1136/jitc-2021-002883 . ПМЦ 8562524 . ПМИД 34725211 . S2CID 240422681 .
- ^ Завада Дж. Ф., Инь Г., Штайнер А.Р., Ян Дж., Нареш А., Рой С.М. и др. (июль 2011 г.). «Наращивание производства бесклеточных цитокинов от микромасштаба до производства — новый подход к сокращению сроков разработки производства белка» . Биотехнология и биоинженерия . 108 (7): 1570–8. дои : 10.1002/бит.23103 . ПМК 3128707 . ПМИД 21337337 .
- ^ Flygare JA, Pillow TH, Aristoff P (январь 2013 г.). «Конъюгаты антитело-лекарственное средство для лечения рака». Химическая биология и дизайн лекарств . 81 (1): 113–21. дои : 10.1111/cbdd.12085 . ПМИД 23253133 . S2CID 20523083 .
- ^ Лехар С.М., Пиллоу Т., Сюй М., Стабен Л., Кадзихара К.К., Вандлен Р. и др. (ноябрь 2015 г.). «Новый конъюгат антитело-антибиотик уничтожает внутриклеточный S. aureus». Природа . 527 (7578): 323–8. Бибкод : 2015Natur.527..323L . дои : 10.1038/nature16057 . ПМИД 26536114 . S2CID 205246581 .
- ^ «Ambrx сотрудничает с Merck для проектирования и разработки конъюгатов биологических лекарств» . Архивировано из оригинала (пресс-релиз) 7 января 2013 г.
- ^ Макферсон М.Дж., Хобсон А.Д. (2020). «Расширяя границы: развитие АЦП за пределами онкологии». Конъюгаты антитело-лекарственное средство . Методы Мол Биол. Том. 2078. стр. 23–36. дои : 10.1007/978-1-4939-9929-3_2 . ISBN 978-1-4939-9928-6 . ПМИД 31643047 . S2CID 204849993 .