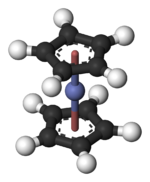
Кобальтоцен
| |||
| Имена | |||
|---|---|---|---|
| ИЮПАК имена Кобальтоцен Бис ( н 5 -циклопентадиенил)кобальт | |||
| Другие имена КП 2 Ко | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| КЭБ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.013.692 | ||
| Номер ЕС |
| ||
ПабХим CID | |||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| [Co( η 5 -С 5 Н 5 ) 2 ] | |||
| Молярная масса | 189.12 g/mol | ||
| Появление | Тёмно-фиолетовый сплошной | ||
| Температура плавления | 171–173 ° C (340–343 ° F; 444–446 К) | ||
| нерастворимый | |||
| Структура | |||
| бутерброд | |||
| ноль | |||
| Термохимия | |||
Стандартный моляр энтропия ( S ⦵ 298 ) | 236 г. до н.э. −1 моль −1 | ||
Стандартная энтальпия образование (Δ f H ⦵ 298 ) | +237 кДж/моль (неопределенно) | ||
Стандартная энтальпия горение (Δ c H ⦵ 298 ) | −5839 кДж/моль | ||
| Опасности | |||
| СГС Маркировка : | |||
  [1] [1] | |||
| Опасность [1] | |||
| Х228 , Х317 , Х351 [1] | |||
| П210 , П261 , П280 , П363 , П405 , П501 [1] | |||
| NFPA 704 (огненный алмаз) | |||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности | ||
| Родственные соединения | |||
Родственные металлоцены | Ферроцен никелоцен Родоцен | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Кобальтоцен , известный также как бис(циклопентадиенил)кобальт(II) или даже «бис-Cp-кобальт», представляет собой кобальторганическое соединение с формулой Co(C 5 H 5 ) 2 . Это темно-фиолетовое твердое вещество, которое легко сублимируется при температуре немного выше комнатной. Кобальтоцен был открыт вскоре после ферроцена , первого металлоцена . Из-за легкости реакции с кислородом соединение необходимо хранить и использовать без доступа воздуха .
Синтез
[ редактировать ]
Кобальтоцен получают реакцией циклопентадиенида натрия (NaC 5 H 5 ) с безводным хлоридом кобальта(II) в ТГФ растворе . Хлорид натрия когенерируют, а металлоорганический продукт обычно очищают вакуумной сублимацией . [2]
Структура и связь
[ редактировать ]В Co(C 5 H 5 ) 2 центр Co «зажат» между двумя циклопентадиенильными (Cp) кольцами. Длина связи Co–C составляет около 2,1 Å, что немного больше, чем связь Fe–C в ферроцене. [3]
Co(C 5 H 5 ) 2 принадлежит к группе металлоорганических соединений, называемых металлоценами или сэндвич-соединениями. [4] Кобальтоцен имеет 19 валентных электронов, что на один больше, чем обычно встречается в комплексах органопереходных металлов, таких как его очень стабильный родственник ферроцен. (См. правило 18 электронов .) Этот дополнительный электрон занимает орбиталь, которая является разрыхляющей по отношению к связям Co–C. Следовательно, расстояния Co–C несколько длиннее, чем связи Fe–C в ферроцене. Многие химические реакции Co(C 5 H 5 ) 2 характеризуются тенденцией терять этот «лишний» электрон, образуя 18-электронный катион, известный как кобальтоцений:
, близкий родственник кобальтоцена, Родоцен не существует в виде мономера, но спонтанно димеризуется за счет образования связи C–C между кольцами Cp.
Реакции
[ редактировать ]Редокс-свойства
[ редактировать ]Co(C 5 H 5 ) 2 является распространенным одноэлектронным восстановителем в лабораторных условиях. [5] Фактически, обратимость пары Co(C 5 H 5 ) 2 окислительно-восстановительной настолько хороша, что Co(C 5 H 5 ) 2 можно использовать в циклической вольтамперометрии в качестве внутреннего стандарта . Его перметилированный аналог декаметилкобальтоцен (Co(C 5 Me 5 ) 2 ) является особенно мощным восстановителем из-за индуктивного отдачи электронной плотности от 10 метильных групп, побуждая кобальт тем более отдавать свой «лишний» электрон. Эти два соединения являются редкими примерами восстановителей, растворяющихся в неполярных органических растворителях. Ниже приведены потенциалы восстановления этих соединений с использованием пары ферроцен- ферроцений в качестве эталона:
| Полуреакция | И 0 (V) |
|---|---|
| Fe(C 55Ч 5 ) + 2+ и − ⇌ Fe(C 5 H 5 ) 2 | 0,00 (по определению) |
| Fe(C 5 меня 5 ) + 2+ и − ⇌ Fe(C 5 Me 5 ) 2 | −0.59 |
| Что(С 55Ч 5 ) + 2+ и − ⇌ Со(С 5 Н 5 ) 2 | −1.33 |
| Что(С 5 меня 5 ) + 2+ и − ⇌ Co(C 5 Me 5 ) 2 | −1.94 |
Данные показывают, что декаметиловые соединения примерно на 600 мВ более восстанавливающие, чем исходные металлоцены. Однако этот эффект заместителя затмевается влиянием металла: переход от Fe к Co делает восстановление более благоприятным более чем на 1,3 вольта.
Карбонилирование
[ редактировать ]Обработка Co(C 5 H 5 ) 2 окисью углерода дает производное кобальта(I) Co(C 5 H 5 )(CO) 2 , что сопровождается потерей одного Cp-лиганда. Это преобразование проводится при температуре около 130 ° C и давлении CO 500 фунтов на квадратный дюйм. [2] [6]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д «Бис(циклопентадиенил)кобальт(II)» . Американские элементы . Проверено 24 августа 2018 г.
- ^ Jump up to: а б Кинг, РБ (1965). Металлоорганические синтезы . Том. 1. Нью-Йорк, штат Нью-Йорк: Академик Пресс.
- ^ Антипин М. Ю.; Бозе, Р.; Аугарт, Н.; Шмид, Г. (1993). «Переопределение кристаллической структуры кобальтоцена при 100 К и 297 К: сравнение с ферроценом и никельоценом». Структура. хим. 4 (2): 91–101. дои : 10.1007/BF00677370 . S2CID 93871667 .
- ^ Эльшенбройх, К.; Зальцер, А. (1992). Металлоорганические соединения: краткое введение (2-е изд.). Вайнхайм: Wiley-VCH. ISBN 978-3-527-28165-7 .
- ^ Коннелли, Нью-Йорк; Гейгер, МЫ (1996). «Химические окислительно-восстановительные агенты для металлоорганической химии». хим. Откр. 96 (2): 877–910. дои : 10.1021/cr940053x . ПМИД 11848774 .
- ^ Кинг, РБ; Стоун, FGA (1967). Циклопентадиенил-металлкарбонилы и некоторые производные . Неорганические синтезы. Том. 7. С. 99–115. дои : 10.1002/9780470132388.ch31 . ISBN 9780470132388 .