Энантиомер
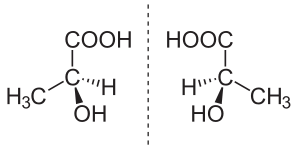
Он укреплял , и Эйнда Майна ( / / Nod. [ 1 ] ih-nan-wee-m Мар ; Из древнегреческого экземпляра (Enantíos) «противоположный» и часть (méros) «часть») - также называется оптическим изомером , [ 2 ] Антипод , [ 3 ] или оптический антипод [ 4 ] - один из двух стереоизомеров , которые не подлежат подставке для их собственного зеркального изображения . Энантиомеры друг друга очень похожи на правых и левых рук; Без зеркалирования одного из них, руки не могут быть суперпозированы друг на друга. [ 5 ] Это исключительно взаимосвязь хиральности и постоянных трехмерных отношений между молекулами или другими химическими структурами: никакое количество переориентации молекулы в целом или конформационном изменении превращает одно химическое вещество в его энантиомер. Химические структуры с хиральностью вращаются плоскополярным светом. [ 6 ] Смесь равного количества каждого энантиомера, раковой смеси или ракемного рода не вращается. [ 7 ] [ 8 ] [ 9 ]
Стереоизомеры включают как энантиомеры, так и диастереомеры . Диастереомеры, такие как энантиомеры, имеют одну и ту же молекулярную формулу и также не подлежат подставки друг к другу; Однако они не являются зеркальными изображениями друг друга. [ 10 ]
Наименование соглашений
[ редактировать ]Существует три общих соглашения об именах для определения одного из двух энантиомеров ( абсолютная конфигурация ) данной хиральной молекулы: система R/S основана на геометрии молекулы; (+) - и ( -) - система (также написанная с использованием устаревших эквивалентов D - и L -) основана на ее оптического вращения свойствах ; и система D / L основана на отношениях молекулы с энантиомерами глицеральдегида .
Система R/S основана на геометрии молекулы относительно хирального центра. [ 11 ] Система R/S присваивается молекуле, основанной на правилах приоритета, назначенных правилами приоритета CAHN -Engold -ProLog , в которых группе или атом с наибольшим атомным числом присваивается самый высокий приоритет, а группа или атом с наименьшим атомным Число назначается самым низким приоритетом.
молекулы (+) Или ( -) символ используется для указания оптического вращения - направления, в котором поляризация света вращается при прохождении через раствор, содержащий молекулу. [ 12 ] Когда молекула обозначена декстроротационной, она вращает плоскость поляризованного света по часовой стрелке, а также может быть обозначена как (+). [ 11 ] Когда он обозначается как леворатор, он вращает плоскость поляризованного света против часовой стрелки, а также может быть обозначена как ( -). [ 11 ]
Латинские слова для левых являются Laevus и зловещим , а слово для справа - Dexter (или прямая кишка в смысле правильного или добродетельного). Английское слово «право» - это родственная кишка прямая . Это происхождение обозначений D/L и R/S, а также занятость префиксов Levo- и Dexstro- в общих именах .
Префикс AR- , из латинского ректо (справа), применяется к правой версии; es- , от латинской зловещей (слева), до левшей молекулы. Пример: кетамин , аркетамина , эскетамина . [ 13 ]
Хиральности центры
[ редактировать ]
Асимметричный атом называется центром хиральности , [ 14 ] [ 15 ] тип стереоцентра . Центр хиральности также называется хиральным центром [ 16 ] [ 17 ] [ 18 ] или асимметричный центр . [ 19 ] Некоторые источники используют термины стереоцентра , стереогенный центр , стереогенный атом или стереоген, чтобы относиться исключительно в центр хиральности, [ 16 ] [ 18 ] [ 20 ] в то время как другие используют термины более широко для ссылки на центры, которые приводят к диастереомерам (стереоизомеры, которые не являются энантиомерами). [ 15 ] [ 21 ] [ 22 ]
Соединения, которые содержат ровно одно (или любое нечетное число) асимметричных атомов, всегда являются хиральными. Тем не менее, в соединениях, которые содержат равномерное количество асимметричных атомов, иногда не хватает хиральности, потому что они расположены в зеркальных симметричных парах и известны как мезо соединения . Например, мезо татарная кислота (показанная справа) имеет два асимметричных атома углерода, но она не демонстрирует энантиомеризм, потому что существует плоскость зеркальной симметрии. И наоборот, существуют формы хиральности, которые не требуют асимметричных атомов, таких как осевая , плоская и спиральная хиральность. [ 16 ] : pg. 3
Несмотря на то, что хиральная молекула не имеет отражения (C S ) и роторефекции симметрии (S 2 N ), она может иметь другие молекулярные симметрии , и ее симметрия описывается одной из хиральных точечных групп : C N , D N , T, O, или I. Например, перекись водорода является хиральной и имеет симметрию C 2 (двойной вращение). Общим хиральным случаем является точечная группа C 1 , что означает отсутствие симметрии, что относится к молочной кислоте.
Примеры
[ редактировать ]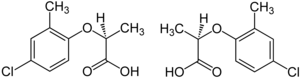

Примером такого энантиомера является седативный талидомид , который был продан в ряде стран мира с 1957 по 1961 год. Он был отозван с рынка, когда было обнаружено, что он вызывает врожденные дефекты. Один энантиомер вызвал желательные седативные эффекты, а другой - неизбежно [ 23 ] присутствует в равных количествах, вызвало врожденные дефекты. [ 24 ]
Гербицидный )-(+) - мекопроп является рацемической смесью, с ( r энантиомер («mecoprop-p», «Дуплозан КВ») обладает гербицидной активностью. [ 25 ]
Другим примером являются антидепрессантные препараты эсциталопрам и циталопрам . Циталопрам является ракемейной смесью [1: 1 ( S ) -циталопрам и ( R ) -циталопрам]; Эсциталопрам [( S ) -Citalopram] является чистым энантиомером. Дозировки для эсциталопрама, как правило, 1/2 из -за циталопрама. Здесь (S) -Citalopram называется хиральным переключением циталопрама.
Хиральные препараты
[ редактировать ]Соединения Enantiopure состоят только из одного из двух энантиомеров. Enantiopurity имеет практическое значение, поскольку такие композиции имеют повышенную терапевтическую эффективность. [ 26 ] Переход от рацемического препарата на препарат по энантиопу, называется хиральным переключателем . Во многих случаях энантиомеры имеют четкий эффект. Один случай - это пропоксифен. Энантиомерная пара пропоксифена отдельно продается Эли Лилли и Компанией. Одним из партнеров является декстропропсифен , анальгетический агент (DARVON), а другой называется левопропоксифеном , эффективным противополучительным (Novrad). [ 27 ] [ 28 ] Интересно отметить, что торговые названия лекарств, Darvon и Novrad, также отражают отношения химического зеркала. В других случаях не может быть никакой клинической пользы для пациента. В некоторых юрисдикциях односетиомерные препараты отдельно патентоспособны из раковой смеси. [ 29 ] Возможно, что только один из энантиомеров активен. Или может случиться так, что оба являются активными, и в этом случае разделение смеси не имеет объективных преимуществ, но расширяет патентоспособность препарата. [ 30 ]
Энантиоселективные препараты
[ редактировать ]При отсутствии эффективной энантиомерной среды ( предшественник , хиральный катализатор или кинетическое разрешение ) разделение расической смеси на энантиомерные компоненты невозможно, хотя некоторые рационы смеси спонтанно кристаллизуются в форме рационического конгломерата , в которых кристаллы Энантиомеры физически сегрегируются и могут быть разделены механически. Тем не менее, большинство Racemates образуют кристаллы, содержащие обоих энантиомеров в соотношении 1: 1.
В своей новаторской работе Луи Пастер смог изолировать изомеры тартрата аммония натрия, потому что отдельные энантиомеры кристаллизуются отдельно от раствора. Безусловно, образуются равные количества энантиоморфных кристаллов, но два вида кристаллов могут быть разделены с помощью пинцета. Такое поведение необычно. Менее распространенный метод- энантиомерная самоопровозглашение .
Вторая стратегия - асимметричный синтез: использование различных методов для приготовления желаемого соединения при высоком энантиомерном избытках . Методы включают в себя использование хиральных стартовых материалов ( синтез хирального бассейна ), использование хиральных вспомогательных средств и хиральных катализаторов и применение асимметричной индукции . Использование ферментов ( биокатализа ) также может производить желаемое соединение.
Третья стратегия - это энантиоконвергентный синтез , синтез одного энантиомера из рацемического предшественника, используя обоих энантиомеров. Используя хиральный катализ, оба энантиомеры реагента приводят к одному энантиомеру продукта. [ 31 ]
Энантиомеры могут не быть изолированными, если есть доступный путь для рацизма (взаимосвязь между энантиоморфами с получением расической смеси) при заданной температуре и временной шкале. Например, амины с тремя различными заместителями являются хиральными, но, за небольшим количеством исключений (например, заменить n -интерлоазиридины), они быстро подвергаются « инверсии зонтика » при комнатной температуре, что приводит к рационированию. Если рацизация достаточно быстрая, молекула часто можно рассматривать как ахиральную, усредненную структуру.
Нарушение паритета
[ редактировать ]Для всех намерений и целей каждый энантиомер в паре имеет одинаковую энергию. Однако теоретическая физика предсказывает, что из -за нарушения паритета слабой ядерной силы (единственная сила в природе, которая может «рассказать слева справа»), на самом деле существует минутная разница в энергии между энантиомерами (по порядку 10 −12 EV или 10 −10 KJ/MOL или меньше) из -за слабый механизм нейтрального тока . Эта разница в энергии намного меньше, чем изменения энергии, вызванные даже небольшими изменениями в молекулярной конформации, и слишком мала, чтобы измерить текущую технологию, и, следовательно, химически несущественно. [ 17 ] [ 32 ] [ 33 ] В том смысле, используемом физиками частиц, «истинный» энантиомер молекулы, которая имеет точно такое же содержание массовой энергии, как и оригинальная молекула, является зеркальным изображением, которое также построено из антипротечки (антипротоны, антинейтроны и позитроны)) Полем [ 17 ] На протяжении всей этой статьи «Enantiomer» используется только в химическом смысле соединений обычного вещества, которые не являются сверхпозируемыми на их зеркальном изображении.
Квази -дельомеры
[ редактировать ]Quasi -Enantiomers -это молекулярные виды, которые не являются строго энантиомерами, но ведут себя так, как будто они есть. В квази -детандиомерах большинство молекулы отражается; Однако атом или группа в молекуле изменяется на аналогичный атом или группу. [ 34 ] Quasi -Enantiomers также могут быть определены как молекулы, которые могут стать энантиомерами, если заменен атом или группа в молекуле. [ 35 ] Примером квази -дельомеров будут ( ы ) -Bromobutane и ( r ) -iodobutane. В нормальных условиях энантиомеры для ( s ) -Bromobutane и ( r ) -iodobutane будут ( r) -Bromobutane и ( s ) -iodobutane соответственно. Квази -детантиомеры также будут производить квази -ракемы, которые похожи на обычные ракемы (см. Раковую смесь ) в том смысле, что они образуют равную смесь квазинтиомеров . [ 34 ]
Хотя это не считается фактическими энантиомерами, соглашение об именах для квазинтиомеров также следует той же тенденции, что и энантиомеры при рассмотрении ( R ) и ( S ) конфигурации, которые рассматриваются на геометрической основе (см. Правила приоритета CAHN -Engold -PRELOG ).
Quasi -Enantiomers имеют применение в параллельном кинетическом разрешении . [ 36 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ «Enantiomer: определение и значение» . Dictionary.com . Получено 2024-04-26 .
- ^ Химия (IUPAC), Международный союз чистого и применения. «Iupac - оптические изомеры (O04308)» . Goldbook.iupac.org . doi : 10.1351/goldbook.o04308 . Получено 2022-11-17 .
- ^ Химия (IUPAC), Международный союз чистого и применения. «Iupac - антиподы (A00403)» . Goldbook.iupac.org . doi : 10.1351/goldbook.a00403 . Получено 2022-11-17 .
- ^ Химия (IUPAC), Международный союз чистого и применения. «IUPAC - Оптические антиподы (O04304)» . Goldbook.iupac.org . doi : 10.1351/goldbook.o04304 . Получено 2022-11-17 .
- ^ МакКонати, Джонатан; Оуэнс, Майкл Дж. (2003). «Стереохимия в действиях наркотиков» . Первичная помощь в журнале клинической психиатрии . 5 (2): 70–73. doi : 10.4088/pcc.v05n0202 . ISSN 1523-5998 . PMC 353039 . PMID 15156233 .
- ^ «Хиральность и оптическая деятельность» . Chemed.chem.purdue.edu . Получено 2022-11-17 .
- ^ Химия (IUPAC), Международный союз чистого и применения. "Iupac - раством (R05026)" . Goldbook.iupac.org . doi : 10.1351/goldbook.r05026 . Получено 2022-11-17 .
- ^ Химия (IUPAC), Международный союз чистого и применения. "Iupac - Racemate (R05025)" . Goldbook.iupac.org . doi : 10.1351/goldbook.r05025 . Получено 2022-11-17 .
- ^ Вебер, Эрин. «Руководство библиотеки: Chem 221: стереохимия / изомеризм» . LibraryGuides.Salisbury.edu . Получено 2022-11-17 .
- ^ Смит, Майкл Б.; Март, Джерри (2007), Advanced Organic Chemistry: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Jump up to: а беременный в Брюстер, Джеймс Х. (декабрь 1986 г.). «Различие диастереомеров в нотации Cahn-ingold-Prelog (RS)» . Журнал органической химии . 51 (25): 4751–4753. doi : 10.1021/jo00375a001 . ISSN 0022-3263 .
- ^ Колдуэлл, Джон; Wainer, Irving W. (декабрь 2001 г.). «Стереохимия: определения и заметка о номенклатуре» . Психофармакология человека: клиническая и экспериментальная . 16 (S2): S105 - S107. doi : 10.1002/hup.334 . ISSN 0885-6222 . PMID 12404716 . S2CID 12367578 .
- ^ Лонг, Аарон С.; Чжан, Одри Д.; Мейер, Кейтлин Э.; Эгилман, Александр С.; Росс, Джозеф С.; Уоллах, Джошуа Д. (6 мая 2021 г.). «Оценка испытаний, сравнивающих односетиомерные препараты с их раковыми предшественниками: систематический обзор» . Джама сеть открыта . 4 (5): E215731. doi : 10.1001/jamanetworkopen.2021.5731 . PMC 8103227 - через Silverchair.
- ^ Iupac , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « Центр хиральности ». Два : 10.1351/goldbook.c01060
- ^ Jump up to: а беременный Уэйд, Леруа Г. (2006). «Точность в стереохимической терминологии». J. Chem. Образовательный 83 (12): 1793. Bibcode : 2006jched..83.1793W . doi : 10.1021/ed083p1793 . ISSN 0021-9584 .
- ^ Jump up to: а беременный в Каррас, Манфред (2018). «Синтез энантиометрически чистых спиральных ароматических ароматических средств, таких как NHC -лиганды, и их использование в асимметричном катализе (PhD). Университет Чарльза . Получено 6 августа 2021 года .
- ^ Jump up to: а беременный в Элиэль, Эрнест Л.; Уилен, Сэмюэль Х.; Мандер, Льюис Н. (1994). Стереохимия органических соединений . Нью -Йорк: Уайли. ISBN 0471016705 Полем OCLC 27642721 .
- ^ Jump up to: а беременный Клейден, Джонатан; Гривз, Ник; Уоррен, Стюарт Г. (2012). Органическая химия . Оксфорд: издательство Оксфордского университета. ISBN 978-0-19-927029-3 Полем OCLC 761379371 .
- ^ Iupac , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « Асимметричный центр ». два : 10.1351/goldbook.a00480
- ^ Кларк, Эндрю; Китсон, Рассел Р.А.; Мистри, Нимеш; Тейлор, Пол; Тейлор, Мэтью; Ллойд, Майкл; Akamune, Кэролайн (2021). Введение в стереохимию . Кембридж, Великобритания. ISBN 978-1-78801-315-4 Полем OCLC 1180250839 .
{{cite book}}: CS1 Maint: местоположение отсутствует издатель ( ссылка ) - ^ Iupac , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « Стереогенная единица (стереоген/стереоэлемент) ». два : 10.1351/goldbook.s05980
- ^ Вскоре, Курт; Зигель, Джей (1984). «Стереоизомеризм и местная хиральность». J. Am. Химический Соц 106 (11): 3319–3328. doi : 10.1021/ja00323a043 . ISSN 0002-7863 .
- ^ Knoche, B; Blaschke, G (1994). «Исследования по рационизации талидомида in vitro с помощью высокоэффективной жидкой хроматографии». Журнал хроматографии а . 666 (1–2): 235–240. doi : 10.1016/0021-9673 (94) 80385-4 .
- ^ Голосовать, Дональд; Голосовать, Джудит Г.; Пратт, Шарлотта В. (2006). Основы биохимии П. 89 ISBN 0-471-21495-7 .
- ^ Г. Смит; Chl Kennard; Ах белый; PG Hodgson (апрель 1980 г.). «(±) -2- (4-хлор-2-метилфенокси) пропионовая кислота (mecoprop)». Acta Crystallogr. Беременный 36 (4): 992–994. doi : 10.1107/s0567740880005134 .
- ^ Ariëns, Everardus J. (1986). «Стереохимия: источник проблем в лекарственной химии» . Обзоры лекарственных исследований . 6 (4): 451–466. doi : 10.1002/med.2610060404 . ISSN 0198-6325 . PMID 3534485 . S2CID 36115871 .
- ^ Дрейер, Деннис Э. (1986). «Фармакодинамические и фармакокинетические различия между энантиомерами лекарств у людей: обзор» . Клиническая фармакология и терапия . 40 (2): 125–133. doi : 10.1038/clpt.1986.150 . ISSN 0009-9236 . PMID 3731675 . S2CID 33537650 .
- ^ Ariens, EJ (1989). Хиральное разделение от ВЭЖХ . Чичестер: Эллис Хорвод. С. 31–68.
- ^ «Европейское агентство по лекарственным средствам - - Sepracor Pharmaceuticals Ltd снимает свое заявление на авторизацию по маркетингу для Lunivia (Eszopiclone)» . www.ema.europa.eu . 17 сентября 2018 года. Архивировано с оригинала 1 декабря 2017 года . Получено 14 февраля 2011 года .
- ^ Merrill Goozner (2004). Таблетка в 800 миллионов долларов: правда, стоящая за стоимостью новых лекарств (отрывок) . Калифорнийский университет. ISBN 0-520-23945-8 .
- ^ Mohr, JT; Мур, JT; STOLTZ, BM (2016). «EnantioConvergent Catalysis» . Beilstein J. Org. Химический 12 : 2038–2045. doi : 10.3762/bjoc.12.192 . PMC 5082454 . PMID 27829909 . Получено 4 августа 2021 года .
- ^ Альберт, Гиджарро (2008). Происхождение хиральности в молекулах жизни: пересмотр от осознания на текущие теории и перспективы этой нерешенной проблемы . Юс, Мигель. Кембридж, Великобритания: Королевское химическое общество. ISBN 9781847558756 Полем OCLC 319518566 .
- ^ Stickler, Benjamin A.; Дикманн, Мира; Бергер, Роберт; Ван, Дакин (2021-09-14). «Enantiomer Superpositions из межполосных вмешательств в хиральных молекулах» . Физический обзор x . 11 (3): 031056. Arxiv : 2102.06124 . BIBCODE : 2021PHRVX..11C1056S . doi : 10.1103/physrevx.11.031056 . ISSN 2160-3308 . S2CID 231879820 .
- ^ Jump up to: а беременный Чжан, Цишенг; Ривкин, Алексей; Курран, Деннис П. (2002-05-01). «Квазиракемический синтез: концепции и реализация со стратегией флюарного помечения, чтобы сделать как энантиомеры пиридоверина, так и маппицина» . Журнал Американского химического общества . 124 (20): 5774–5781. doi : 10.1021/ja025606x . ISSN 0002-7863 . PMID 12010052 .
- ^ Чжан, Цишенг; Курран, Деннис П. (2005-08-19). «Квазиенантиомеры и квазиракематы: новые инструменты для идентификации, анализа, разделения и синтеза энантиомеров» . Химия - европейский журнал . 11 (17): 4866–4880. doi : 10.1002/Chem.200500076 . ISSN 0947-6539 . PMID 15915521 .
- ^ GS Coumbarides, M. Dingjan, J. Eames, A. Flinn, J 46 (2005), с. 2897er
Внешние ссылки
[ редактировать ] СМИ, связанные с энантиомерами в Wikimedia Commons
СМИ, связанные с энантиомерами в Wikimedia Commons - Chemwiki: стереоизомеризм