Тиазол
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
1,3-тиазол | |||
| Другие имена
Тиазол
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.005.475 | ||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 3 Ч 3 Н С | |||
| Молярная масса | 85.12 g·mol −1 | ||
| Точка кипения | От 116 до 118 ° C (от 241 до 244 ° F; от 389 до 391 К) | ||
| Кислотность ( pKa ) | 2,5 (сопряженной кислоты) [ 1 ] | ||
| -50.55·10 −6 см 3 /моль | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
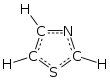
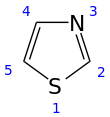
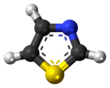
Тиазол ( / ˈ θ aɪ . ə z oʊ l / ), или 1,3-тиазол , представляет собой 5-членное гетероциклическое соединение , содержащее как серу, так и азот. Термин «тиазол» также относится к большому семейству производных. Сам тиазол представляет собой бледно-желтую жидкость с пиридиноподобным запахом и молекулярной формулой C 3 H 3 NS. [ 2 ] Тиазольное кольцо известно как компонент витамина тиамина ( B 1 ).
Молекулярная и электронная структура
[ редактировать ]Тиазолы относятся к группе азолов , гетероциклов, к которым относятся имидазолы и оксазолы . Тиазол также можно считать функциональной группой , когда он является частью более крупной молекулы.
Будучи планарными, тиазолы характеризуются значительной делокализацией пи-электронов и обладают некоторой степенью ароматичности , большей, чем соответствующие оксазолы . Об этой ароматности свидетельствует 1 Химический сдвиг H-ЯМР кольцевых протонов, которые поглощают от 7,27 до 8,77 м.д., что указывает на сильный диамагнитный кольцевой ток . Рассчитанная плотность пи-электронов отмечает C5 как основной сайт электрофильного замещения, а C2-H как подверженный депротонированию.
Встречание тиазолов и солей тиазолия
[ редактировать ]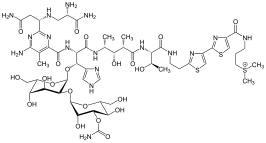
Тиазолы встречаются во множестве специализированных продуктов, часто сплавленных с производными бензола, так называемыми бензотиазолами. Помимо витамина B1 , тиазольное кольцо имеется в эпотилоне . Другими важными производными тиазола являются бензотиазолы , например, люциферин, химическое вещество светлячков . В то время как тиазолы широко представлены в биомолекулах , оксазолы — нет. Он содержится в встречающихся в природе пептидах и используется при разработке пептидомиметиков (т.е. молекул, имитирующих функцию и структуру пептидов). [ 3 ]
Коммерчески значимые тиазолы включают главным образом красители и фунгициды . Тифлузамид, Трициклазол и Тиабендазол продаются для борьбы с различными сельскохозяйственными вредителями. Другим широко используемым производным тиазола является нестероидный противовоспалительный препарат Мелоксикам . Следующие антрохиноновые красители содержат субъединицы бензотиазола: алгол желтый 8 (CAS# [6451-12-3]), алгол желтый GC (CAS# [129-09-9]), индантрен рубин B (CAS# [6371-49-9]). ]), Индантрен Синий CLG (CAS# [6371-50-2] и Индантрен Синий CLB (CAS#[6492-78-0]). Эти тиазольные красители используются для крашения хлопка .
Синтез
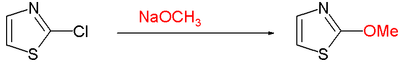
[ редактировать ]Существуют различные лабораторные методы органического синтеза тиазолов. Выдающимся является синтез тиазола Ганча, который представляет собой реакцию между галокетонами и тиоамидами . Например, 2,4-диметилтиазол синтезируют из тиоацетамида и хлорацетона . [ 4 ] В синтезе Кука-Хейльброна тиазолы возникают при конденсации α-аминонитрила с сероуглеродом . Доступ к тиазолам можно получить путем ацилирования 2-аминотиолатов, часто получаемых по реакции Герца .
Биосинтез
[ редактировать ]Тиазолы обычно образуются в результате реакций цистеина , который обеспечивает основу NCCS кольца. Однако тиамин не соответствует этой схеме. Несколько путей биосинтеза приводят к тиазольному кольцу, необходимому для образования тиамина. [ 5 ] Сера тиазола получается из цистеина. У анаэробных бактерий группа CN происходит от дегидроглицина.
Реакции
[ редактировать ]При pK a 2,5 для сопряженной кислоты тиазолы гораздо менее основные, чем имидазол (pK a = 7). [ 6 ]
Депротонирование сильными основаниями происходит по линии C2-H. Отрицательный заряд в этой позиции стабилизируется в виде илида . В этом месте реагируют основания Хаузера и литийорганические соединения , замещая протон. 2-Литиотиазолы также образуются путем обмена металл-галоген из 2-бромтиазола. [ 7 ]
Электрофильное ароматическое замещение у C5, но требует активирующих групп , таких как метильная группа, как показано на примере бромирования :
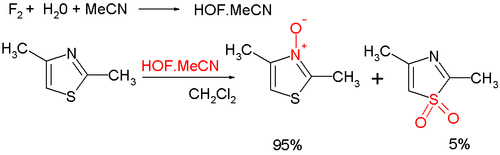
Окисление азотом дает ароматический N -оксид тиазола ; существует множество окислителей, таких как mCPBA ; новым является гипофтористая кислота, полученная из фтора и воды в ацетонитриле ; часть окисления происходит по сере, что приводит к образованию неароматического сульфоксида / сульфона : [ 8 ] -оксиды тиазола N полезны в арилировании CH, катализируемом палладием, где N -оксид способен смещать реакционную способность в пользу положения 2 и позволяет проводить эти реакции в гораздо более мягких условиях. [ 9 ]
- Тиазолы представляют собой формилсинтоны ; Превращение R-тиа в альдегид R-CHO происходит при: [ 7 ] соответственно, йодистый метил ( N -метилирование), органическое восстановление боргидридом натрия и гидролиз хлоридом ртути (II) в воде.
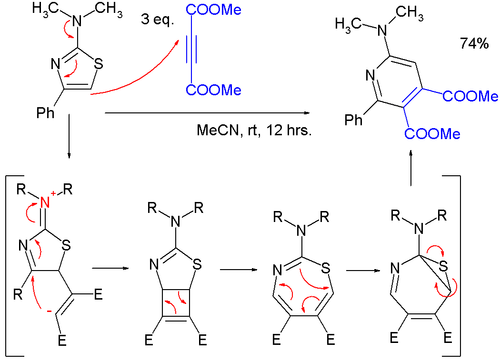
- Тиазолы могут реагировать циклоприсоединениями , но обычно при высоких температурах из-за благоприятной ароматической стабилизации реагента; Реакции Дильса-Альдера с алкинами сопровождаются экструзией серы, конечным продуктом является пиридин ; в одном исследовании, [ 10 ] Было обнаружено, что очень мягкая реакция 2-(диметиламино)тиазола с диметилацетилендикарбоксилатом (ДМАД) с пиридином протекает через цвиттер-ионный интермедиат при формальном [2+2]циклоприсоединении к циклобутену, а затем к 1,3-тиазепину. в раскрытие 4-электронного электроциклического кольца , а затем в 7-тиа-2-азаноркарадиен в 6-электронное электроциклическое кольцо, замыкающееся перед вытеснением атома серы.
Тиазолиевые соли
[ редактировать ]Алкилирование тиазолов по азоту образует катион тиазолия . Соли тиазолия являются катализаторами реакции Стеттера и бензоиновой конденсации . Депротонирование солей N -алкилтиазолия дает свободные карбены. [ 11 ] и карбеновые комплексы переходных металлов .
Алагебриум – препарат на основе тиазолия.
Ссылки
[ редактировать ]- ^ Золтевич, Ю.А.; Дэди, LW (1978). «Кватернизация гетероароматических соединений: количественные аспекты». Достижения гетероциклической химии. Том 22 . Том. 22. С. 71–121. дои : 10.1016/S0065-2725(08)60103-8 . ISBN 9780120206223 .
- ^ Эйхер, Т.; Гауптманн, С. (2003). Химия гетероциклов: структура, реакции, синтез и применение . Уайли. ISBN 978-3-527-30720-3 .
- ^ Мак, Джеффри Ю.В.; Сюй, Вэйцзюнь; Фэрли, Дэвид П. (1 января 2015 г.). Пептидомиметики I (PDF) . Темы гетероциклической химии. Том. 48. Шпрингер Берлин Гейдельберг. стр. 235–266. дои : 10.1007/7081_2015_176 . ISBN 978-3-319-49117-2 .
- ^ Джордж Шварц (1945). «2,4-Диметилтиазол». Органические синтезы . 25:35 . дои : 10.15227/orgsyn.025.0035 .
- ^ Крик, М.; Мартинс, Ф.; Леонарди, Р.; Фэрхерст, ЮАР; Лоу, диджей; Роуч, Польша (2007). «Тиазолсинтаза из Escherichia coli : исследование субстратов и очищенных белков, необходимых для активности in vitro » (PDF) . Ж. Биол. Хим . 282 (24): 17413–17423. дои : 10.1074/jbc.M700782200 . ПМИД 17403671 .
- ^ Томас Л. Гилкрист (1997). Гетероциклическая химия (3-е изд.). Эссекс, Англия: Эддисон Уэсли. п. 414. ИСБН 0-582-27843-0 .
- ^ Jump up to: а б Дондони, А.; Мерино, П. (1995). «Диастереоселективная омологация ацетонида D-(R)-глицеральдегида с использованием 2-(триметилсилил)тиазола». 72:21 . дои : 10.15227/orgsyn.072.0021 .
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Амир, Э.; Розен, С. (2006). «Легкий доступ к семейству тиазол -N -оксидов с использованием HOF·CH 3 CN». Химические коммуникации . 2006 (21): 2262–2264. дои : 10.1039/b602594c . ПМИД 16718323 .
- ^ Кампо, Луи-Шарль; Бертран-Лаперль, Меган; Леклерк, Жан-Филипп; Виллемюр, Элизия; Горельский, Серж; Фаньу, Кейт (01 марта 2008 г.). «Прямое арилирование азолов, N-оксидов C2, C5 и C4, включая реакции при комнатной температуре» . Журнал Американского химического общества . 130 (11): 3276–3277. дои : 10.1021/ja7107068 . ISSN 0002-7863 . ПМИД 18302383 .
- ^ Алахарин, М.; Кабрера, Дж.; Пастор А.; Санчес-Андрада, П.; Баутиста, Д. (2006). «О [2+2]-циклоприсоединении 2-аминотиазолов и диметилацетилендикарбоксилата. Экспериментальные и расчетные доказательства термического дисротационного раскрытия кольца конденсированных циклобутенов». Дж. Орг. хим. 71 (14): 5328–5339. дои : 10.1021/jo060664c . ПМИД 16808523 .
- ^ Ардуэнго, Эй Джей; Герлих-младший; Маршалл, WJ (1997). «Стабильный тиазол-2-илиден и его димер». Либигс Аннален . 1997 (2): 365–374. дои : 10.1002/jlac.199719970213 .