Гексаметилфосфорамид
| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Гексаметилфосфорный триамид [ 3 ] | |
| Другие имена | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 1099903 | |
| КЭБ | |
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.010.595 |
| Номер ЕС |
|
| 3259 | |
| КЕГГ | |
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 2810 3082 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 6 Ч 18 Н 3 О П | |
| Молярная масса | 179.20 g/mol |
| Появление | прозрачная бесцветная жидкость [ 4 ] |
| Запах | ароматный, мягкий, аминоподобный [ 4 ] |
| Плотность | 1,03 г/см 3 |
| Температура плавления | 7,20 ° С (44,96 ° F; 280,35 К) |
| Точка кипения | 232,5 ° C (450,5 ° F; 505,6 К) CRC [ 5 ] |
| смешиваемый [ 4 ] | |
| Давление пара | 0,03 мм рт.ст. (4,0 Па) при 20 °C [ 4 ] |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
Подозрение на канцероген [ 4 ] |
| СГС Маркировка : | |

| |
| Опасность | |
| Х340 , Х350 | |
| П201 , П202 , П281 , П308+П313 , П405 , П501 | |
| точка возгорания | 104,4 ° С (219,9 ° F; 377,5 К) |
| NIOSH (пределы воздействия на здоровье в США): | |
ПЭЛ (допустимо)
|
никто [ 4 ] |
РЕЛ (рекомендуется)
|
Что [ 4 ] |
IDLH (Непосредственная опасность)
|
Это [НД] [ 4 ] |
| Паспорт безопасности (SDS) | Оксфордский паспорт безопасности материалов |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
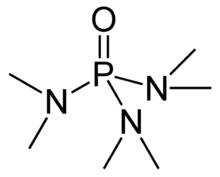
Гексаметилфосфорамид , часто сокращенно HMPA , представляет собой фосфорамид ( амид фосфорной кислоты ) с формулой [(CH 3 ) 2 N] 3 PO. Эта бесцветная жидкость является полезным реагентом в органическом синтезе .
Структура и реакционная способность
[ редактировать ]HMPA представляет собой оксид трис(диметиламино)фосфина P(NMe 2 ) 3 . Как и другие оксиды фосфина (например, оксид трифенилфосфина ), молекула имеет тетраэдрическое ядро и связь P=O, которая сильно поляризована, со значительным отрицательным зарядом, находящимся на атоме кислорода.
Соединения, содержащие связь азот -фосфор, обычно разлагаются соляной кислотой с образованием протонированного амина и фосфата.
Растворяет соли щелочных металлов. [ 6 ] и щелочные металлы, образующие синие растворы, стабильные в течение нескольких часов. сольватированные электроны . В этих синих растворах присутствуют [ 7 ]
Приложения
[ редактировать ]HMPA – специальный растворитель для полимеров , газов и металлоорганических соединений . Он улучшает селективность реакций литиирования за счет разрушения олигомеров литиевых оснований , таких как бутиллитий . Поскольку HMPA избирательно сольватирует катионы, он ускоряет медленные реакции S N 2 за счет образования большего количества голых анионов. Основные азотные центры в HMPA сильно координируются с Li. + . [ 8 ]
HMPA является лигандом в полезных реагентах на основе комплексов молибдена пероксидных , например, MoO(O 2 ) 2 (HMPA)(H 2 O) используется в качестве окислителя в органическом синтезе. [ 9 ]
Альтернативные реагенты
[ редактировать ]Диметилсульфоксид часто можно использовать вместо HMPA в качестве сорастворителя. Оба являются сильными акцепторами водородных связей , а их атомы кислорода связывают катионы металлов . Другие альтернативы HMPA включают N , N' -тетраалкилмочевины DMPU (диметилпропиленмочевина). [ 10 ] [ 11 ] или ДМИ (1,3-диметил-2-имидазолидинон). [ 12 ] Сообщается, что триамид трипирролидинофосфорной кислоты (TPPA) является хорошим реагентом-заменителем HMPA при восстановлении дииодидом самария. [ 13 ] и в качестве базовой добавки Льюиса во многих реакциях с участием самария кетилов . [ 14 ]
Токсичность
[ редактировать ]HMPA лишь слегка токсичен, но было показано, что он вызывает рак у крыс. [ 8 ] HMPA может разлагаться под действием соляной кислоты .
Ссылки
[ редактировать ]- ^ Не рекомендуется: см. справочник по Синей книге.
- ^ Это имя также используется для обозначения трис (диметиламино) фосфина.
- ^ «Фронт материи». Номенклатура органической химии: рекомендации ИЮПАК и предпочтительные названия 2013 г. (Синяя книга) . Кембридж: Королевское химическое общество . 2014. стр. P001–P004. дои : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Jump up to: а б с д и ж г час Карманный справочник NIOSH по химическим опасностям. «#0321» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Хейнс, Уильям М. (2010). Справочник по химии и физике (91 изд.). Бока-Ратон, Флорида, США: CRC Press . п. 3-280. ISBN 978-1-43982077-3 .
- ^ Люэрс, Дин К.; Кохут, Джон П. (1974). «Гексаметилфосфорамидные сольваты солей щелочных металлов». Журнал неорганической и ядерной химии . 36 (7): 1459–1460. дои : 10.1016/0022-1902(74)80605-6 .
- ^ Греммо, Норберто; Рэндлс, Джон Э.Б. (1974). «Сольватированные электроны в гексаметилфосфорамиде. Часть 1. Проводимость растворов щелочных металлов». Журнал Химического общества, Транзакции Фарадея 1: Физическая химия в конденсированных фазах . 70 : 1480–1487. дои : 10.1039/F19747001480 .
- ^ Jump up to: а б Дикстра, Р.Р. (2001). «Гексаметилфосфортриамид». Гексаметилфосфортриамид . Энциклопедия реагентов для органического синтеза . Нью-Йорк, штат Нью-Йорк: Джон Уайли и сыновья. дои : 10.1002/047084289X.rh020 . ISBN 978-0471936237 .
- ^ Дикман, Майкл Х.; Поуп, Майкл Т. (1994). «Пероксо- и супероксокомплексы хрома, молибдена и вольфрама». Химические обзоры . 94 (3): 569–584. дои : 10.1021/cr00027a002 .
- ^ Мухопадхьяй, Т.; Сибах, Д. (1982). «Замена HMPT циклической мочевиной DMPU в качестве сорастворителя для высокореактивных нуклеофилов и оснований» . Helvetica Chimica Acta . 65 (1): 385–391. дои : 10.1002/hlca.19820650141 .
- ^ Бек, АК; Сибах, Д. (2001). « N , N’ -Диметилпропиленмочевина». N,N'-Диметилпропиленмочевина . Энциклопедия реагентов для органического синтеза . Нью-Йорк: Джон Уайли и сыновья. дои : 10.1002/047084289X.rd366 . ISBN 978-0471936237 .
- ^ Ло, Чи-Чу; Чао, Пей-Мин (1990). «Замена канцерогенного растворителя HMPA на DMI в синтезе половых феромонов насекомых». Журнал химической экологии . 16 (12): 3245–3253. дои : 10.1007/BF00982095 . ПМИД 24263426 . S2CID 9859086 .
- ^ Макдональд, Крисс Э.; Рэмси, Джереми Д.; Сэмпселл, Дэвид Г.; Батлер, Джули А.; Чеккини, Майкл Р. (2010). «Триамид трипирролидинофосфорной кислоты как активатор восстановления дииодида самария». Органические письма . 12 (22): 5178–5181. дои : 10.1021/ol102040s . ПМИД 20979412 .
- ^ Берндт, Матиас; Хёлеманн, Александра; Нирманн, Андре; Бенц, Кристоф; Циммер, Рейнхольд; Рейссиг, Ганс-Ульрих (2012). «Замена HMPA в дииодиде самария способствует циклизации и реакциям литийорганических соединений». Европейский журнал органической химии . 2012 (7): 1299–1302. дои : 10.1002/ejoc.201101830 . ISSN 1099-0690 .
Триамид трипирролидинофосфорной кислоты (TPPA) может заменить канцерогенный HMPA в качестве основной добавки Льюиса во многих реакциях с участием кетилов самария. В большинстве случаев выходы и селективность циклизаций (гет)арилов, алкенил- и алкинилкетонов близки.
Внешние ссылки
[ редактировать ]- «Гексаметилфосфорамид № CAS 680-31-9» (PDF) . Отчет о канцерогенах (12-е изд.). Национальная программа токсикологии, Министерство здравоохранения и социальных служб. 2011.
- «Гексаметилфосфорамид» . Карманный справочник NIOSH по химическим опасностям . Центры по контролю и профилактике заболеваний Министерства здравоохранения и социальных служб. 2011.
- Индекс Мерк . Том. 4761 (12-е изд.).