Umbelliferone
Эта статья требует дополнительных цитат для проверки . ( март 2020 г. ) |

| |

| |
| Имена | |
|---|---|
| Предпочтительное имя IUPAC
7-гидрокси-2 H -1-бензопирана-2-ой | |
| Другие имена
7 -гидроксикумарин, гидрангин, спемтин, бета -рассол
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Чеби | |
| Химический | |
| Chemspider | |
| Echa Infocard | 100.002.038 |
PubChem CID
|
|
| НЕКОТОРЫЙ | |
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 9 H 6 O 3 | |
| Молярная масса | 162.14 g/mol |
| Появление | желтовато-белый кристаллический порошок без запаха |
| Точка плавления | 230 ° C (446 ° F; 503 K) (разлагается) |
| -88.22·10 −6 см 3 /мол | |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Umbelliferone , также известный как 7 -гидроксикумарин , гидрангин , спемтин и бета -баболферон , является натуральным продуктом семейства кумаринов .
Он сильно впитывает ультрафиолетовый свет на нескольких длин волн. Есть некоторые признаки того, что это химическое вещество является антимутагенным , [ 1 ] Он используется в солнцезащитных кремах . [ 2 ] Сообщалось, что Umbelliferone обладает антиоксидантными свойствами. [ 3 ] [ 4 ]
Это желтовато-белое кристаллическое твердое вещество, которое имеет небольшую растворимость в горячей воде, но с высокой растворимостью в этаноле .
Природные события и название
[ редактировать ]Имя Umbelliferone из семейства растений Umbelliferae , и семейство растений, в свою очередь, была названа в честь их зонтика в форме соцветий , каждый из которых называется зонтиком .
Umbelliferone встречается во многих знакомых растениях семейства Apiaceae (Umbelliferae), таких как морковь , кориандр и садовая анжелика , а также в растениях других семей, таких как ястреба мыши-мыши ( Hieracium Pilosella , Astecaeae) или Bigleaf Hydrangea ( Hyderangeae Macrophylla , Hydrangeaceae, под названием Hydrangine).
Это один из компонентов Асафоэтиды , сухого латекса от гигантского фенхеля ( Ferula Communis ).
Это также встречается в Justicia pectoralis (Acanthaceae). [ 5 ] [ 6 ]
Биосинтез
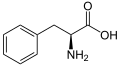
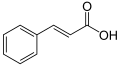
[ редактировать ]Амбеллиферон является фенилпропаноидом и как таковой синтезируется из l-фенилаланина , который, в свою очередь, производится через путь шикимат . Фенилаланин покрыт , корицевой кислотой за которым следует гидроксилирование с помощью 4-гидроксилазы корица с получением 4-кумарной кислоты . 4-кумарная кислота снова гидроксилируется с помощью косинки/кумарата 2-гидроксилазы, чтобы получить 2,4-дигидрокси-циннамическую кислоту ( зонтичную кислоту ) с последующей вращением ненасыщенной связи, прилегающей к группе карбоновой кислоты . Наконец, внутримолекулярная атака от гидроксильной группы C2 'к группе карбоновой кислоты закрывает кольцо и образует лактон -зонтиферон.
Химический синтез
[ редактировать ]Амбеллиферон традиционно синтезируется с использованием конденсации печманна , от резорцинола и формалаксусной кислоты (генерируемой из ямочной кислоты in situ ). [ 7 ]
Более новый синтез использует метил пропионат и палладийский катализатор .
Ультрафиолетовая флуоресценция
[ редактировать ]Umbelliferone сильно поглощается при 300, 305 и 325 нм , при этом значения log ε составляют 3,9, 3,95 и 4,15 соответственно, и он флуоресцирует синюю как у ультрафиолетового, так и в видимом свете. Мощное поглощение на трех разных длин волн, в сочетании с тем фактом, что энергия безопасно рассеивается как видимый свет, сделают Umbelliferone полезным солнцезащитным агентом. Изменения поглощения в щелочном растворе, поскольку фенольная гидроксильная группа депротонирована ( PK A = 7,7).
Использование
[ редактировать ]Ультрафиолетовая активность Umbelliferone привела к его использованию в качестве солнцезащитного агента и оптического осветления для текстиля . Он также использовался в качестве среды усиления для лазеров красителей . Umbelliferone может использоваться в качестве индикатора флуоресценции для ионов металлов, таких как медь и кальций . Он действует как индикатор pH в диапазоне 6,5-8,9. [ Цитация необходима ]
Амбеллиферон является мощным ингибитором типа 3 17β-гидроксистероиддегидрогеназы , первичного фермента, ответственного за преобразование 4 андростена-3,17-дионера в тестостерон с IC50 1,4 мкМ. [ 8 ]
Производные
[ редактировать ]Umbelliferone является родительским соединением для большого количества натуральных продуктов. Герниарин (7 -o -метилумбеллиферон или 7-метоксикумарин) встречается в листьях конопли ( эупатория аяпана ) и Rupturewort ( herniaria ). О -гликозилированные производные, такие как спеммин (7 -O -β -d -глюкопиранозилумбеллферон), встречаются естественным образом и используются для фториметрического определения гликозидгидролазы ферментов . Изопренилированные производные также широко распространены, такие как мармин (найденный в коже грейпфрута и в коре дерева Баэля ) и фурукумарины, такие как мармезин , ангельский и псорален .
Umbelliferone 7-апиосилглюкозид может быть выделен из корня гмелина арборе . [ 9 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Ohta T, Watanabe K, Moriya M, Shirasu Y, Kada T (1983). «Антимутагенные эффекты кумарина и зонтиферона на мутагенез, вызванный 4-нитрохинолином 1-оксидным или УФ-облучением в e. Coli» . Мутационные исследования . 117 (1–2): 135–138. doi : 10.1016/0165-1218 (83) 90160-x . PMID 6403855 .
- ^ Du L (2008). «Рациональный дизайн флуоресцентного зонда перекиси водорода на основе флуорофора Umbelliferone» . Тетраэдр буквы . 49 (19): 3045–3048. doi : 10.1016/j.tetlet.2008.03.063 . PMC 2490821 . PMID 19081820 .
- ^ "Umbelliferone" . www.chemicalland21.com . Получено 21 ноября 2011 года .
- ^ Сим Мо, Ли Хи, Хэм -младший, Сео Ки, Ким М.Дж., Ли М.К. (2015). «Противовоспалительные и антиоксидантные эффекты Umbelliferone у хронических крыс с спиртом» . Nutr Res Pract . 9 (4): 364–369. doi : 10.4162/nrp.2015.9.4.364 . PMC 4523479 . PMID 26244074 .
- ^ Лил Л.К., Ааг Феррейра, Гаерра, Фьяматос, GSB Viana (май 2000). «Тантиноцицептивная, противовоспалительная и бронходилататорная активность бразильских лекарственных растений, содержащих кумарин: сравнительное исследование» Журнал этнофармакологии 70 (2): 151–1 Doi : 10.1016/s0378-8741 (99) 0165-8 ISSN 0378-8 PMID 107771205
- ^ Lino CS, ML Taveira, GSB Viana, FJA Matos (1997). «Анальгетическая и противовоспалительная активность Justicia pectoralis jacq и ее основных компонентов: кумарин и зонтиферон» . Фитотерапевтическое исследование . 11 (3): 211–215. doi : 10.1002/(SICI) 1099-1573 (199705) 11: 3 <211 :: AID-PTR72> 3.0.CO; 2-W . S2CID 84525194 . Архивировано из оригинала 2013-01-05 . Получено 2010-06-26 .
- ^ Ahluwalia VK (2010-09-30). Промежуточные соединения для органического синтеза . IK International. п. 211. ISBN 978-81-88237-33-3 .
- ^ Poirier D (март 2003 г.). «Ингибиторы 17 бета-гидроксистероиддегидрогеназы». Curr Med Chem . 10 (6): 453–477. doi : 10.2174/0929867033368222 . PMID 12570693 .
- ^ P. Satyanarayana, P. Subrahmanyam, R. Kasai, O. Tanaka (1985). «Гликозид кумарина с изменением апиозы из корня Гмелины Арборея». Фитохимия . 24 (8): 1862–1863. Bibcode : 1985pchem..24.1862S . Doi : 10.1016/s0031-9422 (00) 82575-3 .
Дальнейшее чтение
[ редактировать ]- Дин Ф. (1963). Природные соединения кислородного кольца . Лондон: Баттервортс. ISBN 978-0-408-26750-2 .
- Joule J, Mills K (2000). Гетероциклическая химия (4 -е изд.). Оксфорд: Наука Блэквелла. ISBN 978-0-632-05453-4 .
- Barton D, Nakanishi K, Meth-Cohn O, Eds. (1999). Комплексная химия натуральных продуктов . Тол. 2. Оксфорд: Elsevier . п. 677. ISBN 978-0-08-043154-3 .