Биометалл (биология)
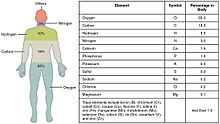
Биометаллы (также называемые биосовместимыми металлами , биоактивными металлами , металлическими биоматериалами ) — это металлы, которые обычно присутствуют в небольших, но важных и измеримых количествах в биологии , биохимии и медицине . Металлы медь , цинк , железо и марганец являются примерами металлов, которые необходимы для нормального функционирования большинства растений и тел большинства животных , таких как организм человека . Некоторые из них ( кальций , калий , натрий ) присутствуют в относительно больших количествах, тогда как большинство других представляют собой микроэлементы , присутствующие в меньших, но важных количествах (на изображении показано процентное соотношение для человека). Примерно 2/3 существующей таблицы Менделеева состоит из металлов с различными свойствами. [1] объясняя различные способы использования металлов (обычно в ионной форме) в природе и медицине.
История
[ редактировать ]Сначала изучение биометаллов называлось бионеорганической химией . Каждая отрасль бионеорганической химии изучала отдельные, отдельные разделы предмета. Однако это привело к изолированному взгляду на каждый конкретный аспект биологической системы. Эта точка зрения была пересмотрена в целостный подход к биометаллам в металломике . [2]
Ионы металлов в биологии изучались в разных специальностях. В питании оно должно было определить самое необходимое для жизни; в токсикологии для определения отрицательного воздействия ионов некоторых металлов на биологические системы и в фармакологии для их терапевтического воздействия. [2] В каждой области сначала они изучались и разделялись по признаку концентрации. В небольших количествах ионы металлов в биологической системе могут функционировать с оптимальной функциональностью, тогда как в более высоких концентрациях ионы металлов могут оказаться фатальными для биологических систем. Однако градиенты концентрации оказались произвольными, поскольку низкие концентрации несущественных металлов (таких как литий или гелий ) в незаменимых металлах (таких как натрий или калий ) могут вызвать неблагоприятное воздействие на биологические системы, и наоборот. [2]
Исследования биометаллов и их эффектов восходят к 19 веку и еще дальше к 18 веку, когда было обнаружено железо в крови. [2] цинк Было установлено, что необходим для роста грибков дрожжей , как показал Жюль Рален в 1869 году, однако никаких доказательств необходимости цинка в клетках человека не было показано до конца 1930-х годов, когда его присутствие было продемонстрировано в карбоангидразе , и 1960-х годов, когда он был идентифицирован. как необходимый элемент для человека. [2] С тех пор понимание цинка в биологии человека продвинулось до такой степени, что он считается таким же важным, как и железо. Современные достижения аналитических технологий прояснили важность биометаллов в сигнальных путях и первоначальные представления о химической основе жизни . [2]
Биометаллы природного происхождения
[ редактировать ]Ионы металлов необходимы для функционирования многих белков, присутствующих в живых организмах, таких как металлопротеины и ферменты, которым ионы металлов необходимы в качестве кофакторов . [3] Процессы, включая транспорт кислорода и репликацию ДНК, осуществляются с использованием таких ферментов, как ДНК-полимераза , для правильного функционирования которой у людей требуются магний и цинк. [4] Другие биомолекулы также содержат в своей структуре ионы металлов, например йода в гормонах щитовидной железы человека. [5]
Ниже перечислено использование некоторых из них. Список не является исчерпывающим, поскольку охватывает только основных членов класса; другие, которые представляют собой следы металлов особенно низкой биоконцентрации, здесь не исследованы. Некоторые элементы, являющиеся неметаллами или металлоидами (например, селен ), выходят за рамки этой статьи.
Кальций
[ редактировать ]Кальций является наиболее распространенным металлом у эукариот и, соответственно, у человека. Тело состоит примерно из 1,5% кальция, и это обилие отражается в отсутствии окислительно-восстановительной токсичности и его участии в стабильности структуры мембран и других биомолекул. [6] Кальций участвует в оплодотворении яйцеклетки, контролирует некоторые процессы развития и может регулировать клеточные процессы, такие как обмен веществ или обучение. Кальций также играет роль в структуре костей , поскольку жесткость костного матрикса позвонков аналогична природе гидроксиапатита кальция . [6] Кальций обычно связывается с другими белками и молекулами, чтобы выполнять другие функции в организме. Белки, связанные с кальцием, обычно играют важную роль в межклеточной адгезии , гидролитических процессах (таких как гидролитические ферменты, такие как гликозидазы и сульфатазы ), а также в сворачивании и сортировке белков . [6] Эти процессы влияют на большую часть клеточной структуры и метаболизма.
Магний
[ редактировать ]Магний является наиболее распространенным свободным катионом в цитозоле растений , центральным атомом хлорофилла выступает в качестве мостикового иона для агрегации рибосом и в растениях. [7] Даже небольшие изменения концентрации магния в цитозоле или хлоропластах растений могут радикально повлиять на ключевые ферменты, присутствующие в хлоропластах. Он чаще всего используется в качестве кофактора у эукариот и действует как важный функциональный ключ в таких ферментах, как РНК-полимераза и АТФаза . [7] В фосфорилирующих ферментах, таких как АТФаза или киназы и фосфаты , магний действует как стабилизирующий ион в полифосфатных соединениях из-за его кислотности по Льюису . [6] Магний также был отмечен как возможный вторичный посредник нейронной передачи. [6] Магний действует как аллостерический ингибитор фермента вакуолярной пирофосфатазы (V-PP iазы ). In vitro концентрация свободного магния действует как строгий регулятор и стабилизатор активности фермента V-PP - иазы. [7]
Марганец
[ редактировать ]Марганец , как и магний, играет решающую роль в качестве кофактора в различных ферментах, хотя его концентрация заметно ниже, чем у другого. [6] Ферменты, в которых марганец используется в качестве кофактора, известны как «марганцовопротеины». Эти белки включают ферменты, такие как оксидоредуктазы , трансферазы и гидролазы , которые необходимы для метаболических функций и антиоксидантных реакций. [6] Марганец играет важную роль в защите организма, свертывании крови, репродукции, пищеварении и различных других функциях организма. В частности, что касается защиты хозяина, марганец действует как профилактическая мера окислительного стресса, уничтожая свободные радикалы , которые представляют собой ионы , имеющие неспаренный электрон во внешних оболочках.
Цинк
[ редактировать ]Цинк — второй по распространенности переходный металл, присутствующий в живых организмах, уступающий только железу. Это имеет решающее значение для роста и выживания клеток. У человека цинк в основном содержится в различных органах и тканях, таких как мозг, кишечник, поджелудочная железа и молочные железы. [8] У прокариотов цинк может действовать как противомикробное средство , а наночастицы оксида цинка могут действовать как антибактериальное средство или антибиотик. цинка Гомеостаз строго контролируется, что позволяет использовать его преимущества без риска смерти из-за его высокой токсичности. [8] Из-за антибиотической природы цинка его часто используют во многих препаратах против бактериальных инфекций у людей. И наоборот, из-за бактериальной природы митохондрий цинковые антибиотики также смертельны для митохондрий и приводят к гибели клеток при высоких концентрациях. [8] Цинк также используется в ряде транскрипционных факторов, белков и ферментов.
Натрий
[ редактировать ]Натрий — это металл, роль которого в организме человека открыли люди, а также он является одним из двух щелочных металлов , которые играют важную роль в функциях организма. Он играет важную роль в поддержании потенциала клеточной мембраны и электрохимического градиента в организме через натриево-калиевый насос и натрий-глюкозные транспортные белки . Натрий также играет важную роль в нервной системе и клеточной коммуникации, поскольку он попадает в аксоны во время потенциала действия, чтобы сохранить силу сигнала. [9] Также было показано, что натрий влияет на иммунный ответ как по эффективности, так и по скорости. Макрофаги увеличивают скорость пролиферации при высоких концентрациях соли, и организм использует высокие концентрации натрия в изолированных регионах для создания усиленного иммунного ответа, который исчезает после того, как инфекция устранена. [10]
Калий
[ редактировать ]В растениях калий играет ключевую роль в поддержании здоровья растений. Высокие концентрации калия в растениях играют ключевую роль в синтезе необходимых белков в растениях, а также в развитии растительных органелл, таких как клеточные стенки, для предотвращения повреждения вирусами и насекомыми. [11] Он также снижает концентрацию молекул с низкой молекулярной массой, таких как сахара и аминокислоты, и увеличивает концентрацию молекул с высокой молекулярной массой, таких как белок, которые также предотвращают развитие и распространение вирусов. [11] Абсорбция калия имеет положительную корреляцию с аквапоринами и поглощением воды растительными клетками через белки клеточных мембран. [11] Из-за этой корреляции было отмечено, что калий также играет ключевую роль в движении и регуляции устьиц, поскольку высокие концентрации калия перемещаются в устьица растений , чтобы поддерживать их открытыми и способствовать фотосинтезу . [11] У животных калий также играет ключевую роль наряду с натрием в поддержании потенциала клеточной мембраны в состоянии покоя и межклеточной коммуникации посредством реполяризации аксонных путей после возникновения потенциала действия между нейронами. [9] Калий также может играть ключевую роль в поддержании кровяного давления у животных, как показано в исследовании, в котором тяжесть заболеваний пародонта и гипертонии обратно коррелировали с экскрецией калия с мочой (характерный признак низкого потребления калия). [12]
Железо
[ редактировать ]Железо также является наиболее распространенным переходным металлом в организме человека и используется в различных процессах, таких как транспорт кислорода и производство АТФ. Он играет ключевую роль в функционировании таких ферментов, как цитохромы a , b и c, а также комплексов железа и серы , которые играют важную роль в производстве АТФ. [13] Он присутствует во всех типах клеток мозга, поскольку сам мозг имеет очень высокие потребности в энергии и, как следствие, очень высокую потребность в железе. [13] У животных железо играет очень важную роль в транспортировке кислорода от легких к тканям и CO 2 от тканей к легким. Это происходит с помощью двух важных транспортных белков, называемых гемоглобином и миоглобином . [14] Гемоглобин в крови переносит кислород из легких в миоглобин в тканях. Оба белка представляют собой тетрамерные комплексы с белковыми комплексами железа, называемыми гемами, встроенными в каждую субъединицу тетрамера. Кислород связывается с железом в геме посредством аффинного связывания или лигандирования и диссоциирует от белка, как только он достигает места назначения. [14] Железо также может быть потенциальным канцерогеном по трем причинам; во-первых, это производство гидроксильных радикалов . Ионы железа можно восстановить с помощью супероксида , а продукт можно повторно окислить с помощью пероксида с образованием гидроксильных радикалов. Гидроксильные радикалы и другие активные формы кислорода, образующиеся вблизи ДНК, могут вызывать точечные мутации , перекрестные связи и разрывы . [15] Второе — усиление роста неопластических клеток за счет подавления защитных сил хозяина. Избыточное железо угнетает активность CD4 - лимфоцитов и подавляет туморицидную активность макрофагов . [15] Третий способ действовать как канцероген — это функционирование в качестве важного питательного вещества для неограниченного пролиферации опухолевых клеток. [15]
Литий
[ редактировать ]Литий присутствует в биологических системах в следовых количествах ; его функции неопределенны. Соли лития оказались полезными в качестве стабилизатора настроения и антидепрессанта при лечении психических заболеваний, таких как биполярное расстройство .
Неприродные биометаллические комплексы
[ редактировать ]Термин «биометалл» можно использовать как синоним металлического элемента, участвующего в функционировании биомолекулы . [16] следовательно, когда речь идет о биометаллах, можно учитывать и искусственные системы. Такие системы, как металлопротеины , металлопептиды и искусственные металлоферменты, являются примерами биомолекул, содержащих металлические элементы. Создание de novo структур, включающих металлы в функцию самой биомолекулы, осуществляется биомиметическим способом, но также и для обеспечения неестественной активности биомолекул . [17]
Биометаллы в медицине
[ редактировать ]Ионы металлов и соединения металлов часто используются в медицинских целях и диагностике. [18] В качестве лекарств можно использовать соединения, содержащие ионы металлов, например соединения лития и ауранофин . [19] [20] Соединения и ионы металлов также могут оказывать вредное воздействие на организм из-за токсичности некоторых типов металлов. [18] Например, мышьяк действует как мощный яд из-за своего эффекта ингибитора ферментов, нарушая выработку АТФ . [21] С другой стороны, проволоки Ni-Ti-Cu используются для искусственных мышц сердца. [22] а частицы железа и золота могут направлять магнитную доставку лекарств или разрушать опухолевые клетки. [22]
Более крупные биометаллические структуры (основанные на металлических элементах и сплавах ) в медицине можно разделить на три типа: волокна , объемные каркасы и нанотрубки . [23] А в некоторых случаях термин «биометалл» также используется для обозначения металлической системы, применение которой в биомедицине напрямую связано не с биохимической функцией биомолекул , а с биосовместимостью этих металлических систем. [24] Примерами являются каркасы из нержавеющей стали или титанового сплава для создания винтов или пластин для остеосинтеза , а также титановые объемы для точного моделирования костной ткани . [24] [22] В аналитических целях биометаллы можно использовать при магнитной сепарации различных материалов. [22]
Ссылки
[ редактировать ]- ^ Фейг А.Л., Уленбек О.К. (1999). «Роль ионов металлов в биохимии РНК» (PDF) . Серия монографий Колд-Спринг-Харбор . 37 : 287–320. Архивировано из оригинала (PDF) 1 марта 2021 г. Проверено 26 июля 2014 г.
- ^ Jump up to: а б с д и ж Марет В. (2018). «Металломика: наука о биометаллах и биометаллоидах» . В Арруде М.А. (ред.). Металломика . Достижения экспериментальной медицины и биологии. Том. 1055. Чам: Springer International Publishing. стр. 1–20. дои : 10.1007/978-3-319-90143-5_1 . ISBN 978-3-319-90143-5 . ПМИД 29884959 . S2CID 46997332 .
- ^ Банки Л, изд. (2013). Металломика и клетка . Дордрехт: Спрингер. ISBN 978-94-007-5560-4 .
- ^ Аггетт П.Дж. (август 1985 г.). «Физиология и обмен эссенциальных микроэлементов: очерк». Клиники эндокринологии и обмена веществ . 14 (3): 513–543. дои : 10.1016/S0300-595X(85)80005-0 . ПМИД 3905079 .
- ^ Кавальери Р.Р. (апрель 1997 г.). «Обмен йода и физиология щитовидной железы: современные представления». Щитовидная железа . 7 (2): 177–181. дои : 10.1089/thy.1997.7.177 . ПМИД 9133680 .
- ^ Jump up to: а б с д и ж г Фулкье Ф., Легран Д. (октябрь 2020 г.). «Биометаллы и гликозилирование у людей: врожденные нарушения гликозилирования проливают свет на решающую роль гомеостаза марганца по аппарату Гольджи» (PDF) . Biochimica et Biophysical Acta (BBA) – Общие предметы . 1864 (10): 129674. doi : 10.1016/j.bbagen.2020.129674 . ПМИД 32599014 . S2CID 220268697 .
- ^ Jump up to: а б с Шауль О (1 сентября 2002 г.). «Транспорт и функции магния в растениях: верхушка айсберга». Биометаллы . 15 (3): 307–321. дои : 10.1023/A:1016091118585 . ISSN 1572-8773 . ПМИД 12206396 . S2CID 32535554 .
- ^ Jump up to: а б с Член парламента Куахунко, Рамирес М.С., Толмаски М.Е. (февраль 2021 г.). «Цинк: многомерное воздействие на живые организмы» . Биомедицины . 9 (2): 208. doi : 10.3390/biomedicines9020208 . ПМЦ 7926802 . ПМИД 33671781 .
- ^ Jump up to: а б Тортора Г.Дж., Дерриксон Б. (2009). Основы анатомии и физиологии (12-е изд.). John Wiley & Sons, Inc. с. 437. ИСБН 978-0-7303-9202-6 . OCLC 1268517745 .
- ^ Уилк Н., Балог А., Марко Л., Бартоломеус Х., Мюллер Д.Н. (сентябрь 2019 г.). «Роль натрия в модуляции функции иммунных клеток». Обзоры природы. Нефрология . 15 (9): 546–558. дои : 10.1038/s41581-019-0167-y . ПМИД 31239546 . S2CID 195354083 .
- ^ Jump up to: а б с д Ван М, Чжэн Ц, Шэнь Ц, Го С (апрель 2013 г.). «Критическая роль калия в реакции растений на стресс» . Международный журнал молекулярных наук . 14 (4): 7370–7390. дои : 10.3390/ijms14047370 . ПМЦ 3645691 . ПМИД 23549270 .
- ^ Ямори М., Нджелекела М., Мтабаджи Дж., Ямори Ю., Бесшо К. (04 августа 2011 г.). «Гипертония, заболевания пародонта и потребление калия у некурящих и непьющих африканских женщин, не принимающих лекарств» . Международный журнал гипертонии . 2011 : 695719. doi : 10.4061/2011/695719 . ПМК 3150144 . ПМИД 21826260 .
- ^ Jump up to: а б Фасае К.Д., Аболаджи А.О., Фалойе Т.Р., Одунси А.Ю., Ойетайо Б.О., Энья Дж.И. и др. (сентябрь 2021 г.). «Металлобиология и терапевтическое хелатирование биометаллов (меди, цинка и железа) при болезни Альцгеймера: ограничения, текущие и будущие перспективы» . Журнал микроэлементов в медицине и биологии . 67 : 126779. doi : 10.1016/j.jtemb.2021.126779 . ПМИД 34034029 .
- ^ Jump up to: а б Нельсон Д.Л. (2021). Ленингер «Принципы биохимии» . [Sl]: У. Х. Фриман. ISBN 978-1-319-38147-9 . ОСЛК 1333920083 .
- ^ Jump up to: а б с Вайнберг Э.Д. (февраль 1996 г.). «Роль железа в раке». Европейский журнал профилактики рака . 5 (1): 19–36. JSTOR 45074238 . ПМИД 8664805 .
- ^ Уильямс, Д.; Чжан, X. (01 января 2019 г.). III - Типы биоматериалов (доступно онлайн 21 июня 2019 г., версия записи 21 июня 2019 г., ред.). Эльзевир. стр. Страницы 25–54. ISBN 9780128182918 .
- ^ Хаммер, Стефан С.; Найт, Андерс М.; Арнольд, Фрэнсис Х. (октябрь 2017 г.). «Дизайн и эволюция ферментов для неприродной химии» . Текущее мнение о зеленой и устойчивой химии . 7 : 23–30. дои : 10.1016/j.cogsc.2017.06.002 . ISSN 2452-2236 .
- ^ Информация о потребительских лекарствах AHFS (2014 г.). «Литий» . Медлайн . Национальная медицинская библиотека США.
- ^ Кин В.Ф., Харт Л., Бьюкенен В.В. (май 1997 г.). «Ауранофин» . Британский журнал ревматологии . 36 (5): 560–572. дои : 10.1093/ревматология/36.5.560 . ПМИД 9189058 .
- ^ Сингх А.П., Гоэл Р.К., Каур Т. (июль 2011 г.). «Механизмы, относящиеся к токсичности мышьяка» . Международная токсикология . 18 (2): 87–93. дои : 10.4103/0971-6580.84258 . ПМК 3183630 . ПМИД 21976811 .
- ^ Jump up to: а б с д Основы бионаноматериалов . Эльзевир. 2022. дои : 10.1016/c2020-0-00039-3 . ISBN 978-0-12-824147-9 .
- ^ «Наука, разработка и оценка нанобиоматериалов» . НаукаДирект . ISBN 978-0-08-100963-5 . Проверено 7 июня 2024 г.
- ^ Jump up to: а б Достижения в аддитивном производстве, искусственном интеллекте, природном и биопроизводстве . Эльзевир. 2023. doi : 10.1016/c2020-0-03877-6 . ISBN 978-0-323-91834-3 .